indicador de pH - pH indicator
Um indicador de pH é um composto químico halocrômico adicionado em pequenas quantidades a uma solução para que o pH ( acidez ou basicidade ) da solução possa ser determinado visualmente. Portanto, um indicador de pH é um detector químico de íons hidrônio (H 3 O + ) ou íons de hidrogênio (H + ) no modelo de Arrhenius . Normalmente, o indicador faz com que a cor da solução mude dependendo do pH. Os indicadores também podem mostrar mudanças em outras propriedades físicas; por exemplo, indicadores olfativos mostram mudança em seu odor . O valor de pH de uma solução neutra é 7,0 a 25 ° C ( condições padrão de laboratório ). Soluções com valor de pH abaixo de 7,0 são consideradas ácidas e soluções com valor de pH acima de 7,0 são básicas (alcalinas). Como a maioria dos compostos orgânicos de ocorrência natural são protólitos fracos, ácidos carboxílicos e aminas , os indicadores de pH encontram muitas aplicações em biologia e química analítica. Além disso, os indicadores de pH formam um dos três tipos principais de compostos indicadores usados em análises químicas. Para a análise quantitativa de cátions metálicos, o uso de indicadores complexométricos é preferido, enquanto a terceira classe de compostos, os indicadores redox , são usados em titulações envolvendo uma reação redox como base da análise.
Teoria
Por si só, os indicadores de pH são freqüentemente ácidos fracos ou bases fracas. O esquema geral de reação de um indicador de pH pode ser formulado como:
- HInd + H
2O ⇌ H
3O+
+ Ind-
Aqui, HInd representa a forma ácida e Ind - a base conjugada do indicador. A proporção deles determina a cor da solução e conecta a cor ao valor de pH. Indicadores de pH que são protólitos fracos, a equação de Henderson-Hasselbalch para eles pode ser escrita como:
- pH = p K a + log 10
[ Ind-
] / [Traseiro]
A equação, derivada da constante de acidez , afirma que quando o pH é igual ao valor p K a do indicador, ambas as espécies estão presentes na proporção de 1: 1. Se o pH estiver acima do valor de p K a , a concentração da base conjugada é maior do que a concentração do ácido e a cor associada à base conjugada predomina. Se o pH estiver abaixo do valor de p K a , o inverso é verdadeiro.
Normalmente, a mudança de cor não é instantânea no valor de p K a , mas existe uma faixa de pH onde uma mistura de cores está presente. Esta faixa de pH varia entre os indicadores, mas como regra geral, fica entre o valor de p K a mais ou menos um. Isso pressupõe que as soluções retêm sua cor enquanto pelo menos 10% das outras espécies persistirem. Por exemplo, se a concentração da base conjugada é 10 vezes maior que a concentração do ácido, sua proporção é 10: 1 e, conseqüentemente, o pH é p K a + 1. Por outro lado, se um excesso de 10 vezes do ácido ocorre em relação à base, a razão é 1:10 e o pH é p K a - 1.
Para obter a precisão ideal, a diferença de cor entre as duas espécies deve ser a mais clara possível, e quanto mais estreita a faixa de pH da mudança de cor, melhor. Em alguns indicadores, como a fenolftaleína , uma das espécies é incolor, enquanto em outros indicadores, como o vermelho de metila , ambas as espécies conferem uma cor. Embora os indicadores de pH funcionem de forma eficiente em sua faixa de pH designada, eles geralmente são destruídos nas extremidades da escala de pH devido a reações colaterais indesejadas.
Aplicativo
Os indicadores de pH são frequentemente empregados em titulações em química analítica e biologia para determinar a extensão de uma reação química . Devido à escolha subjetiva (determinação) da cor, os indicadores de pH são suscetíveis a leituras imprecisas. Para aplicações que requerem medição precisa de pH, um medidor de pH é freqüentemente usado. Às vezes, uma mistura de diferentes indicadores é usada para obter várias mudanças suaves de cor em uma ampla faixa de valores de pH. Esses indicadores comerciais (por exemplo, indicador universal e papéis Hydrion ) são usados quando apenas um conhecimento aproximado do pH é necessário.
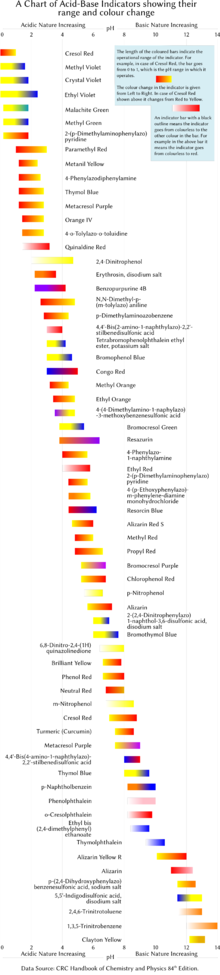
A tabela abaixo contém vários indicadores de pH comuns de laboratório. Os indicadores geralmente exibem cores intermediárias em valores de pH dentro da faixa de transição listada. Por exemplo, o vermelho de fenol exibe uma cor laranja entre pH 6,8 e pH 8,4. A faixa de transição pode mudar ligeiramente dependendo da concentração do indicador na solução e da temperatura na qual ele é usado. A figura à direita mostra indicadores com sua faixa de operação e mudanças de cor.
| Indicador | Cor de baixo pH | Transição de baixo custo |
Transição de ponta |
Cor de pH alto |
|---|---|---|---|---|
| Violeta de genciana ( violeta de metila 10B ) | amarelo | 0,0 | 2.0 | azul-violeta |
| Verde malaquita (primeira transição) | amarelo | 0,0 | 2.0 | verde |
| Verde malaquita (segunda transição) | verde | 11,6 | 14,0 | incolor |
| Azul timol (primeira transição) | vermelho | 1,2 | 2,8 | amarelo |
| Azul timol (segunda transição) | amarelo | 8,0 | 9,6 | azul |
| Amarelo metílico | vermelho | 2,9 | 4,0 | amarelo |
| Azul de bromofenol | amarelo | 3,0 | 4,6 | azul |
| Vermelho congo | azul-violeta | 3,0 | 5.0 | vermelho |
| Laranja de metila | vermelho | 3,1 | 4,4 | amarelo |
| Laranja de metila filtrada (primeira transição) | vermelho | 0,0 | 3,2 | cinza-púrpura |
| Laranja de metila filtrada (segunda transição) | cinza-púrpura | 3,2 | 4,2 | verde |
| Verde de bromocresol | amarelo | 3,8 | 5,4 | azul |
| Vermelho de metila | vermelho | 4,4 | 6,2 | amarelo |
| Roxo metílico | roxa | 4,8 | 5,4 | verde |
| Azolitmin (tornassol) | vermelho | 4,5 | 8,3 | azul |
| Bromocresol roxo | amarelo | 5,2 | 6,8 | roxa |
| Azul de bromotimol (primeira transição) | magenta | <0 | 6,0 | amarelo |
| Azul de bromotimol (segunda transição) | amarelo | 6,0 | 7,6 | azul |
| Vermelho de fenol | amarelo | 6,4 | 8,0 | vermelho |
| Vermelho neutro | vermelho | 6,8 | 8,0 | amarelo |
| Naftolftaleína | vermelho pálido | 7,3 | 8,7 | azul-esverdeado |
| Vermelho cresol | amarelo | 7,2 | 8,8 | roxo-avermelhado |
| Cresolftaleína | incolor | 8,2 | 9,8 | roxa |
| Fenolftaleína (primeira transição) | laranja-avermelhado | <0 | 8,3 | incolor |
| Fenolftaleína (segunda transição) | incolor | 8,3 | 10,0 | roxo Rosa |
| Fenolftaleína (terceira transição) | roxo Rosa | 12,0 | 13,0 | incolor |
| Timolftaleína (primeira transição) | vermelho | <0 | 9,3 | incolor |
| Timolftaleína (segunda transição) | incolor | 9,3 | 10,5 | azul |
| Alizarine Yellow R | amarelo | 10,2 | 12,0 | vermelho |
| Índigo carmim | azul | 11,4 | 13,0 | amarelo |
Indicador universal
| faixa de pH | Descrição | Cor |
|---|---|---|
| 1-3 | Ácido forte | vermelho |
| 3 - 6 | Ácido fraco | Laranja amarelo |
| 7 | Neutro | Verde |
| 8-11 | Base fraca | Azul |
| 11-14 | Base forte | Violeta / Indigo |
Medição precisa de pH
Um indicador pode ser usado para obter medições bastante precisas de pH medindo a absorbância quantitativamente em dois ou mais comprimentos de onda. O princípio pode ser ilustrado tomando o indicador como um ácido simples, HA, que se dissocia em H + e A - .
- HA ⇌ H + + A -
O valor da constante de dissociação do ácido , p K a , deve ser conhecido. As absorbâncias molares , ε HA e ε A - das duas espécies HA e A - nos comprimentos de onda λ x e λ y também devem ter sido determinadas por experimento anterior. Supondo que a lei de Beer seja obedecida, as absorbâncias medidas A x e A y nos dois comprimentos de onda são simplesmente a soma das absorbâncias devidas a cada espécie.
Estas são duas equações nas duas concentrações [HA] e [A - ]. Uma vez resolvido, o pH é obtido como
Se as medições forem feitas em mais de dois comprimentos de onda, as concentrações [HA] e [A - ] podem ser calculadas por mínimos quadrados lineares . Na verdade, todo um espectro pode ser usado para esse propósito. O processo é ilustrado para o indicador verde de bromocresol . O espectro observado (verde) é a soma dos espectros de HA (ouro) e de A - (azul), ponderados pela concentração das duas espécies.
Quando um único indicador é usado, este método é limitado a medições na faixa de pH p K a ± 1, mas esta faixa pode ser estendida usando misturas de dois ou mais indicadores. Como os indicadores têm espectros de absorção intensos, a concentração do indicador é relativamente baixa e o próprio indicador é considerado como tendo um efeito insignificante no pH.
Ponto equivalente
Em titulações ácido-base, um indicador de pH inadequado pode induzir uma mudança de cor na solução que contém o indicador antes ou depois do ponto de equivalência real. Como resultado, diferentes pontos de equivalência para uma solução podem ser concluídos com base no indicador de pH usado. Isso ocorre porque a menor mudança de cor da solução contendo o indicador sugere que o ponto de equivalência foi alcançado. Portanto, o indicador de pH mais adequado tem uma faixa de pH eficaz, onde a mudança na cor é aparente, que abrange o pH do ponto de equivalência da solução sendo titulada.
Indicadores de pH de ocorrência natural
Muitas plantas ou partes de plantas contêm produtos químicos da família de compostos das antocianinas naturalmente coloridas . Eles são vermelhos em soluções ácidas e azuis em soluções básicas. As antocianinas podem ser extraídas com água ou outros solventes de uma infinidade de plantas coloridas são partes de plantas, incluindo folhas ( repolho roxo ); flores ( gerânio , papoula ou pétalas de rosa ); bagas ( mirtilos , groselha preta ); e caules ( ruibarbo ). Extrair antocianinas de plantas domésticas, especialmente repolho roxo , para formar um indicador de pH bruto é uma demonstração introdutória de química popular.
Tornassol , usado por alquimistas na Idade Média e ainda disponível, é um indicador de pH de ocorrência natural feito de uma mistura de espécies de líquen , particularmente Roccella tinctoria . A palavra tornassol vem literalmente de 'musgo colorido' em nórdico antigo (ver Litr ). A cor muda entre vermelho em soluções ácidas e azul em álcalis. O termo 'teste de tornassol' tornou-se uma metáfora amplamente usada para qualquer teste que pretenda distinguir com autoridade entre alternativas.
As flores de Hydrangea macrophylla podem mudar de cor dependendo da acidez do solo. Em solos ácidos, ocorrem reações químicas no solo que disponibilizam o alumínio para essas plantas, tornando as flores azuis. Em solos alcalinos, essas reações não podem ocorrer e, portanto, o alumínio não é absorvido pela planta. Como resultado, as flores permanecem rosadas.
Outro indicador de pH natural útil é a especiaria açafrão . É amarelo quando exposto a ácidos e marrom avermelhado quando na presença de um álcali .
| Indicador | Cor de baixo pH | Cor de pH alto |
|---|---|---|
| Flores de hortênsia | azul | rosa para roxo |
| Antocianinas | vermelho | azul |
| Litmus | vermelho | azul |
| Açafrão | amarelo | marrom avermelhado |
Couve-flor roxa embebida em bicarbonato de sódio (à esquerda) e vinagre (à direita). A antocianina atua como um indicador de pH.
Veja também
Referências
- Longa lista de indicadores
- "Lista completa de indicadores" (PDF) (em francês). (57,3 KiB )




![{\ displaystyle {\ begin {alinhados} A_ {x} & = [{\ ce {HA}}] \ varepsilon _ {{\ ce {HA}}} ^ {x} + [{\ ce {A-}} ] \ varejpsilon _ {{\ ce {A -}}} ^ {x} \\ A_ {y} & = [{\ ce {HA}}] \ varepsilon _ {{\ ce {HA}}} ^ {y } + [{\ ce {A -}}] \ varepsilon _ {{\ ce {A -}}} ^ {y} \ end {alinhado}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/407bba3b954782cbec25c32d99393bf282c2c36d)
![{\ displaystyle \ mathrm {pH} = \ mathrm {p} K _ {\ mathrm {a}} + \ log {\ frac {[{\ ce {A -}}]} {[{\ ce {HA}}] }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2ed476e8f78a1980748a81ec195978b60032411f)




