Periodate - Periodate
 O íon metaperiodato
|
|
 O íon ortoperiodato
|
|
| Nomes | |
|---|---|
|
Nome IUPAC sistemático
tetraoxoiodato (1−) hexaoxoiodato (5−) |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
| UNII | |
|
|
|
|
| Propriedades | |
| IO 4 - ou IO 6 5- | |
| Ácido conjugado | Ácido periódico |
| Compostos relacionados | |
|
Outros ânions
|
Perclorato Perbromato Permanganato |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
| Referências da Infobox | |
Periodato / p ə r aɪ . ə d eɪ t / é um ânion composto de iodo e oxigênio . É um dos vários oxiânions de iodo e é o mais alto da série, com o iodo existindo no estado de oxidação +7. Ao contrário de outros perhalogenatos, como perclorato , pode existir em duas formas: metaperiodato IO-
4e ortoperiodato IO5−
6. A este respeito, é comparável ao íon telurato do grupo adjacente . Ele pode se combinar com vários contra-íons para formar periodatos , que também podem ser considerados sais do ácido periódico .
Os periodatos foram descobertos por Heinrich Gustav Magnus e CF Ammermüller; quem primeiro sintetizou o ácido periódico em 1833.
Síntese
Classicamente, o periodato era mais comumente produzido na forma de periodato de hidrogênio de sódio (Na 3 H 2 IO 6 ). Este está disponível comercialmente, mas também pode ser produzido pela oxidação de iodatos com cloro e hidróxido de sódio . Ou, da mesma forma, de iodetos por oxidação com bromo e hidróxido de sódio:
- NaIO 3 + Cl 2 + 4 NaOH → Na 3 H 2 IO 6 + 2 NaCl + H 2 O
- NaI + 4 Br 2 + 10 NaOH → Na 3 H 2 IO 6 + 8 NaBr + 4 H 2 O
A produção em escala industrial moderna envolve a oxidação eletroquímica de iodatos, em um ânodo de PbO 2 , com o seguinte potencial de eletrodo padrão :
Os metaperiodatos são tipicamente preparados pela desidratação do hidrogênio periodato de sódio com ácido nítrico , ou por desidratação do ácido ortoperiódico por aquecimento a 100 ° C sob vácuo.
- Na 3 H 2 IO 6 + 2 HNO 3 → NaIO 4 + 2 NaNO 3 + 2 H 2 O
- H 5 IO 6 → HIO 4 + 2 H 2 O
Eles também podem ser gerados diretamente a partir de iodatos por tratamento com outros agentes oxidantes fortes, como hipocloritos :
Formas e interconversão
O periodato pode existir em uma variedade de formas em meio aquoso, com o pH sendo um fator de controle. O ortoperiodato tem várias constantes de dissociação de ácido .
H 5 IO 6 ⇌ H
4IO-
6+ H + p K a = 3,29 H
4IO-
6⇌ H
3IO2−
6+ H + p K a = 8,31 H
3IO2−
6⇌ H
2IO3−
6+ H + p K a = 11,60
As formas orto e metaperiodato também existem em equilíbrio.
-
H
4IO-
6⇌ IO-
4+ 2 H 2 O, K = 29
Por esta razão, o ortoperiodato é às vezes referido como o di- hidrato de metaperiodato, escrito IO-
4· 2H 2 O ; no entanto, esta descrição não é estritamente precisa, pois a cristalografia de raios-X de H 5 IO 6 mostra 5 grupos I – OH equivalentes.
Em extremos de pH, espécies adicionais podem se formar. Sob condições básicas, uma reação de desidratação pode ocorrer para formar o diperiodato (às vezes referido como mesoperiodato).
- 2 H
3IO2−
6⇌ H
2eu
2O4−
10+ 2 H 2 O, K = 820
Sob condições fortemente ácidas, o ácido periódico pode ser protonado para dar o cátion ortoperiodônio .
-
H
6IO+
6⇌ H 5 IO 6 + H + , p K a = −0,8
Estrutura e ligação
Tanto no orto- quanto no metaperiodato, o iodo é hipervalente , pois forma mais ligações do que seria classicamente permitido. Isso foi explicado em termos de ligações dativas , confirmando a ausência de ligações duplas nessas moléculas.
As estruturas exatas variam dependendo dos contra-íons, no entanto, em média, os ortoperiodatos adotam uma geometria octaédrica levemente deformada com difração de raios-X mostrando comprimentos de ligação I – O de 1,89 Å . Os metaperiodatos adotam uma geometria tetraédrica distorcida com uma distância I – O média de 1,78 Å.
Reações
Reações de clivagem
Periodatos podem clivar ligações carbono-carbono em uma variedade de alcanos 1,2-difuncionalizados. O exemplo mais comum disso é a clivagem do diol , que também foi a primeira a ser descoberta ( reação de Malaprade ). Além de dióis , os periodatos podem clivar 1,2-hidroxicetonas , 1,2-dicetonas , α-cetoácidos , α-hidroxiácidos , aminoácidos , 1,2-aminoálcoois , 1,2-diaminas e epóxidos para dar aldeídos, cetonas e ácidos carboxílicos.
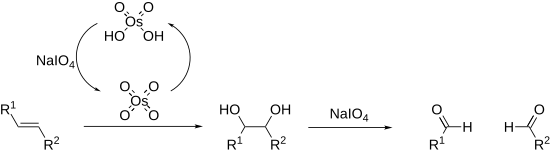
Os alcenos também podem ser oxidados e clivados na oxidação de Lemieux-Johnson . Isso usa um carregamento catalítico de tetróxido de ósmio que é regenerado in situ pelo periodato. O processo geral é equivalente ao da ozonólise .
As reações de clivagem ocorrem por meio de um intermediário cíclico denominado éster de periodato. A formação deste pode ser afetada pelo pH e temperatura, mas é mais fortemente afetada pela geometria do substrato, com cis- dióis reagindo significativamente mais rápido do que trans- dióis. As reações são exotérmicas e são tipicamente realizadas a 0 ° C. Como os sais de periodato são apenas prontamente solúveis em água, as reações são geralmente realizadas em meio aquoso. Quando a solubilidade é um problema, pode-se usar ácido periódico, pois é solúvel em álcoois; catalisadores de transferência de fase também são eficazes em misturas de reação bifásica . Em casos extremos, o periodato pode ser trocado por tetraacetato de chumbo, que reage de maneira semelhante e é solúvel em solventes orgânicos ( oxidação Criegee ).
A clivagem de periodato é frequentemente utilizada em bioquímica molecular para fins de modificação de anéis de sacarídeo , já que muitos açúcares de cinco e seis membros têm dióis vicinais . Historicamente, também foi usado para determinar a estrutura dos monossacarídeos.
A clivagem de periodato pode ser realizada em escala industrial para formar amido dialdeído que tem uso na produção de papel .
Reações de oxidação
Os periodatos são poderosos agentes oxidantes . Eles podem oxidar catecol a 1,2-benzoquinona e hidroquinona a 1,4-benzoquinona . Os sulfetos podem ser efetivamente oxidados a sulfóxidos . Os periodatos são suficientemente poderosos para gerar outros oxidantes inorgânicos fortes, como permanganato , tetróxido de ósmio e tetróxido de rutênio .
Nicho usa
Os periodatos são gravadores altamente seletivos para certos óxidos à base de rutênio .
Vários agentes de coloração usados em microscopia são baseados em periodato (por exemplo , ácido periódico - coloração de Schiff e coloração de Jones )
Periodatos também têm sido usados como agentes oxidantes para uso em pirotecnia . Em 2013, o Exército dos EUA anunciou que iria substituir os produtos químicos prejudiciais ao meio ambiente, nitrato de bário e perclorato de potássio, por metaperiodato de sódio para uso em suas munições traçadoras.
Outros oxiânions
O periodato é parte de uma série de oxiânions nos quais o iodo pode assumir estados de oxidação de -1, +1, +3, +5 ou +7. Vários óxidos de iodo neutros também são conhecidos.
| Estado de oxidação de iodo | -1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| Nome | iodeto | hipoiodito | iodito | iodato | periodato |
| Fórmula | Eu - | IO - |
IO- 2 |
IO- 3 |
IO- 4ou IO5− 6 |
| Estrutura |

|
|
|