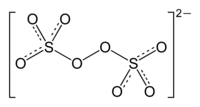
Peroxidisulfato - Peroxydisulfate

O íon peroxidissulfato , S
2O2−
8, é um oxiânion . É comumente referido como íon persulfato ou ânions peroxodissulfato , mas este termo também se refere ao íon peroxomonossulfato , SO2−
5.Neste estado de oxidação de ambos o enxofre é +6, também conhecido como ácido de Marshall. Aproximadamente 500.000 toneladas de sais contendo este ânion são produzidas anualmente. Os sais importantes incluem persulfato de sódio (Na 2 S 2 O 8 ), persulfato de potássio (K 2 S 2 O 8 ) e persulfato de amônio ((NH 4 ) 2 S 2 O 8 ). Esses sais são sólidos incolores e solúveis em água que são oxidantes fortes.
Formulários
Sais de peroxidissulfato são usados principalmente para iniciar a polimerização de vários alquenos , incluindo estireno , acrilonitrila e fluoroalcenos. A polimerização é iniciada pela homólise do peroxidissulfato:
- [O 3 SO – OSO 3 ] 2− ⇌ 2 [SO 4 ] • -
Além disso, o peroxidissulfato de sódio pode ser usado para remediação de solo e água subterrânea , tratamento de água e esgoto e corrosão de cobre em placas de circuito.
Também tem sido usado para produzir clareadores e alvejantes para cabelos, medicamentos, celofane, borracha, sabonetes, detergentes, papéis adesivos, tinturas para têxteis e na fotografia.
Além de suas principais aplicações comerciais, o peroxidisulfato participa de reações de interesse no laboratório:
- Oxidação de persulfato de Elbs
- Oxidação de Ag + para Ag 2+
Referências
- ^ a b c Shafiee, Saiful Arifin; Aarons, Jolyon; Hamzah, Hairul Hisham (2018). "Electroreduction of Peroxodisulfate: A Review of a Complicated Reaction" . Journal of the Electrochemical Society . ECS. 165 (13): H785 – H798. doi : 10.1149 / 2.1161811jes .
- ^ Wacławek, S., Lutze, HV, Grübel, K., Padil, VVT, Černík, M., Dionysiou, DD (2017) (2017). "Química de persulfatos em tratamento de água e esgoto: Uma revisão". Chemical Engineering Journal . 330 : 44–62. doi : 10.1016 / j.cej.2017.07.132 .CS1 maint: multiple names: authors list (link)