Fenóis - Phenols
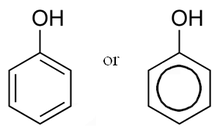
Em química orgânica , os fenóis , às vezes chamados de fenólicos , são uma classe de compostos químicos que consistem em um ou mais grupos hidroxila ( -O H ) ligados diretamente a um grupo de hidrocarboneto aromático . O mais simples é o fenol , C
6H
5OH . Os compostos fenólicos são classificados como fenóis ou polifenóis simples com base no número de unidades fenólicas na molécula.
Os fenóis são sintetizados industrialmente e produzidos por plantas e microrganismos.
Propriedades
Acidez
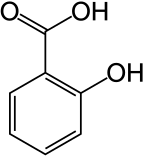
Os fenóis são mais ácidos do que os álcoois típicos. A acidez do grupo hidroxila nos fenóis é comumente intermediária entre a dos álcoois alifáticos e os ácidos carboxílicos (seu pK a está geralmente entre 10 e 12). A desprotonação de um fenol forma um íon fenolato ou íon fenóxido negativo correspondente , e os sais correspondentes são chamados de fenolatos ou fenóxidos ( arilóxidos de acordo com o IUPAC Gold Book ).
Condensação com aldeídos e cetonas
Os fenóis são suscetíveis a substituições aromáticas eletrofílicas . A condensação com formaldeído dá materiais resinosos, a famosa baquelita .
Outra substituição eletrofílica aromática em escala industrial é a produção de bisfenol A , que é produzido pela condensação com acetona .
C-alquilação com alquenos
O fenol é prontamente alquilado nas posições orto usando alquenos na presença de um ácido de Lewis, como o fenóxido de alumínio:
- CH 2 = CR 2 + C 6 H 5 OH → R 2 CHCH 2 -2-C 6 H 4 OH
Mais de 100.000 toneladas de terc-butil fenóis são produzidos anualmente (ano: 2000) dessa forma, usando isobutileno (CH 2 = CMe 2 ) como agente alquilante. Especialmente importante é o 2,6-ditert-butilfenol , um antioxidante versátil .
Outras reações
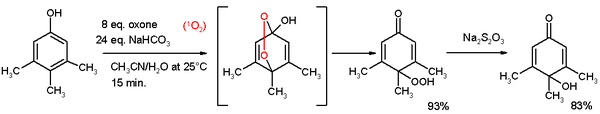
Os fenóis sofrem esterificação . Os ésteres de fenol são ésteres ativos , com tendência à hidrólise. Os fenóis são espécies reativas à oxidação . Clivagem oxidativa, por exemplo, clivagem de 1,2-dihidroxibenzeno em monometiléster de ácido 2,4 hexadienodioico com oxigênio, cloreto de cobre em piridina Desaromatização oxidativa em quinonas, também conhecida como reação de Teuber . e oxone . Na reação descrita abaixo, 3,4,5-trimetilfenol reage com oxigênio singlete gerado a partir de oxona / carbonato de sódio em uma mistura de acetonitrila / água para um para-peroxiquinol. Este hidroperóxido é reduzido a quinol com tiossulfato de sódio .
Os fenóis são oxidados a hidroquinonas na oxidação do persulfato de Elbs .
Reação de naftóis e hidrazinas e bissulfito de sódio na síntese de carbazol de Bucherer
Síntese
Muitos fenóis de interesse comercial são preparados pela elaboração de fenol ou cresóis . Eles são tipicamente produzidos pela alquilação de benzeno / tolueno com propileno para formar cumeno e depois O
2é adicionado com H
2TÃO
4para formar fenol ( processo Hock ). Além das reações acima, muitas outras reações mais especializadas produzem fenóis:
- rearranjo de ésteres o rearranjo de Fries
- rearranjo de N- fenilhidroxilaminas no rearranjo Bamberger
- desalquilação de éteres fenólicos
- redução de quinonas
- substituição de uma amina aromática por um grupo hidroxila com água e bissulfeto de sódio na reação de Bucherer
- decomposição térmica de sais de aril diazônio , os sais são convertidos em fenol
- pela oxidação de aril silanos - uma variação aromática da oxidação de Fleming-Tamao
Classificação

Existem vários esquemas de classificação . Um esquema comumente usado é baseado no número de carbonos e foi desenvolvido por Jeffrey Harborne e Simmonds em 1964 e publicado em 1980:
| Fenol | o composto original, usado como desinfetante e para síntese química |
| Bisfenol A | e outros bisfenóis produzidos a partir de cetonas e fenol / cresol |
| BHT | (hidroxitolueno butilado) - um antioxidante solúvel em gordura e aditivo alimentar |
| 4-nonilfenol | um produto da decomposição de detergentes e nonoxinol-9 |
| Ortofenil fenol | um fungicida usado para encerar frutas cítricas |
| Ácido Pícrico | (trinitrofenol) - um material explosivo |
| Fenolftaleína | indicador de pH |
| Xilenol | usado em anti-sépticos e desinfetantes |
Medicamentos e produtos naturais bioativos
| tirosina | um dos 20 aminoácidos padrão |
| L-DOPA | pró-droga dopamina usada para tratar a doença de Parkinson |
| propofol | agente anestésico intravenoso de curta ação |
| vitamina K hidroquinona | agente de coagulação do sangue que converte |
| levotiroxina (L-tiroxina) | Medicamento mais vendido para tratar a deficiência do hormônio tireoidiano. |
| amoxicilina | Antibiótico mais vendido |
| estradiol | o principal hormônio sexual feminino |
Referências
- ^ Hättenschwiler, Stephan; Vitousek, Peter M. (2000). "O papel dos polifenóis na ciclagem de nutrientes do ecossistema terrestre". Tendências em Ecologia e Evolução . 15 (6): 238–243. doi : 10.1016 / S0169-5347 (00) 01861-9 . PMID 10802549 .
- ^ a b Fiege H; Voges HW; Hamamoto T; Umemura S; Iwata T; Miki H; Fujita Y; Buysch HJ; Garbe D. (2000). "Derivados de fenol". Enciclopédia de Química Industrial de Ullmann . Weinheim: Wiley-VCH. doi : 10.1002 / 14356007.a19_313 .
- ^ Ácido 2,4-hexadienodioico, éster monometílico, (Z, Z) - Organic Syntheses , Coll. Vol. 8, p.490 (1993); Vol. 66, p.180 (1988) Artigo
- ^ "2,5-Ciclohexadieno-1,4-diona, 2,3,5-trimetil". Sínteses orgânicas . 52 : 83. 1972.
- ^ Carreño, M. Carmen; González-López, Marcos; Urbano, Antonio (2006). "Oxidative De-aromatization of para-Alkyl Phenols into para-Peroxyquinols and para-Quinols Mediated by Oxone as a Source of Singlet Oxygen". Angewandte Chemie International Edition . 45 (17): 2737–2741. doi : 10.1002 / anie.200504605 . PMID 16548026 .
- ^ HE Ungnade, EF Orwoll (1943). "3-Bromo-4-hidroxitolueno". Sínteses orgânicas . 23 : 11. doi : 10.15227 / orgsyn.023.0011 .
- ^ Bracegirdle, Sonia; Anderson, Edward A. (2010). "Oxidação de arilsilano - novas rotas para aromáticos hidroxilados" . Chem. Com . 46 (20): 3454–6. doi : 10.1039 / b924135c . PMID 20582346 . S2CID 31736757 .
- ^ a b Wilfred Vermerris e Ralph Nicholson. Phenolic Compound Biochemistry Springer, 2008
- ^ Harborne, JB (1980). "Plantas fenólicas". Em Bell, EA; Charlwood, BV (eds.). Enciclopédia de Fisiologia Vegetal, volume 8 Produtos Vegetais Secundários . Berlin Heidelberg New York: Springer-Verlag. pp. 329–395.