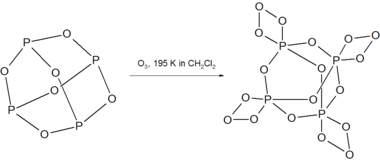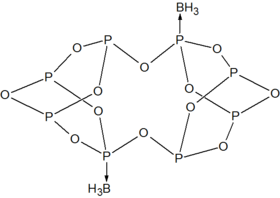Trióxido de fósforo - Phosphorus trioxide
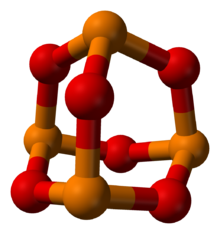 Fósforo em laranja, oxigênio em vermelho
|
|

|
|
| Nomes | |
|---|---|
| Outros nomes | |
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100.032.414 |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| P 4 O 6 | |
| Massa molar | 219,88 g mol −1 |
| Aparência | cristais monoclínicos incolores ou líquido |
| Densidade | 2,135 g / cm 3 |
| Ponto de fusão | 23,8 ° C (74,8 ° F; 296,9 K) |
| Ponto de ebulição | 173,1 ° C (343,6 ° F; 446,2 K) |
| reage | |
| Acidez (p K a ) | 9,4 |
| Estrutura | |
| Veja o Texto | |
| 0 | |
| Perigos | |
| Tóxico (T +) | |
| NFPA 704 (diamante de fogo) | |
| Compostos relacionados | |
|
Outros ânions
|
Trissulfeto de fósforo |
|
Outros cátions
|
Trióxido de dinitrogênio Trióxido de arsênio Trióxido de antimônio |
|
Compostos relacionados
|
Pentóxido de fósforo Ácido fosforoso |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
Trióxido de fósforo é o composto químico de fórmula molecular P 4 O 6 . Embora a fórmula molecular sugira o nome hexóxido de tetrafósforo, o nome trióxido de fósforo precedeu o conhecimento da estrutura molecular do composto e seu uso continua até hoje. Este sólido incolor está estruturalmente relacionado ao adamantano . É formalmente o anidrido do ácido fosforoso , H 3 PO 3 , mas não pode ser obtido pela desidratação do ácido. Sólido branco que derrete à temperatura ambiente, é ceroso, cristalino e altamente tóxico, com odor de alho.
Preparação
É obtido pela combustão do fósforo em um fornecimento limitado de ar a baixa temperatura.
- P 4 + 3 O 2 → P 4 O 6
Os subprodutos incluem o subóxido de fósforo vermelho.
Propriedades quimicas
O trióxido de fósforo reage com a água para formar ácido fosforoso , refletindo o fato de ser o anidrido desse ácido.
- P 4 O 6 + 6 H 2 O → 4 H 3 PO 3
Reage com cloreto de hidrogênio para formar H 3 PO 3 e tricloreto de fósforo .
- P 4 O 6 + 6 HCl → 2 H 3 PO 3 + 2 PCl 3
Com cloro ou bromo forma o haleto de fosforila correspondente , e reage com iodo em um tubo selado para formar tetraiodeto de difósforo .
P 4 O 6 reage com ozônio a 195 K para dar o composto instável P 4 O 18 .
P 4 O 18 decompõe-se acima de 238 K em solução com a liberação de gás O 2 . A decomposição do P 4 O 18 seco é explosiva.
Em uma reação de desproporção , P 4 O 6 é convertido na espécie P (III) P (V) mista P 4 O 8 quando aquecido em um tubo selado a 710 K, com o produto secundário sendo fósforo vermelho.
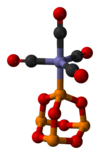
Como um ligante
P 4 O 6 é um ligante para metais de transição, comparável ao fosfito . Um complexo ilustrativo é P 4 O 6 · Fe (CO) 4 . Com BH 3 , um aduto dimérico é produzido: