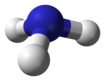
Hidreto de Pnictogen - Pnictogen hydride
Hidretos grupo do nitrogênio ou pnictides de hidrogénio são compostos binários de hidrogénio com grupo do nitrogênio ( / p n ɪ k t ə dʒ ə n / ou / n ɪ k t ə dʒ ə n / ; a partir do grego clássico : πνῑγω "para sufocar" e -gen , átomos "geradores") (elementos do grupo 15: nitrogênio , fósforo , arsênio , antimônio e bismuto ) ligados covalentemente ao hidrogênio .
Triidridos de pnictogênicos
A série mais simples tem a fórmula química XH 3 (menos comumente H 3 X), com X representando qualquer um dos pnictogênios. Eles assumem a estrutura piramidal (em oposição ao arranjo trigonal planar dos hidretos do grupo 13 ) e, portanto, são polares. Esses triidridos de pnictogênicos são geralmente cada vez mais instáveis e venenosos com elementos mais pesados.
Tal como os simples halogenetos de hidrogénio e calcogenetos , os hidretos de grupo do nitrogênio são água - solúvel . Ao contrário de outros hidretos, como o sulfeto de hidrogênio e o fluoreto de hidrogênio , que formam soluções aquosas ácidas, a amônia se dissolve na água para formar o hidróxido de amônio que é básico (formando um íon hidróxido em oposição ao hidrônio ). A fosfina também é solúvel em água. Arsine e stibine são menos, e não se sabe se bismuthine é.
| Nomes compostos | Fórmula química | Geometria | Modelo de preenchimento de espaço |
|---|---|---|---|
| hidreto de nitrogênio amônia (azano) |
NH 3 |  |

|
| hidreto de fósforo fosfina (fosfano) |
PH 3 | 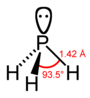 |

|
| hidreto de arsênio arsina (arsano) |
AsH 3 |  |

|
| hidreto de antimônio estibina (estibano) |
SbH 3 |  |

|
| hidreto de bismuto bismutina (bismutano) |
BiH 3 |  |

|
Seguem algumas propriedades dos tri-hidretos de pnictogênio:
| Propriedade | NH 3 | PH 3 | AsH 3 | SbH 3 | BiH 3 |
|---|---|---|---|---|---|
| Ponto de fusão (° C) | -77,8 | -133,5 | -116,3 | -88 | ? |
| Ponto de ebulição (° C) | -34,5 | -87,5 | -62,4 | -18,4 | 16,8 (extrapolado) |
| Densidade do líquido (g / cm 3 ) | 0,683 (−34 ° C) | 0,746 (−90 ° C) | 1,640 (−64 ° C) | 2,204 (−18 ° C) | ? |
| Δ H° f/ kJ mol −1 |
-46,1 | -9,6 (?) | +66,4 | +145,1 | +277,8 |
| Distância (X – H) / pm | 101,7 | 141,9 | 151,9 | 170,7 | 177,59 |
| Ângulo H – X – H | 107,8 ° | 93,6 ° | 91,8 ° | 91,3 ° | 90,48 ° |
Esses gases não têm cheiro na forma pura, ganhando-o ao entrar em contato com o ar. A amônia tem um odor intenso e infame, semelhante a urina e / ou peixe , comumente resultante da decomposição da uréia . A fosfina tem cheiro de peixe ou alho, e a estibina tem cheiro de ovo podre, semelhante ao sulfeto de hidrogênio e seleneto .
Tetraidridos dipnictogênicos
| Nomes compostos | Fórmula química | Geometria | Modelo de preenchimento de espaço |
|---|---|---|---|
| dinitrogênio hidreto hidrazina (diazano) |
N 2 H 4 |  |

|
| difosfina hidreto difosforado ( difosfano ) |
P 2 H 4 | 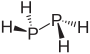 |

|
| hidreto diarsênico diarsina ( diarsano ) |
Como 2 H 4 |  |

|
Propriedades
Todos os peptídeos de hidrogênio saturados de cadeia linear seguem a fórmula X n H n + 2 .
A amônia é produzida industrialmente em maior escala entre todos os compostos. Como a água, a ligação de hidrogênio resulta em um alto ponto de fusão e ebulição em comparação com os outros hidretos de pnictogênio, embora 26% sejam perdidos na fusão, outros 7% quando o líquido é aquecido até a ebulição e os 67% restantes na ebulição. Outros efeitos da ligação de hidrogênio são uma alta constante dielétrica, bem como baixos valores de densidade, viscosidade e condutividade elétrica. Como a água, é um solvente ionizante excelente e muito usado. Mais de vinte outros hidretos de nitrogênio são conhecidos, sendo os mais importantes a hidrazina (N 2 H 4 ) e a azida de hidrogênio (HN 3 ). A hidrazina tem propriedades físicas que são notavelmente semelhantes às da água: seus pontos de fusão e ebulição são 2,0 ° C e 113,5 ° C, a densidade do sólido a -5 ° C é 1,146 g / cm 3 , enquanto a do líquido a 25 ° C é de 1,00 g / cm 3 . Os azanos são uma série que inclui amônia, hidrazina e triazano .
A fosfina, um gás tóxico e incolor, é o hidreto de fósforo mais estável e é o primeiro da série de polifosfano de cadeia linear homóloga P n H n +2 ( n = 1-9) que se torna cada vez mais instável termicamente à medida que n aumenta. Outras séries de polifosfanos cíclicos e condensados são conhecidas, de P n H n a P n H n −18 , totalizando 85 fosfanos conhecidos em 1997. Insolúvel em água, mas solúvel em líquidos orgânicos (bem como dissulfeto de carbono e ácido tricloroacético ), fosfina é um forte agente redutor.
Arsine, stibine e bismuthine são gases altamente tóxicos, termicamente instáveis e incolores. Nenhuma ligação de hidrogênio apreciável é encontrada na fosfina, arsina, estibina ou bismutina, e não há tendência apreciável para se dissociar como a amônia em MH+
4e MH-
2(M = P, As, Sb, Bi). Os hidretos de pnictogênio tornam-se mais densos no grupo e os comprimentos de ligação M – H aumentam, enquanto o ângulo de ligação H – M – H diminui ligeiramente. As entalpias padrão de formação refletem o aumento da instabilidade térmica ao longo do grupo. O arsino se decompõe em arsênio e hidrogênio a 250–300 ° C, o estibino em antimônio e hidrogênio em temperatura ambiente e a bismutina em bismuto e hidrogênio acima de −45 ° C. A arsina e a estibina são facilmente oxidadas em arsênio ou trióxido de antimônio e água; uma reação semelhante ocorre com o enxofre ou o selênio . A reação com metais em temperaturas elevadas leva a arsenetos e antimonídeos. Alguns hidretos inferiores são conhecidos, como As 2 H 4 , mas eles são ainda mais instáveis e suas propriedades são desconhecidas.
Imidogênio , um radical composto por um átomo de hidrogênio e um átomo de nitrogênio (NH), pode ser classificado como um hidreto de pnictogênio.
Veja também
Referências
Bibliografia
- Greenwood, Norman N .; Earnshaw, Alan (1997). Química dos Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.