Sulfato de potássio - Potassium sulfate
 Arcanite
|
|
|
|
| Nomes | |
|---|---|
| Outros nomes
Sulfato de potássio
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard |
100.029.013 |
| Número E | E515 (i) (reguladores de acidez, ...) |
| KEGG | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| K 2 SO 4 | |
| Massa molar | 174,259 g / mol |
| Aparência | Sólido branco |
| Odor | inodoro |
| Densidade | 2,66 g / cm 3 |
| Ponto de fusão | 1.069 ° C (1.956 ° F; 1.342 K) |
| Ponto de ebulição | 1.689 ° C (3.072 ° F; 1.962 K) |
| 111 g / L (20 ° C) 120 g / L (25 ° C) 240 g / L (100 ° C) |
|
| Solubilidade | ligeiramente solúvel em glicerol insolúvel em acetona , álcool , CS 2 |
| −67,0 · 10 −6 cm 3 / mol | |
|
Índice de refração ( n D )
|
1.495 |
| Estrutura | |
| ortorrômbico | |
| Perigos | |
| Riscos principais | Irritante |
| Ficha de dados de segurança | MSDS externo |
| Frases R (desatualizado) | R22 |
| Frases S (desatualizado) | S36 |
| Ponto de inflamação | Não inflamável |
| Dose ou concentração letal (LD, LC): | |
|
LD 50 ( dose mediana )
|
6.600 mg / kg (oral, rato) |
| Compostos relacionados | |
|
Outros ânions
|
Potássio selenato de potássio telurato |
|
Outros cátions
|
Sulfato de lítio Sulfato de sódio Sulfato de rubídio Sulfato de césio |
|
Compostos relacionados
|
Hidrogenossulfato de potássio Sulfito de potássio Bissulfito de potássio Persulfato de potássio |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
Sulfato de potássio (EUA) ou sulfato de potássio (Reino Unido), também chamado de sulfato de potássio (SOP), arcanita ou potássio arcaico de enxofre , é o composto inorgânico com fórmula K 2 SO 4 , um sólido branco solúvel em água . É comumente usado em fertilizantes , fornecendo potássio e enxofre .
História
O sulfato de potássio (K 2 SO 4 ) é conhecido desde o início do século XIV. Foi estudado por Glauber , Boyle e Tachenius. No século XVII, era denominado arcanuni ou sal duplicatum , por ser uma combinação de um sal ácido com um sal alcalino . Era também conhecido como tártaro vitriólico e sal de Glaser ou sal polychrestum Glaseri em homenagem ao químico farmacêutico Christopher Glaser que o preparou e usou medicinalmente.
Conhecido como arcano duplicatum ( "segredo duplo") ou duplicata panaceia em pré-moderna medicina , foi preparado a partir do resíduo ( caput mortuum ) que sobraram da produção de água fortis (ácido nítrico, HNO 3 ) a partir de nitro (nitrato de potássio, KNO 3 ) e óleo de vitríolo (ácido sulfúrico, H 2 SO 4 ) por meio do processo de Glauber :
- 2 KNO 3 + H 2 SO 4 → 2 HNO 3 + K 2 SO 4
O resíduo foi dissolvido em água quente, filtrado e evaporado até uma cutícula. Foi então deixado para cristalizar. Foi usado como diurético e sudorífico .
De acordo com a Cyclopedia de Chambers , a receita foi comprada por quinhentos táleres por Charles Frederick, duque de Holstein-Gottorp . Schroder, o médico do duque, escreveu maravilhas sobre seus grandes usos em casos hipocondríacos , febres contínuas e intermitentes , pedra, escorbuto e muito mais.
Recursos naturais
A forma mineral do sulfato de potássio, arcanita , é relativamente rara. Os recursos naturais de sulfato de potássio são minerais abundantes no sal de Stassfurt . Estas são cocristalizações de sulfato de potássio e sulfatos de magnésio , cálcio e sódio .
Os minerais relevantes são:
- Cainita , KMg (SO 4 ) · Cl · 3H 2 O
- Schönita (agora conhecido como picromerita), K 2 SO 4 · MgSO 4 · 6H 2 O
- Leonite , K 2 SO 4 · MgSO 4 · 4H 2 O
- Langbeinita , K 2 Mg 2 (SO 4 ) 3
- Afthitalite (anteriormente conhecido como glaserite), K 3 Na (SO 4 ) 2
- Polihalita , K 2 SO 4 · MgSO 4 · 2CaSO 4 · 2H 2 O
O sulfato de potássio pode ser separado de alguns desses minerais, como a cainita, porque o sal correspondente é menos solúvel em água.
Kieserite , MgSO 4 · H 2 O, pode ser combinada com uma solução de cloreto de potássio para produzir sulfato de potássio.
Produção
Aproximadamente 1,5 milhão de toneladas foram produzidas em 1985, tipicamente pela reação de cloreto de potássio com ácido sulfúrico , análogo ao processo de Mannheim para a produção de sulfato de sódio. O processo envolve a formação intermediária de bissulfato de potássio , uma reação exotérmica que ocorre à temperatura ambiente:
- KCl + H 2 SO 4 → HCl + KHSO 4
A segunda etapa do processo é endotérmica, exigindo entrada de energia:
- KCl + KHSO 4 → HCl + K 2 SO 4
Estrutura e propriedades
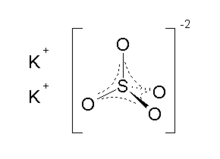
Duas formas cristalinas são conhecidas. O β-K 2 SO 4 ortorrômbico é a forma comum, mas se converte em α-K 2 SO 4 acima de 583 ° C. Essas estruturas são complexas, embora o sulfato adote a geometria tetraédrica típica.
Não forma um hidrato, ao contrário do sulfato de sódio . O sal se cristaliza como pirâmides duplas de seis lados, classificadas como rômbicas. São transparentes, muito duros e têm um sabor amargo e salgado. O sal é solúvel em água, mas insolúvel em soluções de hidróxido de potássio ( sp. Gr. 1.35) ou em etanol absoluto .
Quando o sulfato de potássio é aquecido em água e sujeito a turbilhonamento em um copo, os cristais formam uma estrutura em espiral com vários braços quando deixados em sedimentação.
Usos
O uso dominante de sulfato de potássio é como fertilizante . O K 2 SO 4 não contém cloreto, o que pode ser prejudicial para algumas culturas. O sulfato de potássio é o preferido para essas culturas, que incluem tabaco e algumas frutas e vegetais. Culturas menos sensíveis ainda podem exigir sulfato de potássio para um crescimento ideal se o solo acumular cloreto da água de irrigação.
O sal bruto também é usado ocasionalmente na fabricação de vidro. O sulfato de potássio também é usado como um redutor de flash em cargas de propelente de artilharia . Reduz o flash do focinho , flareback e a sobrepressão da explosão.
Às vezes é usado como um meio alternativo de jateamento, semelhante ao refrigerante no jateamento de refrigerante , pois é mais duro e igualmente solúvel em água.
O sulfato de potássio também pode ser usado em pirotecnia em combinação com nitrato de potássio para gerar uma chama roxa .
Reações
Acidificação
Hidrogenossulfato de potássio (também conhecido como bissulfato de potássio), KHSO 4 , é prontamente produzido pela reação de K 2 SO 4 com ácido sulfúrico . Forma pirâmides rômbicas , que fundem a 197 ° C (387 ° F). Dissolve-se em três partes de água a 0 ° C (32 ° F). A solução se comporta como se seus dois congêneres , K 2 SO 4 e H 2 SO 4 , estivessem presentes lado a lado não combinados; um excesso de etanol precipita o sulfato normal (com pouco bissulfato) com o excesso de ácido remanescente.
O comportamento do sal seco fundido é semelhante quando aquecido a várias centenas de graus; ele age sobre silicatos , titanatos , etc., da mesma forma que o ácido sulfúrico que é aquecido além de seu ponto de ebulição natural. Por isso, é freqüentemente usado em química analítica como um agente desintegrante. Para obter informações sobre outros sais que contêm sulfato, consulte sulfato .



