Superóxido de potássio - Potassium superoxide
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Dióxido de potássio
|
|
| Outros nomes
Superóxido de potássio
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.031.574 |
| Número EC | |
|
PubChem CID
|
|
| Número RTECS | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| K O 2 | |
| Massa molar | 71,096 g · mol −1 |
| Aparência | sólido amarelo |
| Densidade | 2,14 g / cm 3 , sólido |
| Ponto de fusão | 560 ° C (1.040 ° F; 833 K) (decompõe-se) |
| Hidrólise | |
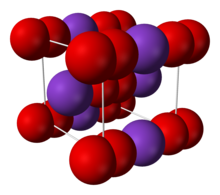
| Estrutura | |
| Cúbico centrado no corpo ( O- 2) |
|
| Termoquímica | |
|
Entropia molar padrão ( S |
117 J · mol −1 · K −1 |
| −283 kJ · mol −1 | |
| Perigos | |
| Riscos principais | corrosivo, oxidante |
| Frases R (desatualizado) | 14-8-34 |
| Frases S (desatualizado) | 17-27-36 / 37/39 |
| NFPA 704 (diamante de fogo) | |
| Compostos relacionados | |
|
Outros ânions
|
Óxido de potássio peróxido de potássio |
|
Outros cátions
|
Superóxido de lítio Superóxido de sódio Superóxido de rubídio |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O superóxido de potássio é um composto inorgânico com a fórmula KO 2 . É um sólido paramagnético amarelo que se decompõe no ar úmido. É um exemplo raro de um sal estável do ânion superóxido . O superóxido de potássio é usado como um CO
2purificador, H
2O desumidificador e O
2gerador em rebreathers , naves espaciais , submarinos e sistemas de suporte de vida de traje espacial .
Produção e reações
O superóxido de potássio é produzido pela queima de potássio fundido em uma atmosfera de oxigênio .
- K + O
2 → KO
2
O sal consiste em K+
e O-
2íons, ligados por ligação iônica. A distância O-O é 1,28 Å.
Reatividade
O superóxido de potássio é um oxidante forte , capaz de converter óxidos em peróxidos ou oxigênio molecular . A hidrólise fornece gás oxigênio, peróxido de hidrogênio e hidróxido de potássio :
- 2 KO
2 + 2 H
2O → 2 KOH + H
2O
2+ O
2
Hidróxido de potássio (KOH) absorvendo dióxido de carbono produz carbonatos:
- 2 KOH + CO
2 → K 2 CO 3 + H 2 O - KOH + CO
2 → KHCO 3
A combinação dessas duas reações produz:
- 4 KO
2 + 2 CO
2 → 2 K 2 CO 3 + 3 O
2 - 4 KO
2 + 4 CO
2 + 2 H 2 O → 4 KHCO 3 + 3 O
2
O superóxido de potássio encontra apenas usos em nicho como um reagente de laboratório. Porque reage com a água, KO
2é frequentemente estudado em solventes orgânicos. Uma vez que o sal é pouco solúvel em solventes não polares, os éteres de coroa são normalmente usados. O sal de tetraetilamônio também é conhecido. As reações representativas desses sais envolvem o uso de superóxido como nucleófilo , por exemplo, na conversão de brometos de alquila em álcoois e cloretos de acila em peróxidos de diacil .
Formulários
A Agência Espacial Russa teve sucesso usando superóxido de potássio em geradores químicos de oxigênio para seus trajes espaciais e a espaçonave Soyuz . KO
2também foi usado em botijões de rebreathers para combate a incêndio e trabalho de resgate em minas , mas tinha uso limitado em rebreathers de mergulho por causa de sua reação perigosamente explosiva com água.
KO
2reage com CO
2 na seguinte reação:
- 4 KO 2 (s) + 2 CO 2 (g) → 2K 2 CO 3 (s) + 3O 2 (g)
Teoricamente, 1 kg de KO
2absorve 0,310 kg de CO
2enquanto libera 0,338 kg de O
2. Um mole de KO
2absorve 0,5 moles de CO
2mas libera apenas 0,75 moles de moléculas de gás oxigênio ( O 2 ).
Perigos
O superóxido de potássio é um oxidante potente e pode produzir reações explosivas quando combinado com uma variedade de substâncias e compostos, incluindo água, ácidos, orgânicos ou grafite em pó. Mesmo o superóxido seco pode produzir um composto explosivo sensível ao impacto quando combinado com óleos orgânicos, como o querosene. Em 1999, no Laboratório Nacional de Oak Ridge, a limpeza de óxidos de potássio de um vazamento de metal NaK produziu uma explosão sensível ao impacto enquanto saturada com óleo mineral.
Referências
- ^ a b Zumdahl, Steven S. (2009). Princípios Químicos (6ª ed.). Houghton Mifflin. p. A22. ISBN 978-0-618-94690-7.
- ^ Hayyan M .; Hashim MA; AlNashef IM (2016). "Íon Superóxido: Geração e Implicações Químicas" . Chem. Rev . 116 (5): 3029–3085. doi : 10.1021 / acs.chemrev.5b00407 . PMID 26875845 .CS1 maint: usa o parâmetro de autores ( link )
- ^ Jakob, Harald; Leininger, Stefan; Lehmann, Thomas; Jacobi, Sylvia; Gutewort, Sven (2007). "Peroxo Compounds, Inorganic". Enciclopédia de Química Industrial de Ullmann . Wiley-VCH. doi : 10.1002 / 14356007.a19_177.pub2 . ISBN 978-3527306732.
- ^ Abrahams, SC; Kalnajs, J. (1955). "The Crystal Structure of α-Potassium Superoxide" . Acta Crystallographica . 8 (8): 503–6. doi : 10.1107 / S0365110X55001540 .
- ^ Kumar De, Anil (2007). A Text Book of Inorganic Chemistry . New Age International. p. 247. ISBN 978-8122413847.
- ^ Johnson, Roy A .; Adrio, Javier; Ribagorda, María (2001). "Superóxido de potássio". e-EROS Encyclopedia of Reagents for Organic Synthesis . Wiley. doi : 10.1002 / 047084289X.rp250.pub2 . ISBN 0471936235.
-
^ Aerojet Nuclear Company (1975). "Uma análise de riscos de explosivos da solução eutética de NaK e KO
2". Idaho National Engineering Laboratory. - ^ "Investigação de acidentes Y-12 NaK" . Departamento de Energia dos EUA. Fevereiro de 2000. Arquivado do original em 2010-05-28.

