Bateria recarregável - Rechargeable battery

Uma bateria recarregável , bateria de armazenamento ou célula secundária (ou acumulador arcaico ) é um tipo de bateria elétrica que pode ser carregada, descarregada em uma carga e recarregada muitas vezes, ao contrário de uma bateria descartável ou primária , que é fornecida totalmente carregada e descartada após o uso. É composto por uma ou mais células eletroquímicas . O termo "acumulador" é usado porque acumula e armazena energia por meio de uma reação eletroquímica reversível . As baterias recarregáveis são produzidas em muitos formatos e tamanhos diferentes, variando de células-botão a sistemas de megawatts conectados para estabilizar uma rede de distribuição elétrica . Várias combinações diferentes de materiais de eletrodo e eletrólitos são usadas, incluindo chumbo-ácido , zinco-ar , níquel-cádmio (NiCd), hidreto metálico de níquel (NiMH), íon-lítio (íon-lítio), fosfato de ferro-lítio (LiFePO4) e polímero de íon-lítio ( polímero de íon-lítio).
Baterias recarregáveis geralmente custam mais do que baterias descartáveis, mas têm um custo total de propriedade e impacto ambiental muito mais baixo , pois podem ser recarregadas de maneira econômica muitas vezes antes de precisarem ser substituídas. Alguns tipos de baterias recarregáveis estão disponíveis nos mesmos tamanhos e tensões dos tipos descartáveis e podem ser usados alternadamente com eles.
Bilhões de dólares em pesquisa estão sendo investidos em todo o mundo para melhorar as baterias e a indústria também se concentra na construção de baterias melhores.
Formulários

Os dispositivos que usam baterias recarregáveis incluem motores de partida para automóveis , dispositivos portáteis de consumo, veículos leves (como cadeiras de rodas motorizadas , carrinhos de golfe , bicicletas elétricas e empilhadeiras elétricas ), veículos rodoviários (carros, vans, caminhões, motocicletas), trens, pequenos aviões, ferramentas , fontes de alimentação ininterrupta e estações de energia de armazenamento de bateria . As aplicações emergentes em baterias híbridas de combustão interna e veículos elétricos impulsionam a tecnologia para reduzir custo, peso e tamanho, e aumentar a vida útil.
As baterias recarregáveis mais antigas se descarregam de maneira relativamente rápida e precisam ser carregadas antes do primeiro uso; algumas baterias NiMH de baixa auto-descarga mais recentes mantêm sua carga por muitos meses e são normalmente vendidas carregadas de fábrica com cerca de 70% de sua capacidade nominal.
Estações de energia de armazenamento de bateria usam baterias recarregáveis para nivelamento de carga (armazenamento de energia elétrica em momentos de baixa demanda para uso durante os períodos de pico) e para usos de energia renovável (como armazenamento de energia gerada a partir de matrizes fotovoltaicas durante o dia para ser usada à noite). O nivelamento de carga reduz a potência máxima que uma usina deve ser capaz de gerar, reduzindo o custo de capital e a necessidade de usinas de energia de pico .
De acordo com um relatório da Research and Markets, os analistas prevêem que o mercado global de baterias recarregáveis cresça a uma CAGR de 8,32% durante o período de 2018–2022.
Pequenas baterias recarregáveis podem alimentar dispositivos eletrônicos portáteis , ferramentas elétricas, eletrodomésticos e assim por diante. Baterias pesadas alimentam veículos elétricos , desde scooters a locomotivas e navios . Eles são usados na geração distribuída de eletricidade e em sistemas de energia autônomos .
Carregando e descarregando

Durante o carregamento, o material ativo positivo é oxidado , produzindo elétrons , e o material negativo é reduzido , consumindo elétrons. Esses elétrons constituem o fluxo de corrente no circuito externo . O eletrólito pode servir como um tampão simples para o fluxo interno de íons entre os eletrodos , como nas células de íon-lítio e níquel-cádmio , ou pode ser um participante ativo na reação eletroquímica , como nas células de chumbo-ácido .
A energia usada para carregar baterias recarregáveis geralmente vem de um carregador de bateria com eletricidade da rede elétrica CA , embora alguns sejam equipados para usar uma tomada de energia CC de 12 volts do veículo. A voltagem da fonte deve ser maior do que a da bateria para forçar a corrente a fluir para ela, mas não muito maior ou a bateria pode ser danificada.
Os carregadores levam de alguns minutos a várias horas para carregar a bateria. Carregadores lentos "burros", sem capacidade de detecção de tensão ou temperatura, carregam a uma taxa baixa, normalmente levando 14 horas ou mais para atingir uma carga completa. Normalmente, os carregadores rápidos podem carregar as células em duas a cinco horas, dependendo do modelo, com o mais rápido levando apenas quinze minutos. Os carregadores rápidos devem ter várias maneiras de detectar quando uma célula atinge a carga total (mudança na tensão do terminal, temperatura, etc.) para interromper o carregamento antes que ocorra sobrecarga ou superaquecimento prejudicial. Os carregadores mais rápidos geralmente incorporam ventiladores de resfriamento para evitar o superaquecimento das células. Os pacotes de bateria destinados a carregamento rápido podem incluir um sensor de temperatura que o carregador usa para proteger o pacote; o sensor terá um ou mais contatos elétricos adicionais.
Diferentes químicos de bateria requerem diferentes esquemas de carregamento. Por exemplo, alguns tipos de bateria podem ser recarregados com segurança de uma fonte de tensão constante. Outros tipos precisam ser carregados com uma fonte de corrente regulada que diminui à medida que a bateria atinge a tensão totalmente carregada. Carregar uma bateria incorretamente pode danificá-la; em casos extremos, as baterias podem superaquecer, pegar fogo ou descarregar seu conteúdo de forma explosiva.
Taxa de descarga
As taxas de carga e descarga da bateria são freqüentemente discutidas referindo-se a uma taxa de corrente "C". A taxa C é aquela que teoricamente carregaria ou descarregaria totalmente a bateria em uma hora. Por exemplo, o carregamento lento pode ser executado a C / 20 (ou uma taxa de "20 horas"), enquanto o carregamento e descarregamento típicos podem ocorrer a C / 2 (duas horas para capacidade total). A capacidade disponível das células eletroquímicas varia dependendo da taxa de descarga. Alguma energia é perdida na resistência interna dos componentes da célula (placas, eletrólitos, interconexões) e a taxa de descarga é limitada pela velocidade com que os produtos químicos na célula podem se mover. Para células de chumbo-ácido, a relação entre o tempo e a taxa de descarga é descrita pela lei de Peukert ; uma célula de chumbo-ácido que não consegue mais sustentar uma tensão terminal utilizável em uma corrente alta ainda pode ter capacidade utilizável, se descarregada a uma taxa muito menor. Folhas de dados para células recarregáveis geralmente listam a capacidade de descarga em 8 horas ou 20 horas ou outro horário estabelecido; células para sistemas de fonte de alimentação ininterrupta podem ser classificadas em 15 minutos de descarga.
A tensão terminal da bateria não é constante durante o carregamento e o descarregamento. Alguns tipos têm voltagem relativamente constante durante a descarga em grande parte de sua capacidade. As células alcalinas não recarregáveis e as células de zinco-carbono geram 1,5 V quando novas, mas essa tensão cai com o uso. A maioria das células NiMH AA e AAA são avaliadas em 1,2 V, mas têm uma curva de descarga mais plana do que as alcalinas e geralmente podem ser usadas em equipamentos projetados para usar baterias alcalinas .
As notas técnicas dos fabricantes de baterias geralmente se referem à tensão por célula (VPC) para as células individuais que compõem a bateria. Por exemplo, para carregar uma bateria de chumbo-ácido de 12 V (contendo 6 células de 2 V cada) a 2,3 VPC, é necessária uma tensão de 13,8 V nos terminais da bateria.
Danos de reversão celular
Submeter uma célula descarregada a uma corrente na direção que tende a descarregá-la ainda mais até o ponto em que os terminais positivo e negativo trocam a polaridade causa uma condição chamada reversão celular . Geralmente, empurrar a corrente através de uma célula descarregada desta forma causa a ocorrência de reações químicas indesejáveis e irreversíveis, resultando em danos permanentes à célula. A reversão celular pode ocorrer em várias circunstâncias, sendo as duas mais comuns:
- Quando uma bateria ou célula é conectada a um circuito de carregamento ao contrário.
- Quando uma bateria composta por várias células conectadas em série está profundamente descarregada.
No último caso, o problema ocorre devido às diferentes células em uma bateria terem capacidades ligeiramente diferentes. Quando uma célula atinge o nível de descarga antes das demais, as células restantes forçam a corrente através da célula descarregada.
Muitos dispositivos operados por bateria têm um corte de baixa tensão que evita a ocorrência de descargas profundas que podem causar a reversão da célula. Uma bateria inteligente possui um circuito de monitoramento de tensão embutido.
A reversão celular pode ocorrer em uma célula fracamente carregada, mesmo antes de ser totalmente descarregada. Se a corrente de drenagem da bateria for alta o suficiente, a resistência interna da célula pode criar uma queda de tensão resistiva maior do que a fem direta da célula . Isso resulta na reversão da polaridade da célula enquanto a corrente está fluindo. Quanto maior a taxa de descarga necessária de uma bateria, melhor as células devem ser combinadas, tanto no tipo de célula quanto no estado de carga, a fim de reduzir as chances de reversão das células.
Em algumas situações, como ao corrigir baterias de NiCd que foram sobrecarregadas anteriormente, pode ser desejável descarregar totalmente uma bateria. Para evitar os danos do efeito de reversão da célula, é necessário acessar cada célula separadamente: cada célula é descarregada individualmente conectando-se um clipe de carga nos terminais de cada célula, evitando assim a reversão da célula.
Danos durante o armazenamento em estado totalmente descarregado
Se uma bateria multicelular estiver totalmente descarregada, ela frequentemente será danificada devido ao efeito de reversão de célula mencionado acima. No entanto, é possível descarregar totalmente uma bateria sem causar a reversão da célula - seja descarregando cada célula separadamente ou permitindo que o vazamento interno de cada célula dissipe sua carga ao longo do tempo.
Mesmo se uma célula for levada a um estado totalmente descarregado sem reversão, no entanto, podem ocorrer danos ao longo do tempo simplesmente devido ao fato de permanecer no estado descarregado. Um exemplo disso é a sulfatação que ocorre em baterias de chumbo-ácido que ficam paradas em uma prateleira por longos períodos. Por esse motivo, geralmente é recomendável carregar uma bateria que deve permanecer armazenada e manter seu nível de carga recarregando-a periodicamente. Uma vez que também podem ocorrer danos se a bateria for sobrecarregada, o nível ideal de carga durante o armazenamento é normalmente em torno de 30% a 70%.
Profundidade de descarga
A profundidade de descarga (DOD) é normalmente indicada como uma porcentagem da capacidade nominal de ampere-hora; 0% DOD significa nenhuma descarga. Como a capacidade utilizável de um sistema de bateria depende da taxa de descarga e da voltagem permitida no final da descarga, a profundidade da descarga deve ser qualificada para mostrar a maneira como deve ser medida. Devido às variações durante a fabricação e envelhecimento, o DOD para descarga completa pode mudar com o tempo ou o número de ciclos de carga . Geralmente, um sistema de bateria recarregável tolerará mais ciclos de carga / descarga se o DOD for menor em cada ciclo. As baterias de lítio podem descarregar cerca de 80 a 90% de sua capacidade nominal. As baterias de chumbo-ácido podem descarregar cerca de 50–60%. Enquanto as baterias de fluxo podem descarregar 100%.
Vida útil e estabilidade do ciclo
Se as baterias forem usadas repetidamente, mesmo sem tratamento incorreto, elas perdem capacidade à medida que o número de ciclos de carga aumenta, até que sejam eventualmente consideradas como tendo atingido o fim de sua vida útil. Diferentes sistemas de bateria têm diferentes mecanismos de desgaste. Por exemplo, em baterias de chumbo-ácido, nem todo o material ativo é restaurado nas placas em cada ciclo de carga / descarga; eventualmente, perda de material suficiente para reduzir a capacidade da bateria. Nos tipos de íon-lítio, especialmente na descarga profunda, algum metal de lítio reativo pode ser formado no carregamento, que não está mais disponível para participar do próximo ciclo de descarga. Baterias lacradas podem perder umidade de seu eletrólito líquido, especialmente se sobrecarregadas ou operadas em alta temperatura. Isso reduz a vida útil do ciclismo.
Tempo de recarga
O tempo de recarga é um parâmetro importante para o usuário de um produto alimentado por baterias recarregáveis. Mesmo que a fonte de alimentação de carregamento forneça energia suficiente para operar o dispositivo, bem como recarregar a bateria, o dispositivo é conectado a uma fonte de alimentação externa durante o tempo de carregamento. Para veículos elétricos usados industrialmente, o carregamento fora dos turnos pode ser aceitável. Para veículos elétricos rodoviários, o carregamento rápido é necessário para carregar em um tempo razoável.
Uma bateria recarregável não pode ser recarregada a uma taxa arbitrariamente alta. A resistência interna da bateria produzirá calor e o aumento excessivo da temperatura danificará ou destruirá a bateria. Para alguns tipos, a taxa de carga máxima será limitada pela velocidade na qual o material ativo pode se difundir através de um eletrólito líquido. Altas taxas de carga podem produzir excesso de gás na bateria ou podem resultar em reações colaterais prejudiciais que reduzem permanentemente a capacidade da bateria. De maneira geral, e com muitas exceções e advertências, restaurar a capacidade total de uma bateria em uma hora ou menos é considerado um carregamento rápido. Um sistema de carregador de bateria incluirá estratégias mais complexas de circuito de controle e carregamento para carregamento rápido do que para um carregador projetado para recarga mais lenta.
Componentes ativos
Os componentes ativos em uma célula secundária são os produtos químicos que constituem os materiais ativos positivos e negativos e o eletrólito . O positivo e o negativo são compostos por materiais diferentes, sendo que o positivo apresenta potencial de redução e o negativo apresenta potencial de oxidação . A soma desses potenciais é o potencial ou voltagem padrão da célula .
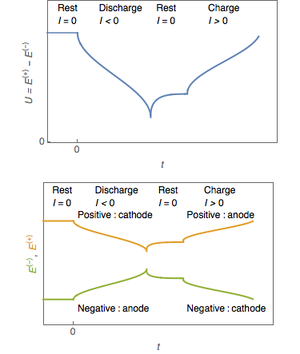
Nas células primárias, os eletrodos positivo e negativo são conhecidos como cátodo e ânodo , respectivamente. Embora essa convenção às vezes seja aplicada a sistemas recarregáveis - especialmente com células de íon-lítio , por causa de suas origens em células primárias de lítio - essa prática pode levar à confusão. Em células recarregáveis, o eletrodo positivo é o cátodo na descarga e o ânodo na carga e vice-versa para o eletrodo negativo.
Tipos

Tipos comerciais
A bateria de chumbo-ácido , inventada em 1859 pelo físico francês Gaston Planté , é o tipo mais antigo de bateria recarregável. Apesar de ter uma relação energia-peso muito baixa e uma relação energia-volume baixa, sua capacidade de fornecer altas correntes de surto significa que as células têm uma relação potência-peso relativamente grande . Esses recursos, juntamente com o baixo custo, o tornam atraente para uso em veículos motorizados para fornecer a alta corrente exigida pelos motores de arranque de automóveis .
A bateria de níquel-cádmio (NiCd) foi inventada por Waldemar Jungner da Suécia em 1899. Ela usa hidróxido de óxido de níquel e cádmio metálico como eletrodos . O cádmio é um elemento tóxico e foi banido para a maioria dos usos pela União Europeia em 2004. As baterias de níquel-cádmio foram quase completamente substituídas pelas baterias de níquel-hidreto metálico (NiMH).
A bateria de níquel-ferro (NiFe) também foi desenvolvida por Waldemar Jungner em 1899; e comercializado por Thomas Edison em 1901 nos Estados Unidos para veículos elétricos e sinalização ferroviária . É composto apenas de elementos não tóxicos, ao contrário de muitos tipos de baterias que contêm mercúrio, cádmio ou chumbo tóxico.
A bateria de níquel-hidreto metálico (NiMH) tornou-se disponível em 1989. Hoje é um consumidor comum e um tipo industrial. A bateria tem uma liga de absorção de hidrogênio para o eletrodo negativo em vez de cádmio .
A bateria de íon-lítio foi introduzida no mercado em 1991, é a escolha na maioria dos eletrônicos de consumo, tendo a melhor densidade de energia e uma perda de carga muito lenta quando não estiver em uso. Ele também tem desvantagens, especialmente o risco de ignição inesperada devido ao calor gerado pela bateria. Esses incidentes são raros e, de acordo com os especialistas, podem ser minimizados "por meio de um projeto, instalação, procedimentos e camadas de proteção adequados", de forma que o risco seja aceitável.
As baterias de polímero de íon de lítio (LiPo) são leves, oferecem densidade de energia ligeiramente maior do que as de íon de lítio a um custo um pouco mais alto e podem ser feitas em qualquer formato. Eles estão disponíveis, mas não substituíram o íon de lítio no mercado. O uso principal das baterias LiPo é para alimentar carros, barcos e aviões com controle remoto. Os pacotes LiPo estão prontamente disponíveis no mercado de consumo, em várias configurações, até 44,4 V, para alimentar certos veículos R / C e helicópteros ou drones. Alguns relatórios de teste alertam sobre o risco de incêndio quando as baterias não são usadas de acordo com as instruções. Avaliações independentes da tecnologia discutem o risco de incêndio e explosão das baterias de íon de lítio sob certas condições porque elas usam eletrólitos líquidos.
Outros tipos experimentais
| Modelo | Tensão a | Densidade de energia b | Poder c | E / $ e | Autodiscussão. f | Eficiência de carga | Ciclos g | Vida h | ||
|---|---|---|---|---|---|---|---|---|---|---|
| (V) | (MJ / kg) | (Wh / kg) | (Wh / L) | (W / kg) | (Wh / $) | (%/mês) | (%) | (#) | (anos) | |
| Lítio-enxofre | 2.0 | 0,94-1,44 | 400 | 350 | ~ 1400 | |||||
| Íon sódio | 3,6 | 30 | 3,3 | 5000+ | Testando | |||||
| Filme fino de lítio | ? | 300 | 959 | 6.000 | ? p | 40.000 | ||||
| Brometo de zinco | 1.8 | 0,27–0,31 | 75-85 | |||||||
| Zinco-cério | 2,5 | Em teste | ||||||||
| Redox de vanádio | 1,15-1,55 | 0,09–0,13 | 25-35 | 20% | 20.000 | 25 anos | ||||
| Sódio-enxofre | 0,54 | 150 | 89-92% | 2500–4500 | ||||||
| Sal derretido | 2,58 | 0,25-1,04 | 70–290 | 160 | 150–220 | 4,54 | 3000+ | <= 20 | ||
| Prata-zinco | 1,86 | 0,47 | 130 | 240 | ||||||
| Bateria quântica (semicondutor de óxido) | 1,5–3 | 500 | 8000 (W / L) | 100.000 | ||||||
‡ citações são necessárias para esses parâmetros
- Notas
- uma tensão nominal da célula em V.
- b Densidade de energia = energia / peso ou energia / tamanho, dada em três unidades diferentes
- c Potência específica = potência / peso em W / kg
- e Energia / preço ao consumidor em W · h / US $ (aproximadamente)
- f Taxa de autodescarga em% / mês
- g Ciclo de durabilidade em número de ciclos
- h Durabilidade do tempo em anos
- i VRLA ou recombinante inclui baterias de gel e tapetes de vidro absorvidos
- p produção piloto
A bateria de lítio-enxofre foi desenvolvida pela Sion Power em 1994. A empresa afirma ter densidade de energia superior a outras tecnologias de lítio.
A bateria de película fina (TFB) é um refinamento da tecnologia de íons de lítio da Excellatron. Os desenvolvedores afirmam um grande aumento nos ciclos de recarga para cerca de 40.000 e taxas de carga e descarga mais altas, pelo menos 5 C de taxa de carga. Descarga sustentada de 60 C e taxa de descarga de pico de 1000 C e um aumento significativo na energia específica e densidade de energia.
A bateria de fosfato de ferro-lítio é usada em algumas aplicações.
UltraBattery , uma bateria híbrida de chumbo-ácido e ultracapacitor inventado pela organização científica nacional da Austrália CSIRO , exibe dezenas de milhares de ciclos de carga parcial e superou as células tradicionais de chumbo-ácido, lítio e NiMH quando comparadas em testes neste modo contra perfis de poder de gerenciamento de variabilidade. A UltraBattery tem instalações em escala de kW e MW na Austrália, Japão e EUA. Ela também foi submetida a testes extensivos em veículos elétricos híbridos e demonstrou durar mais de 100.000 milhas em testes comerciais na estrada em um veículo de correio . A tecnologia tem uma vida útil de 7 a 10 vezes maior que a das baterias convencionais de chumbo-ácido em uso com alta taxa de carga parcial, com benefícios ambientais e de segurança reivindicados em relação a concorrentes como íon-lítio. Seu fabricante sugere que já existe uma taxa de reciclagem de quase 100% para o produto.
A bateria de íons de potássio oferece cerca de um milhão de ciclos, devido à extraordinária estabilidade eletroquímica dos materiais de inserção / extração de potássio, como o azul da Prússia .
A bateria de íon de sódio é destinada ao armazenamento estacionário e compete com baterias de chumbo-ácido. Tem como objetivo um baixo custo total de propriedade por kWh de armazenamento. Isso é alcançado por uma vida útil longa e estável. O número efetivo de ciclos está acima de 5000 e a bateria não é danificada por descarga profunda. A densidade de energia é bastante baixa, um pouco menor do que o ácido-chumbo.
Alternativas
Uma bateria recarregável é apenas um dos vários tipos de sistemas de armazenamento de energia recarregáveis. Existem várias alternativas para baterias recarregáveis ou estão em desenvolvimento. Para usos como rádios portáteis , as baterias recarregáveis podem ser substituídas por mecanismos de relógio que são acionados manualmente, acionando dínamos , embora este sistema possa ser usado para carregar uma bateria em vez de operar o rádio diretamente. Lanternas podem ser acionadas por um dínamo diretamente. Para transporte, sistemas de alimentação ininterrupta e laboratórios, os sistemas de armazenamento de energia do volante armazenam energia em um rotor giratório para conversão em energia elétrica quando necessário; tais sistemas podem ser usados para fornecer grandes pulsos de energia que de outra forma seriam questionáveis em uma rede elétrica comum.
Ultracapacitores - capacitores de valor extremamente alto - também são usados; uma chave de fenda elétrica que carrega em 90 segundos e aciona cerca de metade dos parafusos de um dispositivo com bateria recarregável foi lançada em 2007, e lanternas semelhantes foram produzidas. De acordo com o conceito de ultracapacitores, as baterias betavoltaicas podem ser utilizadas como um método para fornecer uma carga lenta a uma bateria secundária, estendendo consideravelmente a vida útil e a capacidade de energia do sistema de bateria sendo empregado; este tipo de arranjo é freqüentemente referido como uma "fonte de energia betavoltaica híbrida" por aqueles na indústria.
Ultracapacitores estão sendo desenvolvidos para transporte, usando um grande capacitor para armazenar energia em vez dos bancos de baterias recarregáveis usados em veículos híbridos . Uma desvantagem dos capacitores em comparação com as baterias é que a tensão do terminal cai rapidamente; um capacitor que tem 25% de sua energia inicial restante, terá metade de sua tensão inicial. Por outro lado, os sistemas de bateria tendem a ter uma tensão terminal que não diminui rapidamente até quase se esgotar. Essa queda de tensão no terminal complica o projeto da eletrônica de potência para uso com ultracapacitores. No entanto, existem benefícios potenciais na eficiência do ciclo, vida útil e peso em comparação com os sistemas recarregáveis. A China começou a usar ultracapacitores em duas rotas de ônibus comerciais em 2006; um deles é a rota 11 em Xangai .
As baterias de fluxo , usadas para aplicações especializadas, são recarregadas com a substituição do líquido eletrolítico. Uma bateria de fluxo pode ser considerada um tipo de célula de combustível recarregável .
Pesquisar
A pesquisa de baterias recarregáveis inclui o desenvolvimento de novos sistemas eletroquímicos, bem como a melhoria da vida útil e da capacidade dos tipos de corrente.
Veja também
Referências
Leitura adicional
- Belli, Brita. 'Battery University' visa treinar uma força de trabalho para armazenamento de energia de última geração , The New York Times , 8 de abril de 2013. Discute um programa de desenvolvimento profissional na San Jose State University .
- Vlasic, Bill. Empresa chinesa vence licitação para fabricante de baterias automotivas , The New York Times , publicado online em 9 de dezembro de 2012, p. B1.
- Cardwell, Diane. Bateria vista como forma de reduzir perdas de energia relacionadas ao calor , 16 de julho de 2013 online e 17 de julho de 2013 impresso em 17 de julho de 2013, na página B1 da edição de Nova York do The New York Times , p. B1. Discute as baterias de zinco-ar da Eos Energy Systems .
- Cardwell, Diane. SolarCity para usar baterias da Tesla para armazenamento de energia , 4 de dezembro de 2013 on-line, e 5 de dezembro de 2013 na edição da cidade de Nova York do The New York Times , p. B-2. Discute SolarCity , DemandLogic e Tesla Motors .
- Galbraith, Kate. Em Presidio, um aperto no Santo Graal do armazenamento de energia , The New York Times , 6 de novembro de 2010.
- Galbraith, Kate. Preenchendo as lacunas no fluxo de energia renovável , The New York Times , 22 de outubro de 2013.
- Witkin, Jim. Building Better Batteries for Electric Cars , The New York Times , 31 de março de 2011, p. F4. Publicado online em 30 de março de 2011. Discute baterias recarregáveis e a nova tecnologia de bateria de íon de lítio .
- Wald, Matthew L. Segure Esse Megawatt! , The New York Times , 7 de janeiro de 2011. Discute AES Energy Storage.
- Wald, Matthew L. Green Blog: O cheiro de cebolas é assim? Ou suco de bateria? , The New York Times , 9 de maio de 2012. Discute a tecnologia de bateria redox de vanádio .
- Wald, Matthew L. Green Blog: Cutting the Electric Bill with a Giant Battery , The New York Times , 27 de junho de 2012. Discute Saft Groupe SA
- Wald, Matthew L. Procurando iniciar um Vale do Silício para a ciência da bateria , The New York Times , 30 de novembro de 2012.
- Wald, Matthew L. De Harvard, uma bateria de armazenamento mais barata , The New York Times , 8 de janeiro de 2014. Discute a pesquisa em baterias de fluxo utilizando moléculas baseadas em carbono chamadas quinonas .
- Witkin, Jim. Building Better Batteries for Electric Cars , The New York Times , 31 de março de 2011, p. F4. Publicado online em 30 de março de 2011. Discute baterias recarregáveis e baterias de íon de lítio .
- Witkin, Jim. Blog Verde: Uma Segunda Vida para a Bateria de Carros Elétricos , The New York Times , 27 de abril de 2011. Descreve: ABB; Armazenamento de energia da comunidade para o uso de baterias de veículos elétricos para armazenamento de energia da rede.
- Woody, Todd. Blog Verde: Quando se trata de baterias de automóveis, a lei de Moore não computa , The New York Times , 6 de setembro de 2010. Discute baterias de lítio-ar .
- Jang Wook Choi. Promessa e realidade das baterias pós-íon-lítio com altas densidades de energia.