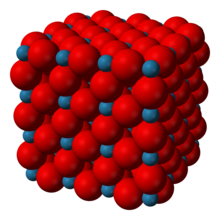
Trióxido de rênio - Rhenium trioxide
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC
Trióxido de rênio
|
|||
| Outros nomes
Rhenia
|
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| ECHA InfoCard |
100.013.845 |
||
| Número EC | |||
|
PubChem CID
|
|||
| UNII | |||
|
Painel CompTox ( EPA )
|
|||
|
|||
|
|||
| Propriedades | |||
| ReO 3 | |||
| Massa molar | 234,205 g / mol | ||
| Aparência | Cristais vermelhos profundos | ||
| Densidade | 6,92 g / cm 3 | ||
| Ponto de fusão | 400 ° C (752 ° F; 673 K) (decompõe-se) | ||
| + 16,0 · 10 −6 cm 3 / mol | |||
|
Índice de refração ( n D )
|
1,68 | ||
| Estrutura | |||
| Cúbico, cP4 | |||
| P m 3 m , No. 221 | |||
a = 374,8 pm
|
|||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
|
|
|||
| Referências da Infobox | |||
Trióxido de rênio ou óxido de rênio (VI) é um composto inorgânico com a fórmula ReO 3 . É um sólido vermelho com brilho metálico, que se assemelha ao cobre na aparência. É o único trióxido estável dos elementos do Grupo 7 ( Mn , Tc , Re ).
Preparação e estrutura
O trióxido de rênio pode ser formado reduzindo o óxido de rênio (VII) com monóxido de carbono a 200 ° C ou rênio elementar a 400 ° C.
- Re 2 O 7 + CO → 2 ReO 3 + CO 2
- 3 Re 2 O 7 + Re → 7 ReO 3
Re 2 O 7 também pode ser reduzido com dioxano .
O trióxido de rênio cristaliza com uma célula unitária cúbica primitiva , com um parâmetro de rede de 3,742 Å (374,2 pm ). A estrutura do ReO 3 é semelhante à da perovskita (ABO 3 ), sem o grande cátion A no centro da célula unitária. Cada centro de rênio é cercado por um octaedro definido por seis centros de oxigênio. Esses octaedros compartilham cantos para formar a estrutura tridimensional. O número de coordenação de O é 2, porque cada átomo de oxigênio tem 2 átomos de Re vizinhos.
Propriedades
Propriedades físicas
ReO 3 é incomum para um óxido porque exibe resistividade muito baixa . Ele se comporta como um metal , pois sua resistividade diminui à medida que sua temperatura diminui. Em 300 K , sua resistividade é 100,0 nΩ · m , enquanto que em 100 K, isso diminui para 6,0 nΩ · m, 17 vezes menos do que em 300 K.
Propriedades quimicas
O trióxido de rênio é insolúvel em água, assim como em ácidos e bases diluídos. Aquecê- lo na base resulta em desproporção para dar ReO
2 e ReO -
4 , enquanto a reação com ácido em alta temperatura fornece Re
2 O
7 . Em ácido nítrico concentrado, produz ácido perrênico . Após o aquecimento a 400 ° C sob vácuo, sofre desproporcionamento :
- 3 ReO 3 → Re 2 O 7 + ReO 2
Usos
Catalisador de hidrogenação
O trióxido de rênio encontra algum uso na síntese orgânica como um catalisador para a redução da amida .