Nitrato de rubídio - Rubidium nitrate

|
|
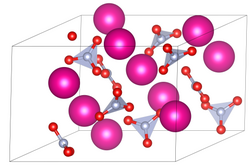 Célula unitária de nitrato de rubídio
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Nitrato de rubídio
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.032.767 |
| Número EC | |
|
PubChem CID
|
|
| Número RTECS | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| RbNO 3 | |
| Massa molar | 147,473 g / mol |
| Aparência | Sólido higroscópico branco |
| Densidade | 3,11 g / cm 3 |
| Ponto de fusão | 310 ° C (590 ° F; 583 K) se decompõe |
| Ponto de ebulição | 578 ° C (1.072 ° F; 851 K) |
| 44,28 g / 100 mL (16 ° C) 65,0 g / 100 mL (25 ° C) |
|
| −41,0 · 10 −6 cm 3 / mol | |
|
Índice de refração ( n D )
|
1.524 |
| Estrutura | |
| trigonal | |
| P3 1 | |
|
a = 10,474 Å, c = 7,443 Å
|
|
|
Volume da rede ( V )
|
707,2 Å 3 |
| Perigos | |
| Riscos principais | Oxidante |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | Não inflamável |
| Dose ou concentração letal (LD, LC): | |
|
LD 50 ( dose mediana )
|
4625 mg / kg (rato, oral) |
| Compostos relacionados | |
|
Outros ânions
|
Sulfato de rubídio Cloreto de rubídio |
|
Outros cátions
|
Nitrato de lítio Nitrato de sódio Nitrato de potássio Nitrato de césio |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O nitrato de rubídio é um composto inorgânico com a fórmula Rb NO 3 . Este nitrato de metal alcalino, sal é branca e altamente solúvel em água.
Propriedades
O nitrato de rubídio é um pó cristalino branco altamente solúvel em água e muito ligeiramente solúvel em acetona . Em um teste de chama , RbNO 3 fornece uma cor lilás / roxo claro.
Usos
Os compostos de rubídio têm muito poucas aplicações. Como o nitrato de césio , é usado em óptica de radiação infravermelha , em composições pirotécnicas como um corante pirotécnico e como um oxidante , por exemplo , em iscas e chamas de iluminação, embora seja raramente usado em fogos de artifício para produzir uma cor vermelho-violeta. É também utilizado como matéria-prima para a preparação de outros compostos de rubídio e rubídio metálico, na fabricação de catalisadores e em contadores de cintilação .
Produção
O RbNO 3 pode ser preparado dissolvendo o rubídio metálico, seu hidróxido ou carbonato em ácido nítrico.
- RbOH + HNO 3 → RbNO 3 + H 2 O
- 2 Rb + 2 HNO 3 → 2 RbNO 3 + H 2
Referências
- ^ a b W. Lenk, H. Prinz, A. Steinmetz, "Rubidium and Rubidium Compounds" em Ullmann's Encyclopedia of Industrial Chemistry, 2010 Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim. doi : 10.1002 / 14356007.a23_473.pub2
- ^ Jutta Pohl, Dieter Pohl, Gunadi Adiwidjaja (1992). "Phase Transition in Rubidium Nitrate at 346 K and Structure at 296, 372, 413 and 437 K" . Acta Crystallographica Section B . B48 : 160–166. doi : 10.1107 / S0108768191013459 .CS1 maint: vários nomes: lista de autores ( link )


