Saquinavir - Saquinavir
 | |
 | |
| Dados clínicos | |
|---|---|
| Nomes comerciais | Invirase, Fortovase |
| AHFS / Drugs.com | Monografia |
| MedlinePlus | a696001 |
| Dados de licença | |
Categoria de gravidez |
|
| Código ATC | |
| Status legal | |
| Status legal | |
| Dados farmacocinéticos | |
| Biodisponibilidade | ~ 4% (sem potenciação de ritonavir ) |
| Ligação proteica | 98% |
| Metabolismo | Fígado, principalmente por CYP3A4 |
| Meia-vida de eliminação | 9-15 horas |
| Excreção | fezes (81%) e urina (3%) |
| Identificadores | |
| |
| Número CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL | |
| NIAID ChemDB | |
| Ligante PDB | |
| Painel CompTox ( EPA ) | |
| Dados químicos e físicos | |
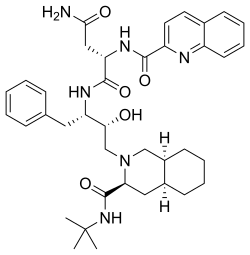
| Fórmula | C 38 H 50 N 6 O 5 |
| Massa molar | 670,855 g · mol −1 |
| Modelo 3D ( JSmol ) | |
| |
| |
| (verificar) | |
O saquinavir ( SQV ), vendido sob as marcas Invirase e Fortovase , é um medicamento antirretroviral usado junto com outros medicamentos para tratar ou prevenir o HIV / AIDS . Normalmente é usado com ritonavir ou lopinavir / ritonavir para aumentar seu efeito. É tomado por via oral.
Os efeitos colaterais comuns incluem náuseas, vômitos, diarreia e sensação de cansaço. Os efeitos colaterais mais sérios incluem problemas com o prolongamento do intervalo QT , bloqueio cardíaco , níveis elevados de lipídios no sangue e problemas no fígado. Parece ser seguro na gravidez. É da classe dos inibidores da protease e atua bloqueando a protease do HIV .
O Saquinavir foi patenteado em 1988 e vendido pela primeira vez em 1995.
Usos médicos
O saquinavir é usado junto com outros medicamentos para tratar ou prevenir o HIV / AIDS . Normalmente é usado com ritonavir ou lopinavir / ritonavir para aumentar seu efeito.
Efeitos colaterais
Os eventos adversos mais frequentes com saquinavir em qualquer formulação são sintomas gastrointestinais leves, incluindo diarreia , náuseas , fezes amolecidas e desconforto abdominal. O Invirase é mais bem tolerado do que o Fortovase.
Biodisponibilidade e interações medicamentosas
O saquinavir, na formulação Invirase, apresenta uma biodisponibilidade oral baixa e variável, quando administrado isoladamente. A formulação de Fortovase na dosagem padrão fornece aproximadamente oito vezes mais medicamento ativo do que o Invirase, também na dosagem padrão.
Na clínica, verificou-se que a biodisponibilidade oral do saquinavir em ambas as formulações aumenta significativamente quando os pacientes também recebem o IP ritonavir . Para os pacientes, isso tem o principal benefício de poderem tomar menos saquinavir, enquanto mantêm níveis suficientes de saquinavir no plasma sanguíneo para suprimir de forma eficiente a replicação do HIV.
O mecanismo por trás dessa observação bem-vinda não era conhecido diretamente, mas mais tarde foi determinado que o ritonavir inibe a isozima 3A4 do citocromo P450 . Normalmente, esta enzima metaboliza o saquinavir para uma forma inativa, mas com o ritonavir inibindo esta enzima, os níveis plasmáticos de saquinavir aumentaram consideravelmente. Além disso, o ritonavir também inibe os transportadores de múltiplas drogas, embora em grau muito menor.
Ao contrário de outros inibidores da protease, a absorção do saquinavir parece ser melhorada pelo omeprazol .
Mecanismo de ação
O saquinavir é um inibidor da protease . As proteases são enzimas que clivam as moléculas de proteínas em fragmentos menores. A protease do HIV é vital tanto para a replicação viral dentro da célula quanto para a liberação de partículas virais maduras de uma célula infectada. O saquinavir liga-se ao sítio ativo da protease viral e evita a clivagem das poliproteínas virais, evitando a maturação do vírus. O saquinavir inibe as proteases do HIV-1 e HIV-2.
História

O saquinavir foi desenvolvido pela empresa farmacêutica Roche . O saquinavir foi o sexto antirretroviral e o primeiro inibidor de protease aprovado pela Food and Drug Administration (FDA) dos Estados Unidos , levando o ritonavir e o indinavir por alguns meses. Esta nova classe de anti-retrovirais desempenhou um papel crítico no desenvolvimento da terapia anti-retroviral altamente ativa (HAART), que ajudou a reduzir significativamente o risco de morte por causas relacionadas à AIDS, como visto pela redução da taxa anual de mortalidade associada ao HIV nos Estados Unidos, de mais de 50.000 para cerca de 18.000 em um período de dois anos.
A Roche solicitou e recebeu a aprovação do Invirase por meio do programa de "Aprovação Acelerada" do FDA - um processo projetado para acelerar o lançamento de medicamentos para o tratamento de doenças graves - uma decisão que foi controversa, já que ativistas da AIDS discordavam sobre os benefícios de testes completos e acesso antecipado a novos medicamentos. Foi aprovado novamente em 7 de novembro de 1997, como Fortovase, uma cápsula de gel mole reformulada para melhorar a biodisponibilidade . A Roche anunciou em maio de 2005 que, diante da redução da demanda, o Fortovase deixaria de ser comercializado no início de 2006, em favor do Invirase potenciado com ritonavir , devido à capacidade deste último co-formulado de inibir a enzima que metaboliza os medicamentos para a AIDS .
Sociedade e cultura
Economia
A partir de 2015, não está disponível como medicamento genérico .
Formulações
Duas formulações foram comercializadas:
- uma formulação de cápsula de gel duro do mesilato , com o nome comercial Invirase, que requer combinação com ritonavir para aumentar a biodisponibilidade do saquinavir ;
- uma formulação de cápsula de gel mole de saquinavir ( microemulsão , formulação para administração oral), com o nome comercial Fortovase, que foi descontinuado em todo o mundo em 2006.
Referências
links externos
- "Saquinavir" . Portal de informações sobre medicamentos . Biblioteca Nacional de Medicina dos EUA.
