Peróxido de sódio - Sodium peroxide

|
|
|
|

|
|
| Nomes | |
|---|---|
| Outros nomes
Dióxido dissódico
Flocool Solozone peróxido dissódico |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.013.828 |
| Número EC | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| Número ONU | 1504 |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| Na 2 O 2 | |
| Massa molar | 77,98 g / mol |
| Aparência | pó amarelo a branco |
| Densidade | 2,805 g / cm 3 |
| Ponto de fusão | 460 ° C (860 ° F; 733 K) (decompõe-se) |
| Ponto de ebulição | 657 ° C (1.215 ° F; 930 K) (se decompõe) |
| reage violentamente | |
| Solubilidade | solúvel em ácido insolúvel em base reage com etanol |
| −28,10 · 10 −6 cm 3 / mol | |
| Estrutura | |
| hexagonal | |
| Termoquímica | |
|
Capacidade de calor ( C )
|
89,37 J / (mol · K) |
|
Entropia molar padrão ( S |
95 J / (mol · K) |
| −515 kJ · mol −1 | |
|
Energia livre de Gibbs (Δ f G ˚)
|
−446,9 kJ / mol |
| Perigos | |
| Ficha de dados de segurança | MSDS externo |
|
|
|
| Frases R (desatualizado) | R8 , R35 |
| Frases S (desatualizado) | (S1 / 2) , S8 , S27 , S39 , S45 |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | Não inflamável |
| Compostos relacionados | |
|
Outros cátions
|
Peróxido de lítio Peróxido de potássio Peróxido de rubídio Peróxido de césio |
|
Óxido de sódio Superóxido de sódio |
|
|
Compostos relacionados
|
Hidróxido de sódio peróxido de hidrogênio |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O peróxido de sódio é o composto inorgânico com a fórmula Na 2 O 2 . Este sólido amarelado é o produto do sódio inflamado no excesso de oxigênio. É uma base forte. Este peróxido de metal existe em vários hidratos e peroxidratos, incluindo Na 2 O 2 · 2H 2 O 2 · 4H 2 O, Na 2 O 2 · 2H 2 O, Na 2 O 2 · 2H 2 O 2 e Na 2 O 2 · 8H 2 O. O octahidratado, de simples preparo, é branco, ao contrário do anidro.
Propriedades
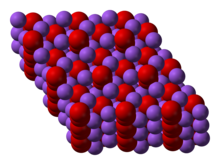
O peróxido de sódio cristaliza com simetria hexagonal. Após o aquecimento, a forma hexagonal sofre uma transição para uma fase de simetria desconhecida a 512 ° C. Com aquecimento adicional acima do ponto de ebulição de 657 ° C, o composto se decompõe em Na 2 O, liberando O 2 .
- 2 Na 2 O 2 → 2 Na 2 O + O 2
Preparação
O octahidrato é produzido pelo tratamento do hidróxido de sódio com peróxido de hidrogênio.
O peróxido de sódio pode ser preparado em grande escala pela reação do sódio metálico com o oxigênio a 130–200 ° C, um processo que gera óxido de sódio , que em uma etapa separada absorve o oxigênio:
- 4 Na + O 2 → 2 Na 2 O
- 2 Na 2 O + O 2 → 2 Na 2 O 2
Também pode ser produzido passando gás ozônio sobre iodeto de sódio sólido dentro de um tubo de platina ou paládio . O ozônio oxida o sódio para formar peróxido de sódio. O iodo pode ser sublimado por aquecimento moderado. A platina ou paládio catalisa a reação e não é atacado pelo peróxido de sódio.
Usos
O peróxido de sódio hidrolisa para dar hidróxido de sódio e peróxido de hidrogênio de acordo com a reação
- Na 2 O 2 + 2 H 2 O → 2 NaOH + H 2 O 2
O peróxido de sódio foi usado para branquear a polpa de madeira para a produção de papel e têxteis. Atualmente, é usado principalmente para operações laboratoriais especializadas, por exemplo, a extração de minerais de vários minérios. O peróxido de sódio pode ter os nomes comerciais de Solozone e Flocool . Em preparações químicas, o peróxido de sódio é usado como agente oxidante. Ele também é usado como uma fonte de oxigênio, reagindo-o com dióxido de carbono para produzir oxigênio e carbonato de sódio:
- 2 Na 2 O 2 + 2 CO 2 → 2 Na 2 CO 3 + O 2
É, portanto, particularmente útil em equipamentos de mergulho, submarinos, etc. O peróxido de lítio e o superóxido de potássio têm usos semelhantes.

