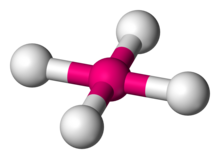
Geometria molecular quadrada plana - Square planar molecular geometry
| Geometria molecular quadrada plana | |
|---|---|
 | |
| Exemplos |
XeF 4 , PtCl 2− 4 |
| Grupo de pontos | D 4h |
| Número de coordenação | 4 |
| Ângulo (s) de ligação | 90 ° |
| μ (polaridade) | 0 |

A geometria molecular quadrada plana em química descreve a estereoquímica (arranjo espacial dos átomos) que é adotada por certos compostos químicos . Como o nome sugere, as moléculas dessa geometria têm seus átomos posicionados nos cantos.
Exemplos
Numerosos compostos adotam essa geometria, sendo os exemplos especialmente numerosos para complexos de metais de transição. O composto de gás nobre XeF 4 adota essa estrutura conforme previsto pela teoria VSEPR . A geometria é predominante para complexos de metal de transição com configuração d 8 , que inclui Rh (I), Ir (I), Pd (II), Pt (II) e Au (III). Exemplos notáveis incluem as drogas anticâncer cisplatina [PtCl 2 (NH 3 ) 2 ] e carboplatina . Muitos catalisadores homogéneos são planares quadrados no seu estado de repouso, tal como catalisador de Wilkinson e catalisador de Crabtree . Outros exemplos incluem o complexo de Vaska e o sal de Zeise . Certos ligantes (como porfirinas ) estabilizam essa geometria.
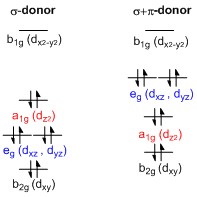
Divisão da energia dos orbitais d em complexos quadrados de metal de transição planar
Um diagrama de divisão orbital d geral para complexos de metais de transição planos quadrados (D 4h ) pode ser derivado do diagrama de divisão octaédrico (O h ) geral , no qual os orbitais d z 2 e d x 2 - y 2 são degenerados e superiores em energia do que o conjunto degenerado de orbitais d xy , d xz e d yz . Quando os dois ligantes axiais são removidos para gerar uma geometria plana quadrada, o orbital d z 2 é direcionado para uma menor energia, pois a repulsão elétron-elétron com ligantes no eixo z não está mais presente. No entanto, para ligantes puramente doadores de σ, o orbital d z 2 ainda é mais alto em energia do que os orbitais d xy , d xz e d yz por causa do lóbulo em forma de toro do orbital d z 2 . Ele carrega densidade de elétrons nos eixos xey e, portanto, interage com os orbitais do ligante preenchidos. Os orbitais d xy , d xz e d yz são geralmente apresentados como degenerados, mas eles têm que se dividir em dois níveis de energia diferentes com relação às representações irredutíveis do grupo de pontos D 4h . Sua ordem relativa depende da natureza do complexo particular. Além disso, a divisão dos orbitais d é perturbada por ligantes doadores de π em contraste com os complexos octaédricos . No caso plano quadrado, os ligantes doadores de π fortemente podem fazer com que os orbitais d xz e d yz tenham mais energia do que o orbital d z 2 , enquanto que no caso octaédrico ligantes doadores de π apenas afetam a magnitude da divisão do orbital d e a ordem relativa dos orbitais é conservada.
Veja também
Referências
links externos
- Química 3D - Química, Estruturas e Moléculas 3D
- IUMSC - Centro de Estrutura Molecular da Universidade de Indiana
- Exemplos moleculares interativos para grupos de pontos
- [1] - Números de coordenação e íons complexos