Entalpia padrão de formação - Standard enthalpy of formation
A entalpia padrão de formação ou calor padrão de formação de um composto é a mudança da entalpia durante a formação de 1 mol da substância a partir de seus elementos constituintes , com todas as substâncias em seus estados padrão . O valor de pressão padrão p ⦵ = 10 5 Pa (= 100 kPa = 1 bar ) é recomendado pela IUPAC , embora antes de 1982 o valor 1,00 atm (101,325 kPa) fosse usado. Não existe uma temperatura padrão. Seu símbolo é Δ f H ⦵ . O Plimsoll sobrescritoneste símbolo indica que o processo ocorreu sob condições padrão na temperatura especificada (geralmente 25 ° C ou 298,15 K). Os estados padrão são os seguintes:
- Para um gás: o estado hipotético que teria assumindo que obedecia à equação do gás ideal a uma pressão de 1 bar
- Para um soluto gasoso ou sólido presente em uma solução diluída ideal : o estado hipotético de concentração do soluto de exatamente um mol por litro (1 M ) a uma pressão de 1 bar extrapolado da diluição infinita
- Para uma substância pura ou um solvente em um estado condensado (um líquido ou um sólido): o estado padrão é o líquido puro ou sólido sob uma pressão de 1 bar
- Para um elemento: a forma na qual o elemento é mais estável sob 1 bar de pressão. Uma exceção é o fósforo , para o qual a forma mais estável a 1 bar é o fósforo preto , mas o fósforo branco é escolhido como o estado de referência padrão para a entalpia de formação zero.
Por exemplo, a entalpia padrão de formação de dióxido de carbono seria a entalpia da seguinte reação nas condições acima:
- C (s, grafite ) + O 2 (g) → CO 2 (g)
Todos os elementos são escritos em seus estados padrão e um mol de produto é formado. Isso é verdade para todas as entalpias de formação.
A entalpia padrão de formação é medida em unidades de energia por quantidade de substância, geralmente expressa em quilojoule por mol (kJ mol -1 ), mas também em quilocaloria por mol , joule por mol ou quilocaloria por grama (qualquer combinação dessas unidades em conformidade à energia por massa ou diretriz de quantidade).
Todos os elementos em seus estados padrão ( gás oxigênio , carbono sólido na forma de grafite , etc.) têm uma entalpia padrão de formação de zero, pois não há alteração envolvida em sua formação.
A reação de formação é um processo de pressão e temperatura constantes. Uma vez que a pressão da reação de formação padrão é fixada em 1 bar, a entalpia de formação padrão ou o calor da reação é uma função da temperatura. Para fins de tabulação, as entalpias de formação padrão são todas dadas a uma única temperatura: 298 K, representada pelo símbolo Δ f H⦵
298 K.
Lei de Hess
Para muitas substâncias, a reação de formação pode ser considerada como a soma de uma série de reações mais simples, reais ou fictícias. A entalpia de reação pode então ser analisada aplicando-se a Lei de Hess , que afirma que a soma das alterações de entalpia para uma série de etapas de reação individuais é igual à alteração de entalpia da reação geral. Isso é verdade porque a entalpia é uma função de estado , cujo valor para um processo geral depende apenas dos estados inicial e final e não de quaisquer estados intermediários. Exemplos são fornecidos nas seções a seguir.
Compostos iônicos: ciclo Born-Haber
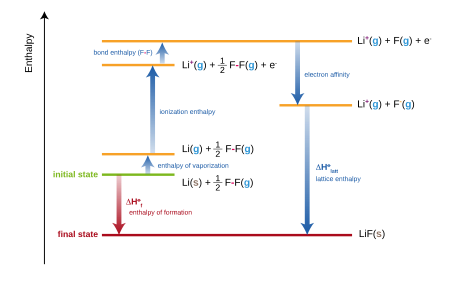
Para compostos iônicos, a entalpia padrão de formação é equivalente à soma de vários termos incluídos no ciclo de Born-Haber . Por exemplo, a formação de fluoreto de lítio ,
- Li (s) + 1 ⁄ 2 F 2 (g) → LiF (s)
pode ser considerada como a soma de várias etapas, cada uma com sua própria entalpia (ou energia, aproximadamente):
- A entalpia padrão de atomização (ou sublimação ) do lítio sólido.
- A primeira energia de ionização do lítio gasoso.
- A entalpia padrão de atomização (ou energia de ligação) do gás flúor.
- A afinidade eletrônica de um átomo de flúor.
- A energia da rede do fluoreto de lítio.
A soma de todas essas entalpias dará a entalpia padrão de formação do fluoreto de lítio.
Na prática, a entalpia de formação do fluoreto de lítio pode ser determinada experimentalmente, mas a energia da rede não pode ser medida diretamente. A equação é, portanto, reorganizada para avaliar a energia da rede.
Compostos orgânicos
As reações de formação para a maioria dos compostos orgânicos são hipotéticas. Por exemplo, o carbono e o hidrogênio não reagirão diretamente para formar o metano (CH 4 ), de modo que a entalpia padrão de formação não pode ser medida diretamente. No entanto, a entalpia padrão de combustão é facilmente mensurável usando calorimetria de bomba . A entalpia padrão de formação é então determinada usando a lei de Hess . A combustão do metano (CH 4 + 2 O 2 → CO 2 + 2 H 2 O) é equivalente à soma da decomposição hipotética em elementos seguida pela combustão dos elementos para formar dióxido de carbono e água:
- CH 4 → C + 2 H 2
- C + O 2 → CO 2
- 2 H 2 + O 2 → 2 H 2 O
Aplicando a lei de Hess,
- Δ comb H ⦵ (CH 4 ) = [Δ f H ⦵ (CO 2 ) + 2 Δ f H ⦵ (H 2 O)] - Δ f H ⦵ (CH 4 ).
Resolvendo o padrão de entalpia de formação,
- Δ f H ⦵ (CH 4 ) = [Δ f H ⦵ (CO 2 ) + 2 Δ f H ⦵ (H 2 O)] - Δ comb H ⦵ (CH 4 ).
O valor de Δ f H ⦵ (CH 4 ) é determinado como sendo −74,8 kJ / mol. O sinal negativo mostra que a reação, se ocorresse, seria exotérmica ; ou seja, o metano é entalpicamente mais estável do que o gás hidrogênio e o carbono.
É possível prever calores de formação para compostos orgânicos não tensionados com o método de aditividade do grupo de calor de formação .
Uso no cálculo de outras reações
A mudança de entalpia padrão de qualquer reação pode ser calculada a partir das entalpias padrão de formação de reagentes e produtos usando a lei de Hess. Uma dada reação é considerada a decomposição de todos os reagentes em elementos em seus estados padrão, seguida pela formação de todos os produtos. O calor de reação é, então, menos a soma das entalpias padrão de formação dos reagentes (cada uma sendo multiplicada por seu respectivo coeficiente estequiométrico, ν ) mais a soma das entalpias padrão de formação dos produtos (cada uma também multiplicada por seus respectivos estequiométricos coeficiente), conforme mostrado na equação abaixo:
- Δ r H ⦵ = Σ ν Δ f H ⦵ (produtos) - Σ ν Δ f H ⦵ (reagentes).
Se a entalpia padrão dos produtos for menor do que a entalpia padrão dos reagentes, a entalpia padrão de reação é negativa. Isso implica que a reação é exotérmica. O inverso também é verdadeiro; a entalpia de reação padrão é positiva para uma reação endotérmica. Este cálculo tem uma suposição tácita de solução ideal entre reagentes e produtos onde a entalpia de mistura é zero.
Por exemplo, para a combustão de metano, CH 4 + 2 O 2 → CO 2 + 2 H 2 O:
- Δ r H ⦵ = [Δ f H ⦵ (CO 2 ) + 2 Δ f H ⦵ (H 2 O)] - [Δ f H ⦵ (CH 4 ) + 2 Δ f H ⦵ (O 2 )].
No entanto, O 2 é um elemento em seu estado padrão, de modo que Δ f H ⦵ (O 2 ) = 0, e o calor de reação é simplificado para
- Δ r H ⦵ = [Δ f H ⦵ (CO 2 ) + 2 Δ f H ⦵ (H 2 O)] - Δ f H ⦵ (CH 4 ),
que é a equação da seção anterior para a entalpia de combustão Δ comb H ⦵ .
Conceitos-chave para fazer cálculos de entalpia
- Quando uma reação é revertida, a magnitude de Δ H permanece a mesma, mas o sinal muda.
- Quando a equação balanceada para uma reação é multiplicada por um número inteiro, o valor correspondente de Δ H também deve ser multiplicado por esse número inteiro.
- A mudança na entalpia para uma reação pode ser calculada a partir das entalpias de formação dos reagentes e dos produtos
- Os elementos em seus estados padrão não contribuem para os cálculos de entalpia da reação, uma vez que a entalpia de um elemento em seu estado padrão é zero. Os alótropos de um elemento diferente do estado padrão geralmente têm entalpias de formação padrão diferentes de zero.
Exemplos: entalpias padrão de formação a 25 ° C
Propriedades termoquímicas de substâncias selecionadas a 298,15 K e 1 atm
Substâncias inorgânicas
| Espécies | Estágio | Fórmula química | Δ f H ⦵ / (kJ / mol) |
|---|---|---|---|
| Alumínio | |||
| Alumínio | Sólido | Al | 0 |
| Cloreto de alumínio | Sólido | AlCl 3 | -705,63 |
| Óxido de alumínio | Sólido | Al 2 O 3 | -1675,5 |
| Hidróxido de alumínio | Sólido | Al (OH) 3 | -1277 |
| Sulfato de alumínio | Sólido | Al 2 (SO 4 ) 3 | -3440 |
| Bário | |||
| Cloreto de bário | Sólido | BaCl 2 | -858,6 |
| Carbonato de bário | Sólido | BaCO 3 | -1216 |
| Hidróxido de bário | Sólido | Ba (OH) 2 | -944,7 |
| Óxido de bário | Sólido | BaO | -548,1 |
| Sulfato de Bário | Sólido | BaSO 4 | -1473,2 |
| Berílio | |||
| Berílio | Sólido | Ser | 0 |
| Hidróxido de berílio | Sólido | Be (OH) 2 | -903 |
| Óxido de berílio | Sólido | BeO | -609,4 |
| Boro | |||
| Tricloreto de boro | Sólido | BCl 3 | -402,96 |
| Bromo | |||
| Bromo | Líquido | Br 2 | 0 |
| Íon brometo | Aquoso | Br - | -121 |
| Bromo | Gás | Br | 111,884 |
| Bromo | Gás | Br 2 | 30,91 |
| Trifluoreto de bromo | Gás | BrF 3 | -255,60 |
| Brometo de hidrogênio | Gás | HBr | -36,29 |
| Cádmio | |||
| Cádmio | Sólido | CD | 0 |
| Óxido de cádmio | Sólido | CdO | -258 |
| Hidróxido de cádmio | Sólido | Cd (OH) 2 | -561 |
| Sulfeto de cádmio | Sólido | CdS | -162 |
| Sulfato de cádmio | Sólido | CdSO 4 | -935 |
| Césio | |||
| Césio | Sólido | Cs | 0 |
| Césio | Gás | Cs | 76,50 |
| Césio | Líquido | Cs | 2.09 |
| Íon césio (I) | Gás | Cs + | 457.964 |
| Cloreto de césio | Sólido | CsCl | -443,04 |
| Cálcio | |||
| Cálcio | Sólido | Ca | 0 |
| Cálcio | Gás | Ca | 178,2 |
| Íon cálcio (II) | Gás | Ca 2+ | 1925,90 |
| Íon cálcio (II) | Aquoso | Ca 2+ | -542,7 |
| Carboneto de cálcio | Sólido | CaC 2 | -59,8 |
| Carbonato de cálcio ( calcita ) | Sólido | CaCO 3 | -1206,9 |
| Cloreto de cálcio | Sólido | CaCl 2 | -795,8 |
| Cloreto de cálcio | Aquoso | CaCl 2 | -877,3 |
| Fosfato de cálcio | Sólido | Ca 3 (PO 4 ) 2 | -4132 |
| Fluoreto de cálcio | Sólido | CaF 2 | -1219,6 |
| Hidreto de cálcio | Sólido | CaH 2 | -186,2 |
| Hidróxido de cálcio | Sólido | Ca (OH) 2 | -986,09 |
| Hidróxido de cálcio | Aquoso | Ca (OH) 2 | -1002,82 |
| Óxido de cálcio | Sólido | CaO | -635,09 |
| Sulfato de Calcio | Sólido | CaSO 4 | -1434,52 |
| Sulfeto de cálcio | Sólido | CaS | -482,4 |
| Wollastonite | Sólido | CaSiO 3 | -1630 |
| Carbono | |||
| Carbono ( Grafite ) | Sólido | C | 0 |
| Carbono ( Diamante ) | Sólido | C | 1,9 |
| Carbono | Gás | C | 716,67 |
| Dióxido de carbono | Gás | CO 2 | -393,509 |
| Dissulfeto de carbono | Líquido | CS 2 | 89,41 |
| Dissulfeto de carbono | Gás | CS 2 | 116,7 |
| Monóxido de carbono | Gás | CO | -110,525 |
| Cloreto de carbonila ( Fosgênio ) | Gás | COCl 2 | -218,8 |
| Dióxido de carbono (não ionizado) | Aquoso | CO 2 (aq) | -419,26 |
| Íon bicarbonato | Aquoso | HCO 3 - | -689,93 |
| Íon carbonato | Aquoso | CO 3 2– | -675,23 |
| Cloro | |||
| Cloro monoatômico | Gás | Cl | 121,7 |
| Íon cloreto | Aquoso | Cl - | -167,2 |
| Cloro | Gás | Cl 2 | 0 |
| Cromo | |||
| Cromo | Sólido | Cr | 0 |
| Cobre | |||
| Cobre | Sólido | Cu | 0 |
| Óxido de cobre (II) | Sólido | CuO | -155,2 |
| Sulfato de cobre (II) | Aquoso | CuSO 4 | -769,98 |
| Flúor | |||
| Flúor | Gás | F 2 | 0 |
| Hidrogênio | |||
| Hidrogênio monoatômico | Gás | H | 218 |
| Hidrogênio | Gás | H 2 | 0 |
| Água | Gás | H 2 O | -241.818 |
| Água | Líquido | H 2 O | -285,8 |
| Íon hidrogênio | Aquoso | H + | 0 |
| Íon hidróxido | Aquoso | OH - | -230 |
| Peróxido de hidrogênio | Líquido | H 2 O 2 | -187,8 |
| Ácido fosfórico | Líquido | H 3 PO 4 | -1288 |
| Cianeto de hidrogenio | Gás | HCN | 130,5 |
| Brometo de hidrogênio | Líquido | HBr | -36,3 |
| Cloreto de hidrogênio | Gás | HCl | -92,30 |
| Cloreto de hidrogênio | Aquoso | HCl | -167,2 |
| Fluoreto de hidrogénio | Gás | HF | -273,3 |
| Iodeto de hidrogênio | Gás | OI | 26,5 |
| Iodo | |||
| Iodo | Sólido | I 2 | 0 |
| Iodo | Gás | I 2 | 62,438 |
| Iodo | Aquoso | I 2 | 23 |
| Íon iodeto | Aquoso | Eu - | -55 |
| Ferro | |||
| Ferro | Sólido | Fe | 0 |
| Carboneto de ferro ( Cementita ) | Sólido | Fe 3 C | 5,4 |
| Carbonato de ferro (II) ( siderita ) | Sólido | FeCO 3 | -750,6 |
| Cloreto de ferro (III) | Sólido | FeCl 3 | -399,4 |
| Óxido de ferro (II) ( Wüstite ) | Sólido | FeO | -272 |
| Óxido de ferro (II, III) ( magnetita ) | Sólido | Fe 3 O 4 | -1118,4 |
| Óxido de ferro (III) ( hematita ) | Sólido | Fe 2 O 3 | -824,2 |
| Sulfato de ferro (II) | Sólido | FeSO 4 | -929 |
| Sulfato de ferro (III) | Sólido | Fe 2 (SO 4 ) 3 | -2583 |
| Sulfeto de ferro (II) | Sólido | FeS | -102 |
| Pirita | Sólido | FeS 2 | -178 |
| Liderar | |||
| Liderar | Sólido | Pb | 0 |
| Dióxido de chumbo | Sólido | PbO 2 | -277 |
| Sulfeto de chumbo | Sólido | PbS | -100 |
| Sulfato de chumbo | Sólido | PbSO 4 | -920 |
| Nitrato de chumbo (II) | Sólido | Pb (NO 3 ) 2 | -452 |
| Sulfato de chumbo (II) | Sólido | PbSO 4 | -920 |
| Lítio | |||
| Fluoreto de lítio | Sólido | LiF | -616,93 |
| Magnésio | |||
| Magnésio | Sólido | Mg | 0 |
| Íon magnésio | Aquoso | Mg 2+ | -466,85 |
| Carbonato de Magnésio | Sólido | MgCO 3 | -1095,797 |
| Cloreto de magnésio | Sólido | MgCl 2 | -641,8 |
| Hidróxido de magnésio | Sólido | Mg (OH) 2 | -924,54 |
| Hidróxido de magnésio | Aquoso | Mg (OH) 2 | -926,8 |
| Óxido de magnésio | Sólido | MgO | -601,6 |
| Sulfato de magnésio | Sólido | MgSO 4 | -1278,2 |
| Manganês | |||
| Manganês | Sólido | Mn | 0 |
| Óxido de manganês (II) | Sólido | MnO | -384,9 |
| Óxido de manganês (IV) | Sólido | MnO 2 | -519,7 |
| Óxido de manganês (III) | Sólido | Mn 2 O 3 | -971 |
| Óxido de manganês (II, III) | Sólido | Mn 3 O 4 | -1387 |
| Permanganato | Aquoso |
MnO- 4 |
-543 |
| Mercúrio | |||
| Óxido de mercúrio (II) (vermelho) | Sólido | HgO | -90,83 |
| Sulfeto de mercúrio (vermelho, cinábrio ) | Sólido | HgS | -58,2 |
| Azoto | |||
| Azoto | Gás | N 2 | 0 |
| Amônia (hidróxido de amônio) | Aquoso | NH 3 (NH 4 OH) | -80,8 |
| Amônia | Gás | NH 3 | -46,1 |
| Nitrato de amônio | Sólido | NH 4 NO 3 | -365,6 |
| Cloreto de amônio | Sólido | NH 4 Cl | -314,55 |
| Dióxido de nitrogênio | Gás | NO 2 | 33,2 |
| Hidrazina | Gás | N 2 H 4 | 95,4 |
| Hidrazina | Líquido | N 2 H 4 | 50,6 |
| Óxido nitroso | Gás | N 2 O | 82,05 |
| Óxido nítrico | Gás | NÃO | 90,29 |
| Tetróxido de dinitrogênio | Gás | N 2 O 4 | 9,16 |
| Pentóxido de dinitrogênio | Sólido | N 2 O 5 | -43,1 |
| Pentóxido de dinitrogênio | Gás | N 2 O 5 | 11,3 |
| Ácido nítrico | Aquoso | HNO 3 | -207 |
| Oxigênio | |||
| Oxigênio monoatômico | Gás | O | 249 |
| Oxigênio | Gás | O 2 | 0 |
| Ozônio | Gás | O 3 | 143 |
| Fósforo | |||
| Fósforo branco | Sólido | P 4 | 0 |
| Fósforo vermelho | Sólido | P | -17,4 |
| Fósforo preto | Sólido | P | -39,3 |
| Tricloreto de fósforo | Líquido | PCl 3 | -319,7 |
| Tricloreto de fósforo | Gás | PCl 3 | -278 |
| Pentacloreto de fósforo | Sólido | PCl 5 | -440 |
| Pentacloreto de fósforo | Gás | PCl 5 | -321 |
| Pentóxido de fósforo | Sólido | P 2 O 5 | -1505,5 |
| Potássio | |||
| Brometo de potássio | Sólido | KBr | -392,2 |
| Carbonato de potássio | Sólido | K 2 CO 3 | -1150 |
| Cloreto de potássio | Sólido | KClO 3 | -391,4 |
| Cloreto de Potássio | Sólido | KCl | −436,68 |
| Fluoreto de Potássio | Sólido | KF | -562,6 |
| Óxido de potássio | Sólido | K 2 O | -363 |
| Nitrato de potássio | Sólido | KNO 3 | -494,5 |
| Perclorato de potássio | Sólido | KClO 4 | -430,12 |
| Silício | |||
| Silício | Gás | Si | 368,2 |
| Carboneto de silício | Sólido | SiC | −74,4, −71,5 |
| Tetracloreto de silício | Líquido | SiCl 4 | -640,1 |
| Sílica ( quartzo ) | Sólido | SiO 2 | -910,86 |
| Prata | |||
| Brometo de prata | Sólido | AgBr | -99,5 |
| Cloreto de prata | Sólido | AgCl | -127,01 |
| Iodeto de prata | Sólido | AgI | -62,4 |
| Óxido de prata | Sólido | Ag 2 O | -31,1 |
| Sulfeto de prata | Sólido | Ag 2 S | -31,8 |
| Sódio | |||
| Sódio | Sólido | N / D | 0 |
| Sódio | Gás | N / D | 107,5 |
| Bicarbonato de Sódio | Sólido | NaHCO 3 | -950,8 |
| Carbonato de Sódio | Sólido | Na 2 CO 3 | -1130,77 |
| Cloreto de Sódio | Aquoso | NaCl | -407,27 |
| Cloreto de Sódio | Sólido | NaCl | -411,12 |
| Cloreto de Sódio | Líquido | NaCl | -385,92 |
| Cloreto de Sódio | Gás | NaCl | -181,42 |
| Clorato de sódio | Sólido | NaClO 3 | -365,4 |
| Fluoreto de Sódio | Sólido | NaF | -569,0 |
| Hidróxido de sódio | Aquoso | NaOH | -469,15 |
| Hidróxido de sódio | Sólido | NaOH | -425,93 |
| Hipoclorito de sódio | Sólido | NaOCl | -347,1 |
| Nitrato de sódio | Aquoso | NaNO 3 | -446,2 |
| Nitrato de sódio | Sólido | NaNO 3 | -424,8 |
| Óxido de sódio | Sólido | Na 2 O | -414,2 |
| Enxofre | |||
| Enxofre (monoclínico) | Sólido | S 8 | 0,3 |
| Enxofre (rômbico) | Sólido | S 8 | 0 |
| Sulfato de hidrogênio | Gás | H 2 S | -20,63 |
| Dióxido de enxofre | Gás | SO 2 | -296,84 |
| Trióxido de enxofre | Gás | SO 3 | -395,7 |
| Ácido sulfúrico | Líquido | H 2 SO 4 | -814 |
| Lata | |||
| Titânio | |||
| Titânio | Gás | Ti | 468 |
| Tetracloreto de titânio | Gás | TiCl 4 | -763,2 |
| Tetracloreto de titânio | Líquido | TiCl 4 | -804,2 |
| Dióxido de titânio | Sólido | TiO 2 | -944,7 |
| Zinco | |||
| Zinco | Gás | Zn | 130,7 |
| Cloreto de zinco | Sólido | ZnCl 2 | -415,1 |
| Óxido de zinco | Sólido | ZnO | -348,0 |
| Sulfato de zinco | Sólido | ZnSO 4 | -980,14 |
Hidrocarbonetos alifáticos
| Fórmula | Nome | Δ f H ⦵ / (kcal / mol) | Δ f H ⦵ / (kJ / mol) |
|---|---|---|---|
| Cadeia linear | |||
| CH 4 | Metano | -17,9 | -74,9 |
| C 2 H 6 | Etano | -20,0 | -83,7 |
| C 2 H 4 | Etileno | 12,5 | 52,5 |
| C 2 H 2 | Acetileno | 54,2 | 226,8 |
| C 3 H 8 | Propano | -25,0 | -104,6 |
| C 4 H 10 | n - butano | -30,0 | -125,5 |
| C 5 H 12 | n - pentano | -35,1 | -146,9 |
| C 6 H 14 | n - hexano | -40,0 | -167,4 |
| C 7 H 16 | n - heptano | -44,9 | -187,9 |
| C 8 H 18 | n - octanagem | -49,8 | -208,4 |
| C 9 H 20 | n - Nonane | -54,8 | -229,3 |
| C 10 H 22 | n - decano | -59,6 | -249,4 |
| Isômeros ramificados de C 4 Alcano | |||
| C 4 H 10 | Isobutano (metilpropano) | -32,1 | -134,3 |
| Isômeros ramificados de alcano C 5 | |||
| C 5 H 12 | Neopentano (dimetilpropano) | -40,1 | -167,8 |
| C 5 H 12 | Isopentano (metilbutano) | -36,9 | -154,4 |
| Isômeros ramificados C 6 Alcano | |||
| C 6 H 14 | 2,2-Dimetilbutano | -44,5 | -186,2 |
| C 6 H 14 | 2,3-Dimetilbutano | -42,5 | -177,8 |
| C 6 H 14 | 2-metilpentano (isohexano) | -41,8 | -174,9 |
| C 6 H 14 | 3-metilpentano | -41,1 | -172,0 |
| Isômeros ramificados C 7 Alcano | |||
| C 7 H 16 | 2,2-dimetilpentano | -49,2 | -205,9 |
| C 7 H 16 | 2,2,3-trimetilbutano | -49,0 | -205,0 |
| C 7 H 16 | 3,3-Dimetilpentano | -48,1 | -201,3 |
| C 7 H 16 | 2,3-Dimetilpentano | -47,3 | -197,9 |
| C 7 H 16 | 2,4-Dimetilpentano | -48,2 | -201,7 |
| C 7 H 16 | 2-metilhexano | -46,5 | -194,6 |
| C 7 H 16 | 3-metilhexano | -45,7 | -191,2 |
| C 7 H 16 | 3-etilpentano | -45,3 | -189,5 |
| Isômeros ramificados de alcano C 8 | |||
| C 8 H 18 | 2,3-Dimetilhexano | -55,1 | -230,5 |
| C 8 H 18 | 2,2,3,3-Tetrametilbutano | -53,9 | -225,5 |
| C 8 H 18 | 2,2-Dimetilhexano | -53,7 | -224,7 |
| C 8 H 18 | 2,2,4-Trimetilpentano (isooctano) | -53,5 | -223,8 |
| C 8 H 18 | 2,5-Dimetilhexano | −53,2 | -222,6 |
| C 8 H 18 | 2,2,3-Trimetilpentano | -52,6 | -220,1 |
| C 8 H 18 | 3,3-Dimetilhexano | -52,6 | -220,1 |
| C 8 H 18 | 2,4-Dimetilhexano | -52,4 | -219,2 |
| C 8 H 18 | 2,3,4-Trimetilpentano | -51,9 | -217,1 |
| C 8 H 18 | 2,3,3-Trimetilpentano | -51,7 | -216,3 |
| C 8 H 18 | 2-metilheptano | -51,5 | -215,5 |
| C 8 H 18 | 3-etil-3-metilpentano | -51,4 | -215,1 |
| C 8 H 18 | 3,4-Dimetilhexano | -50,9 | -213,0 |
| C 8 H 18 | 3-etil-2-metilpentano | -50,4 | -210,9 |
| C 8 H 18 | 3-metilheptano | -60,3 | -252,5 |
| C 8 H 18 | 4-metilheptano | ? | ? |
| C 8 H 18 | 3-etilhexano | ? | ? |
| Isômeros C 9 Alcanos ramificados (selecionados) | |||
| C 9 H 20 | 2,2,4,4-tetrametilpentano | -57,8 | -241,8 |
| C 9 H 20 | 2,2,3,3-Tetrametilpentano | -56,7 | -237,2 |
| C 9 H 20 | 2,2,3,4-Tetrametilpentano | -56,6 | -236,8 |
| C 9 H 20 | 2,3,3,4-Tetrametilpentano | -56,4 | -236,0 |
| C 9 H 20 | 3,3-dietilpentano | -55,7 | -233,0 |
Outros compostos orgânicos
| Espécies | Estágio | Fórmula química | Δ f H ⦵ / (kJ / mol) |
|---|---|---|---|
| Acetona | Líquido | C 3 H 6 O | -248,4 |
| Benzeno | Líquido | C 6 H 6 | 48,95 |
| Ácido benzóico | Sólido | C 7 H 6 O 2 | -385,2 |
| Tetracloreto de carbono | Líquido | CCl 4 | -135,4 |
| Tetracloreto de carbono | Gás | CCl 4 | -95,98 |
| Etanol | Líquido | C 2 H 5 OH | -277,0 |
| Etanol | Gás | C 2 H 5 OH | -235,3 |
| Glicose | Sólido | C 6 H 12 O 6 | -1271 |
| Isopropanol | Gás | C 3 H 7 OH | -318,1 |
| Metanol (álcool metílico) | Líquido | CH 3 OH | -238,4 |
| Metanol (álcool metílico) | Gás | CH 3 OH | -201,0 |
| Linoleato de metila ( biodiesel ) | Gás | C 19 H 34 O 2 | -356,3 |
| Sacarose | Sólido | C 12 H 22 O 11 | -2226,1 |
| Triclorometano ( clorofórmio ) | Líquido | CHCl 3 | -134,47 |
| Triclorometano ( clorofórmio ) | Gás | CHCl 3 | -103,18 |
| Cloreto de vinil | Sólido | C 2 H 3 Cl | -94,12 |
Veja também
Referências
- Zumdahl, Steven (2009). Princípios Químicos (6ª ed.). Boston. Nova York: Houghton Mifflin. pp. 384–387. ISBN 978-0-547-19626-8.


