Estereosseletividade - Stereoselectivity
Em química , estereosseletividade é a propriedade de uma reação química na qual um único reagente forma uma mistura desigual de estereoisômeros durante uma criação não estereoespecífica de um novo estereocentro ou durante uma transformação não estereoespecífica de um pré-existente. A seletividade surge de diferenças nos efeitos estéricos e eletrônicos nas vias mecanísticas que levam aos diferentes produtos. A estereosseletividade pode variar em grau, mas nunca pode ser total, pois a diferença de energia de ativação entre as duas vias é finita. Ambos os produtos são pelo menos possíveis e apenas diferem em quantidade. No entanto, em casos favoráveis, o estereoisômero menor pode não ser detectável pelos métodos analíticos usados.
Uma reação enantiosseletiva é aquela em que um enantiômero é formado em preferência ao outro, em uma reação que cria um produto opticamente ativo a partir de um material de partida aquiral, usando um catalisador quiral, uma enzima ou um reagente quiral. O grau de seletividade é medido pelo excesso enantiomérico . Uma variante importante é a resolução cinética , em que um centro quiral pré-existente sofre reação com um catalisador quiral, uma enzima ou um reagente quiral de modo que um enantiômero reage mais rápido do que o outro e deixa para trás o enantiômero menos reativo, ou no qual um pré - o centro quiral existente influencia a reatividade de um centro de reação em outra parte da mesma molécula.
Uma reação diastereosseletiva é aquela em que um diastereômero é formado em preferência a outro (ou na qual um subconjunto de todos os diastereômeros possíveis domina a mistura do produto), estabelecendo uma estereoquímica relativa preferida. Neste caso, dois ou mais centros quirais são formados ao mesmo tempo, de modo que uma estereoquímica relativa é favorecida ou um centro quiral pré-existente (que não precisa ser opticamente puro) influencia o resultado estereoquímico durante a criação de outro. O grau de seletividade relativa é medido pelo excesso diastereomérico .
A estereoconvergência pode ser considerada o oposto da estereoespecificidade, quando a reação de dois estereoisômeros diferentes produz um único estereoisômero produto.
A qualidade da estereosseletividade preocupa-se exclusivamente com os produtos e sua estereoquímica. De uma série de produtos estereoisoméricos possíveis, a reação seleciona um ou dois a serem formados.
Exemplos
Um exemplo de estereosseletividade modesta é a desidrohalogenação de 2-iodo-butano que rende 60% trans -2-buteno e 20% cis -2-buteno. Uma vez que isômeros geométricos de alceno também são classificados como diastereômeros, essa reação também seria chamada de diastereosseletiva.
A adição de ácido fórmico ao norborneno também é estereoespecífica porque o exoisômero é formado exclusivamente sem qualquer um do isômero endo:
A regra de Cram prevê o diastereômero principal resultante da adição nucleofílica diastereosseletiva a um grupo carbonila próximo a um centro quiral. O centro quiral não precisa ser opticamente puro, pois a estereoquímica relativa será a mesma para ambos os enantiômeros. No exemplo abaixo, o (S) -aldeído reage com um tiazol para formar o diastereômero (S, S), mas apenas uma pequena quantidade do diastereômero (S, R):
A epoxidação Sharpless é um exemplo de processo enantiosseletivo, no qual um substrato de álcool alílico aquiral é transformado em um epóxi-álcool opticamente ativo. No caso de álcoois alílicos quirais, resulta a resolução cinética. Outro exemplo é a diidroxilação assimétrica de Sharpless . No exemplo abaixo, o alceno aquiral produz apenas um dos 4 estereoisômeros possíveis.
Com um centro estereogênico próximo ao carbocátion, a substituição pode ser estereosseletiva em reações inter e intramoleculares. Na reação representada abaixo, o nucleófilo (furano) pode se aproximar do carbocátion formado a partir do lado menos protegido do grupo t-butil volumoso , resultando em alta diastereosseletividade facial:
Biossíntese estereosseletiva
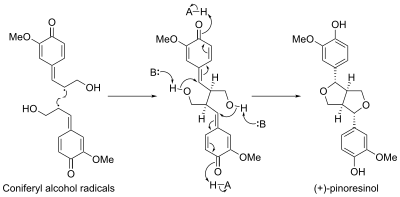
A biossíntese de pinoresinol envolveu uma proteína chamada proteína dirigente . A primeira proteína dirigente foi descoberta em Forsythia intermedia . Esta proteína foi encontrada para dirigir a biossíntese estereosseletiva de (+) - pinoresinol de monômeros de álcool coniferílico . Recentemente, uma segunda proteína dirigente enantiocomplementar foi identificada em Arabidopsis thaliana , que dirige a síntese enantiosseletiva de (-) - pinoresinol.