Tântalo - Tantalum
 | ||||||||||||||||||||||||||||||||||||||||||||||||
| Tântalo | ||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Pronúncia |
/ T Æ n t ə l əm / ( TAN -tə-ləm ) |
|||||||||||||||||||||||||||||||||||||||||||||||
| Aparência | cinza azul | |||||||||||||||||||||||||||||||||||||||||||||||
| Peso atômico padrão A r, std (Ta) | 180,947 88 (2) | |||||||||||||||||||||||||||||||||||||||||||||||
| Tântalo na tabela periódica | ||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||
| Número atômico ( Z ) | 73 | |||||||||||||||||||||||||||||||||||||||||||||||
| Grupo | grupo 5 | |||||||||||||||||||||||||||||||||||||||||||||||
| Período | período 6 | |||||||||||||||||||||||||||||||||||||||||||||||
| Bloquear | bloco d | |||||||||||||||||||||||||||||||||||||||||||||||
| Configuração de elétron | [ Xe ] 4f 14 5d 3 6s 2 | |||||||||||||||||||||||||||||||||||||||||||||||
| Elétrons por camada | 2, 8, 18, 32, 11, 2 | |||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades físicas | ||||||||||||||||||||||||||||||||||||||||||||||||
| Fase em STP | sólido | |||||||||||||||||||||||||||||||||||||||||||||||
| Ponto de fusão | 3290 K (3017 ° C, 5463 ° F) | |||||||||||||||||||||||||||||||||||||||||||||||
| Ponto de ebulição | 5731 K (5458 ° C, 9856 ° F) | |||||||||||||||||||||||||||||||||||||||||||||||
| Densidade (próximo à rt ) | 16,69 g / cm 3 | |||||||||||||||||||||||||||||||||||||||||||||||
| quando líquido (em mp ) | 15 g / cm 3 | |||||||||||||||||||||||||||||||||||||||||||||||
| Calor de fusão | 36,57 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||
| Calor da vaporização | 753 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||
| Capacidade de calor molar | 25,36 J / (mol · K) | |||||||||||||||||||||||||||||||||||||||||||||||
Pressão de vapor
| ||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades atômicas | ||||||||||||||||||||||||||||||||||||||||||||||||
| Estados de oxidação | −3, −1, 0, +1, +2, +3, +4, +5 (um óxido levemente ácido ) | |||||||||||||||||||||||||||||||||||||||||||||||
| Eletro-negatividade | Escala de Pauling: 1,5 | |||||||||||||||||||||||||||||||||||||||||||||||
| Energias de ionização | ||||||||||||||||||||||||||||||||||||||||||||||||
| Raio atômico | empírico: 146 pm | |||||||||||||||||||||||||||||||||||||||||||||||
| Raio covalente | 170 ± 20h | |||||||||||||||||||||||||||||||||||||||||||||||
| Linhas espectrais de tântalo | ||||||||||||||||||||||||||||||||||||||||||||||||
| Outras propriedades | ||||||||||||||||||||||||||||||||||||||||||||||||
| Ocorrência natural | primordial | |||||||||||||||||||||||||||||||||||||||||||||||
| Estrutura de cristal | cúbica de corpo centrado (BCC)
α-Ta |
|||||||||||||||||||||||||||||||||||||||||||||||
| Estrutura de cristal | tetragonal
β-Ta |
|||||||||||||||||||||||||||||||||||||||||||||||
| Velocidade do som haste fina | 3400 m / s (a 20 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||
| Expansão térmica | 6,3 µm / (m⋅K) (a 25 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||
| Condutividade térmica | 57,5 W / (m⋅K) | |||||||||||||||||||||||||||||||||||||||||||||||
| Resistividade elétrica | 131 nΩ⋅m (a 20 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||
| Ordenação magnética | paramagnético | |||||||||||||||||||||||||||||||||||||||||||||||
| Suscetibilidade magnética molar | +154,0 × 10 −6 cm 3 / mol (293 K) | |||||||||||||||||||||||||||||||||||||||||||||||
| Módulo de Young | 186 GPa | |||||||||||||||||||||||||||||||||||||||||||||||
| Módulo de cisalhamento | 69 GPa | |||||||||||||||||||||||||||||||||||||||||||||||
| Módulo de massa | 200 GPa | |||||||||||||||||||||||||||||||||||||||||||||||
| Coeficiente de Poisson | 0,34 | |||||||||||||||||||||||||||||||||||||||||||||||
| Dureza de Mohs | 6,5 | |||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Vickers | 870–1200 MPa | |||||||||||||||||||||||||||||||||||||||||||||||
| Dureza Brinell | 440-3430 MPa | |||||||||||||||||||||||||||||||||||||||||||||||
| Número CAS | 7440-25-7 | |||||||||||||||||||||||||||||||||||||||||||||||
| História | ||||||||||||||||||||||||||||||||||||||||||||||||
| Descoberta | Anders Gustaf Ekeberg (1802) | |||||||||||||||||||||||||||||||||||||||||||||||
| Reconhecido como um elemento distinto por | Heinrich Rose (1844) | |||||||||||||||||||||||||||||||||||||||||||||||
| Isótopos principais de tântalo | ||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||
O tântalo é um elemento químico com o símbolo Ta e o número atômico 73. Anteriormente conhecido como tântalo , recebeu o nome de Tântalo , um vilão da mitologia grega. O tântalo é um metal de transição raro, duro, cinza-azulado e brilhante , altamente resistente à corrosão. Faz parte do grupo dos metais refratários , amplamente utilizados como componentes secundários em ligas.
A inércia química do tântalo o torna uma substância valiosa para equipamentos de laboratório e como substituto da platina . Seu principal uso hoje é em capacitores de tântalo em equipamentos eletrônicos , como telefones celulares , DVD players , sistemas de videogame e computadores . O tântalo, sempre junto com o nióbio quimicamente semelhante , ocorre nos grupos minerais tantalita , columbita e coltan (o último é uma mistura de columbita e tantalita, embora não seja reconhecido como uma espécie mineral separada). O tântalo é considerado um elemento de tecnologia crítica .
História
O tântalo foi descoberto na Suécia em 1802 por Anders Ekeberg , em duas amostras de minerais - uma da Suécia e outra da Finlândia. Um ano antes, Charles Hatchett havia descoberto o columbium (agora nióbio), e em 1809 o químico inglês William Hyde Wollaston comparou seu óxido, columbita com densidade de 5,918 g / cm 3 , ao do tântalo, tantalita com densidade de 7,935 g / cm 3 . Ele concluiu que os dois óxidos, apesar de sua diferença na densidade medida, eram idênticos e mantiveram o nome de tântalo. Depois que Friedrich Wöhler confirmou esses resultados, pensou-se que o columbium e o tântalo eram o mesmo elemento. Esta conclusão foi contestada em 1846 pelo químico alemão Heinrich Rose , que argumentou que havia dois elementos adicionais na amostra de tantalita, e ele os chamou em homenagem aos filhos de Tântalo : nióbio (de Niobe , a deusa das lágrimas) e pelópio ( de Pelops ). O suposto elemento "pelópio" foi posteriormente identificado como uma mistura de tântalo e nióbio, e verificou-se que o nióbio era idêntico ao columbio já descoberto em 1801 por Hatchett.
As diferenças entre tântalo e nióbio foram demonstradas inequivocamente em 1864 por Christian Wilhelm Blomstrand e Henri Etienne Sainte-Claire Deville , bem como por Louis J. Troost , que determinou as fórmulas empíricas de alguns de seus compostos em 1865. Confirmação posterior veio de o químico suíço Jean Charles Galissard de Marignac , em 1866, que provou que existiam apenas dois elementos. Essas descobertas não impediram os cientistas de publicar artigos sobre o chamado ilmênio até 1871. De Marignac foi o primeiro a produzir a forma metálica do tântalo em 1864, quando reduziu o cloreto de tântalo aquecendo-o em uma atmosfera de hidrogênio . Os primeiros investigadores só foram capazes de produzir tântalo impuro, e o primeiro metal dúctil relativamente puro foi produzido por Werner von Bolton em Charlottenburg em 1903. Fios feitos com tântalo metálico foram usados para filamentos de lâmpadas até que o tungstênio o substituiu em uso generalizado.
O nome tântalo foi derivado do nome do mitológico Tântalo , o pai de Niobe na mitologia grega . Na história, ele foi punido após a morte ao ser condenado a ficar com água até os joelhos com frutos perfeitos crescendo acima de sua cabeça, os quais o atormentavam eternamente . (Se ele se abaixou para beber a água, ela drenou abaixo do nível que ele podia alcançar, e se ele estendeu a mão para a fruta, os galhos se moveram fora de seu alcance.) Anders Ekeberg escreveu "Este metal eu chamo de tântalo ... em parte em alusão à sua incapacidade, quando imerso em ácido, de absorvê-lo e ficar saturado. "
Durante décadas, a tecnologia comercial para separar o tântalo do nióbio envolveu a cristalização fracionada de heptafluorotantalato de potássio a partir do monohidrato de oxipentafluoroniobato de potássio, um processo que foi descoberto por Jean Charles Galissard de Marignac em 1866. Este método foi suplantado pela extração de solvente de fluoreto contendo soluções de tântalo.
Características
Propriedades físicas
O tântalo é escuro (cinza-azulado), denso, dúctil, muito duro, facilmente fabricado e altamente condutor de calor e eletricidade. O metal é conhecido por sua resistência à corrosão por ácidos ; de fato, em temperaturas abaixo de 150 ° C, o tântalo é quase completamente imune ao ataque da água régia, normalmente agressiva . Pode ser dissolvido com ácido fluorídrico ou soluções ácidas contendo o íon fluoreto e trióxido de enxofre , bem como com uma solução de hidróxido de potássio . O alto ponto de fusão do tântalo de 3017 ° C (ponto de ebulição 5458 ° C) é excedido entre os elementos apenas pelo tungstênio , rênio e ósmio para metais e carbono .
O tântalo existe em duas fases cristalinas, alfa e beta. A fase alfa é relativamente dúctil e mole; possui estrutura cúbica centrada no corpo ( grupo espacial Im3m , constante de rede a = 0,33058 nm), dureza Knoop 200–400 HN e resistividade elétrica 15–60 µΩ⋅cm. A fase beta é dura e quebradiça; sua simetria de cristal é tetragonal (grupo espacial P42 / mnm , a = 1,0194 nm, c = 0,5313 nm), a dureza Knoop é 1000–1300 HN e a resistividade elétrica é relativamente alta em 170–210 µΩ⋅cm. A fase beta é metaestável e se converte na fase alfa após o aquecimento a 750-775 ° C. O tântalo a granel é quase inteiramente a fase alfa, e a fase beta geralmente existe como filmes finos obtidos por pulverização catódica , deposição de vapor químico ou deposição eletroquímica de uma solução de sal fundido eutético .
Isótopos
O tântalo natural consiste em dois isótopos : 180m Ta (0,012%) e 181 Ta (99,988%). 181 Ta é um isótopo estável . 180m Ta ( m denota um estado metaestável) está previsto para decair de três maneiras: transição isomérica para o estado fundamental de 180 Ta, decaimento beta para 180 W ou captura de elétrons para 180 Hf . No entanto, a radioatividade desse isômero nuclear nunca foi observada, e apenas um limite inferior em sua meia-vida de 2,0 × 10 16 anos foi estabelecido. O estado fundamental de 180 Ta tem meia-vida de apenas 8 horas. 180m Ta é o único isômero nuclear de ocorrência natural (excluindo nuclídeos radiogênicos e cosmogênicos de vida curta). É também o isótopo primordial mais raro do Universo, levando em consideração a abundância elementar de tântalo e a abundância isotópica de 180m Ta na mistura natural de isótopos (e novamente excluindo os nuclídeos radiogênicos e cosmogênicos de vida curta).
O tântalo foi examinado teoricamente como um material de " salga " para armas nucleares (o cobalto é o material de salga hipotético mais conhecido). Uma cápsula externa de 181 Ta seria irradiada pelo fluxo intensivo de nêutrons de alta energia de uma hipotética arma nuclear em explosão. Isso transmutaria o tântalo no isótopo radioativo 182 Ta, que tem meia-vida de 114,4 dias e produz raios gama com aproximadamente 1,12 milhão de elétron-volts (MeV) de energia cada, o que aumentaria significativamente a radioatividade da precipitação nuclear de a explosão por vários meses. Essas armas "salgadas" nunca foram construídas ou testadas, pelo que é publicamente conhecido, e certamente nunca foram usadas como armas.
O tântalo pode ser usado como um material alvo para feixes de prótons acelerados para a produção de vários isótopos de vida curta, incluindo 8 Li, 80 Rb e 160 Yb.
Compostos químicos
O tântalo forma compostos nos estados de oxidação −III a + V. Os mais comumente encontrados são os óxidos de Ta (V), que incluem todos os minerais. As propriedades químicas de Ta e Nb são muito semelhantes. Em meio aquoso, Ta exibe apenas o estado de oxidação + V. Como o nióbio, o tântalo é pouco solúvel em soluções diluídas de ácidos clorídrico , sulfúrico , nítrico e fosfórico devido à precipitação do óxido Ta (V) hidratado. Em meios básicos, Ta pode ser solubilizado devido à formação de espécies de polioxotantalato.
Óxidos, nitretos, carbonetos, sulfetos
O pentóxido de tântalo (Ta 2 O 5 ) é o composto mais importante do ponto de vista das aplicações. Os óxidos de tântalo em estados de oxidação mais baixos são numerosos, incluindo muitas estruturas defeituosas , e são pouco estudados ou mal caracterizados.
Os tantalatos, compostos que contêm [TaO 4 ] 3− ou [TaO 3 ] - são numerosos. O tantalato de lítio (LiTaO 3 ) adota uma estrutura de perovskita. Tantalato de lantânio (LaTaO 4 ) contém TaO isolado3−
4 tetraedro.
Como no caso de outros metais refratários , os compostos de tântalo mais duros conhecidos são os nitretos e os carbonetos. O carboneto de tântalo , TaC, como o carboneto de tungstênio mais comumente usado , é uma cerâmica dura que é usada em ferramentas de corte. O nitreto de tântalo (III) é usado como isolante de película fina em alguns processos de fabricação microeletrônicos.
O calcogeneto mais bem estudado é o TaS 2 , um semicondutor em camadas , como visto para outros dichalcogenetos de metais de transição . Uma liga de tântalo-telúrio forma quasicristais .
Halides
Os halogenetos de tântalo abrangem os estados de oxidação de +5, +4 e +3. O pentafluoreto de tântalo (TaF 5 ) é um sólido branco com ponto de fusão de 97,0 ° C. O ânion [TaF 7 ] 2- é usado para sua separação do nióbio. O cloreto TaCl
5, que existe como um dímero, é o principal reagente na síntese de novos compostos Ta. Ele hidrolisa prontamente em um oxicloreto . Os haletos inferiores TaX
4e TaX
3, apresentam ligações Ta-Ta.
Compostos organotântalo
Os compostos organotântalo incluem pentametiltântalo , cloretos de alquiltântalo mistos, hidretos de alquiltântalo, complexos de alquilideno, bem como derivados de ciclopentadienil dos mesmos. Diversos sais e derivados substituídos são conhecidos para o hexacarbonil [Ta (CO) 6 ] - e isocianetos relacionados .
Ocorrência

Estima-se que o tântalo compõe cerca de 1 ppm ou 2 ppm da crosta terrestre por peso . Existem muitas espécies de minerais de tântalo, apenas algumas das quais até agora estão sendo usadas pela indústria como matéria-prima: tantalita (uma série que consiste em tantalita- (Fe), tantalita- (Mn) e tantalita- (Mg)) microlita (agora um nome de grupo), wodginita , euxenita (na verdade euxenita- (Y)) e poliarase (na verdade, poliarase- (Y)). Tantalita ( Fe , Mn ) Ta 2 O 6 é o mineral mais importante para a extração de tântalo. A tantalita tem a mesma estrutura mineral da columbita ( Fe , Mn ) (Ta, Nb ) 2 O 6 ; quando há mais tântalo do que nióbio é chamada de tantalita e quando há mais nióbio do que tântalo é chamada de columbita (ou niobita ). A alta densidade da tantalita e de outros minerais contendo tântalo torna o uso da separação gravitacional o melhor método. Outros minerais incluem samarskita e fergusonita .
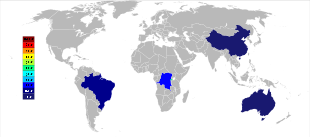
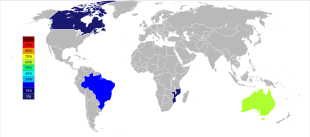
A principal mineração de tântalo está na Austrália , onde o maior produtor, Global Advanced Metals , anteriormente conhecido como Talison Minerals , opera duas minas na Austrália Ocidental, Greenbushes no sudoeste e Wodgina na região de Pilbara . A mina Wodgina foi reaberta em janeiro de 2011 depois que a mineração no local foi suspensa no final de 2008 devido à crise financeira global . Menos de um ano após sua reabertura, a Global Advanced Metals anunciou que, devido a "... amolecimento da demanda de tântalo ..." e outros fatores, as operações de mineração de tântalo deveriam cessar no final de fevereiro de 2012. Wodgina produz um tântalo primário concentrado que é posteriormente atualizado na operação Greenbushes antes de ser vendido aos clientes. Enquanto os grandes produtores de nióbio estão no Brasil e no Canadá , o minério também rende uma pequena porcentagem de tântalo. Alguns outros países, como China , Etiópia e Moçambique, extraem minérios com uma porcentagem maior de tântalo e produzem uma porcentagem significativa da produção mundial dele. O tântalo também é produzido na Tailândia e na Malásia como subproduto da mineração de estanho local. Durante a separação gravitacional dos minérios dos depósitos de placer, não apenas a cassiterita (SnO 2 ) é encontrada, mas uma pequena porcentagem de tantalita também é incluída. A escória das fundições de estanho contém então quantidades economicamente úteis de tântalo, que é lixiviado da escória.
A produção mundial de minas de tântalo passou por uma importante mudança geográfica desde o início do século 21, quando a produção era predominantemente da Austrália e do Brasil. A partir de 2007 e até 2014, as principais fontes de produção de tântalo das minas mudaram drasticamente para a RDC, Ruanda e alguns outros países africanos. Fontes futuras de suprimento de tântalo, em ordem de tamanho estimado, estão sendo exploradas na Arábia Saudita , Egito , Groenlândia , China , Moçambique , Canadá , Austrália , Estados Unidos , Finlândia e Brasil .
Estima-se que faltam menos de 50 anos de recursos de tântalo, com base na extração nas taxas atuais, demonstrando a necessidade de maior reciclagem .
Status como um recurso de conflito
O tântalo é considerado um recurso de conflito . Coltan , o nome industrial de um mineral de columbita - tantalita do qual o nióbio e o tântalo são extraídos, também pode ser encontrado na África Central , razão pela qual o tântalo está sendo relacionado à guerra na República Democrática do Congo (antigo Zaire ). De acordo com um relatório das Nações Unidas de 23 de outubro de 2003 , o contrabando e a exportação de coltan ajudaram a alimentar a guerra no Congo, uma crise que resultou em aproximadamente 5,4 milhões de mortes desde 1998 - tornando-se o conflito documentado mais mortal do mundo desde a Segunda Guerra Mundial . Questões éticas foram levantadas sobre o comportamento corporativo responsável, os direitos humanos e a ameaça à vida selvagem, devido à exploração de recursos como o coltan nas regiões de conflito armado da Bacia do Congo . O Serviço Geológico dos Estados Unidos relata em seu anuário que esta região produziu um pouco menos de 1% da produção mundial de tântalo em 2002-2006, com pico de 10% em 2000 e 2008. Os dados do USGS publicados em janeiro de 2021 indicaram que perto de 40% da produção mundial de minas de tântalo veio da República Democrática do Congo, com outros 18% provenientes dos vizinhos Ruanda e Burundi .
O objetivo declarado do Projeto Solutions for Hope Tantalum é "obter tântalo livre de conflitos da República Democrática do Congo"
Produção e fabricação
Várias etapas estão envolvidas na extração do tântalo da tantalita. Primeiro, o mineral é triturado e concentrado por separação por gravidade . Isso geralmente é realizado perto do local da mina .
Refinando
O refino do tântalo de seus minérios é um dos processos de separação mais exigentes na metalurgia industrial. O principal problema é que os minérios de tântalo contêm quantidades significativas de nióbio , que tem propriedades químicas quase idênticas às do Ta. Um grande número de procedimentos foi desenvolvido para enfrentar esse desafio.
Nos tempos modernos, a separação é realizada por hidrometalurgia . A extração começa com a lixiviação do minério com ácido fluorídrico junto com ácido sulfúrico ou ácido clorídrico . Esta etapa permite que o tântalo e o nióbio sejam separados das várias impurezas não metálicas da rocha. Embora o Ta ocorra como vários minerais, ele é convenientemente representado como pentóxido, uma vez que a maioria dos óxidos de tântalo (V) se comporta de maneira semelhante nessas condições. Uma equação simplificada para sua extração é assim:
- Ta 2 O 5 + 14 HF → 2 H 2 [TaF 7 ] + 5 H 2 O
Reações completamente análogas ocorrem para o componente de nióbio, mas o hexafluoreto é tipicamente predominante nas condições de extração.
- Nb 2 O 5 + 12 HF → 2 H [NbF 6 ] + 5 H 2 O
Essas equações são simplificadas: suspeita-se que bissulfato (HSO 4 - ) e cloreto competem como ligantes para os íons Nb (V) e Ta (V), quando são utilizados os ácidos sulfúrico e clorídrico, respectivamente. Os complexos de tântalo e fluoreto de nióbio são então removidos da solução aquosa por extração líquido-líquido em solventes orgânicos , tais como ciclohexanona , octanol e metil isobutil cetona . Este procedimento simples permite a remoção da maioria das impurezas contendo metais (por exemplo, ferro, manganês, titânio, zircônio), que permanecem na fase aquosa na forma de seus fluoretos e outros complexos.
A separação do tântalo do nióbio é então alcançada diminuindo a força iônica da mistura ácida, o que faz com que o nióbio se dissolva na fase aquosa. É proposto que o oxifluoreto H 2 [NbOF 5 ] seja formado nessas condições. Após a remoção do nióbio, a solução de H 2 purificado [TaF 7 ] é neutralizada com amônia aquosa para precipitar o óxido de tântalo hidratado como um sólido, que pode ser calcinado a pentóxido de tântalo (Ta 2 O 5 ).
Em vez de hidrólise, o H 2 [TaF 7 ] pode ser tratado com fluoreto de potássio para produzir heptafluorotantalato de potássio :
- H 2 [TaF 7 ] + 2 KF → K 2 [TaF 7 ] + 2 HF
Ao contrário do H 2 [TaF 7 ], o sal de potássio é prontamente cristalizado e tratado como um sólido.
K 2 [TaF 7 ] pode ser convertido em tântalo metálico por redução com sódio , a aproximadamente 800 ° C em sal fundido .
- K 2 [TaF 7 ] + 5 Na → Ta + 5 NaF + 2 KF
Em um método mais antigo, chamado de processo de Marignac , a mistura de H 2 [TaF 7 ] e H 2 [NbOF 5 ] foi convertida em uma mistura de K 2 [TaF 7 ] e K 2 [NbOF 5 ], que era então separados por cristalização fracionada , explorando suas diferentes solubilidades em água.
Eletrólise
O tântalo também pode ser refinado por eletrólise, usando uma versão modificada do processo Hall-Héroult . Em vez de exigir que o óxido de entrada e o metal de saída estejam na forma líquida, a eletrólise de tântalo opera em óxidos em pó não líquidos. A descoberta inicial veio em 1997, quando pesquisadores da Universidade de Cambridge imergiram pequenas amostras de certos óxidos em banhos de sal fundido e reduziram o óxido com corrente elétrica. O cátodo usa óxido de metal em pó. O ânodo é feito de carbono. O sal fundido a 1.000 ° C (1.830 ° F) é o eletrólito. A primeira refinaria tem capacidade suficiente para atender de 3 a 4% da demanda global anual.
Fabricação e trabalho em metal
Toda soldagem de tântalo deve ser feita em atmosfera inerte de argônio ou hélio para protegê-lo da contaminação com gases atmosféricos. O tântalo não é soldável . Moer o tântalo é difícil, especialmente para o tântalo recozido . Na condição recozida, o tântalo é extremamente dúctil e pode ser facilmente formado como folhas de metal.
Formulários
Eletrônicos
O principal uso do tântalo, como o pó metálico, é na produção de componentes eletrônicos, principalmente capacitores e alguns resistores de alta potência . Capacitores eletrolíticos de tântalo exploram a tendência do tântalo de formar uma camada superficial de óxido protetora , usando pó de tântalo, prensado em forma de pelota, como uma "placa" do capacitor, o óxido como o dielétrico e uma solução eletrolítica ou sólido condutor como o outro "prato". Como a camada dielétrica pode ser muito fina (mais fina do que a camada semelhante em, por exemplo, um capacitor eletrolítico de alumínio), uma alta capacitância pode ser alcançada em um pequeno volume. Devido às vantagens de tamanho e peso, os capacitores de tântalo são atraentes para telefones portáteis , computadores pessoais , eletrônicos automotivos e câmeras .
Ligas
O tântalo também é usado para produzir uma variedade de ligas com altos pontos de fusão, resistência e ductilidade. Ligado a outros metais, também é usado na fabricação de ferramentas de metal duro para equipamentos de usinagem e na produção de superligas para componentes de motores a jato, equipamentos de processos químicos, reatores nucleares , peças de mísseis, trocadores de calor, tanques e vasos. Devido à sua ductilidade, o tântalo pode ser transformado em fios ou filamentos finos, que são usados para a evaporação de metais como o alumínio . Uma vez que resiste ao ataque de fluidos corporais e não é irritante, o tântalo é amplamente utilizado na fabricação de instrumentos cirúrgicos e implantes. Por exemplo, revestimentos de tântalo poroso são usados na construção de implantes ortopédicos devido à capacidade do tântalo de formar uma ligação direta ao tecido duro.
O tântalo é inerte contra a maioria dos ácidos, exceto o ácido fluorídrico e o ácido sulfúrico quente , e as soluções alcalinas quentes também causam a corrosão do tântalo. Esta propriedade o torna um metal útil para vasos de reação química e tubos para líquidos corrosivos. As serpentinas de troca de calor para o aquecimento a vapor de ácido clorídrico são feitas de tântalo. O tântalo foi amplamente utilizado na produção de tubos de elétrons de ultra-alta frequência para transmissores de rádio. O tântalo é capaz de capturar oxigênio e nitrogênio pela formação de nitretos e óxidos e, portanto, ajudou a sustentar o alto vácuo necessário para os tubos quando usados para peças internas, como grades e placas.
Outros usos

O tântalo foi usado pela NASA para proteger os componentes da espaçonave, como a Voyager 1 e 2, da radiação. O alto ponto de fusão e resistência à oxidação levam ao uso do metal na produção de peças de fornos a vácuo . O tântalo é extremamente inerte e, portanto, é formado em uma variedade de peças resistentes à corrosão, como poços termométricos , corpos de válvula e fixadores de tântalo. Devido à sua alta densidade, os revestimentos de penetração formados de forma explosiva e de carga foram construídos em tântalo. O tântalo aumenta muito as capacidades de penetração da armadura de uma carga modelada devido à sua alta densidade e alto ponto de fusão. Também é ocasionalmente usado em relógios preciosos, por exemplo, da Audemars Piguet , FP Journe , Hublot , Montblanc , Omega e Panerai . O tântalo também é altamente bioinerte e é usado como material de implante ortopédico. A alta rigidez do tântalo torna necessário seu uso como espuma altamente porosa ou andaime com menor rigidez para implantes de prótese de quadril para evitar a proteção contra tensões . Como o tântalo é um metal não ferroso e não magnético, esses implantes são considerados aceitáveis para pacientes submetidos a procedimentos de ressonância magnética. O óxido é usado para fazer vidro especial de alto índice de refração para lentes de câmeras .
Problemas ambientais
O tântalo recebe muito menos atenção no campo ambiental do que em outras geociências. A concentração da crosta superior (UCC) e a razão Nb / Ta na crosta superior e nos minerais estão disponíveis porque essas medições são úteis como uma ferramenta geoquímica. O último valor para a concentração da crosta superior é de 0,92 ppm, e a razão Nb / Ta (w / w) é de 12,7.
Poucos dados estão disponíveis sobre as concentrações de tântalo nos diferentes compartimentos ambientais, especialmente em águas naturais, onde estimativas confiáveis das concentrações de tântalo 'dissolvido' na água do mar e em águas doces nem mesmo foram produzidas. Alguns valores sobre as concentrações dissolvidas nos oceanos foram publicados, mas são contraditórios. Os valores em águas doces se saem um pouco melhor, mas, em todos os casos, provavelmente estão abaixo de 1 ng L -1 , uma vez que as concentrações 'dissolvidas' em águas naturais estão bem abaixo da maioria das capacidades analíticas atuais. A análise requer procedimentos de pré-concentração que, no momento, não fornecem resultados consistentes. E, em qualquer caso, o tântalo parece estar presente em águas naturais principalmente como partículas em vez de dissolvido.
Valores para concentrações em solos, sedimentos de leito e aerossóis atmosféricos são mais fáceis de encontrar. Os valores nos solos são próximos a 1 ppm e, portanto, aos valores UCC. Isso indica origem detrital. Para aerossóis atmosféricos, os valores disponíveis são dispersos e limitados. Quando o enriquecimento de tântalo é observado, é provavelmente devido à perda de mais elementos solúveis em água em aerossóis nas nuvens.
Poluição ligada ao uso humano do elemento não foi detectada. O tântalo parece ser um elemento muito conservador em termos biogeoquímicos, mas seu ciclo e reatividade ainda não são totalmente compreendidos.
Precauções
Compostos contendo tântalo raramente são encontrados no laboratório. O metal é altamente biocompatível e é usado para implantes e revestimentos corporais , portanto, a atenção pode estar voltada para outros elementos ou a natureza física do composto químico .
As pessoas podem ser expostas ao tântalo no local de trabalho ao respirá-lo, ao contato com a pele ou com os olhos. A Administração de Segurança e Saúde Ocupacional (OSHA) definiu o limite legal (limite de exposição permitido ) para a exposição ao tântalo no local de trabalho como 5 mg / m 3 em um dia de trabalho de 8 horas. O Instituto Nacional de Segurança e Saúde Ocupacional (NIOSH) definiu um limite de exposição recomendado (REL) de 5 mg / m 3 ao longo de um dia de trabalho de 8 horas e um limite de curto prazo de 10 mg / m 3 . Em níveis de 2500 mg / m 3 , o tântalo é imediatamente perigoso para a vida e a saúde .
Referências
links externos
- Centro de estudos internacional de tântalo-nióbio
- CDC - Guia de bolso do NIOSH para perigos químicos