Reagente de Tebbe - Tebbe's reagent
|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
μ-Cloro [di (ciclopenta-2,4-dien-1-il)] dimetil (μ-metileno) titaniumalumínio
|
|
| Outros nomes
Reagente de Tebbe
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.157.162 |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 13 H 18 AlClTi | |
| Massa molar | 284,60 g / mol |
| Solubilidade em outros solventes | tolueno, benzeno, diclorometano, THF (somente baixas temperaturas) |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
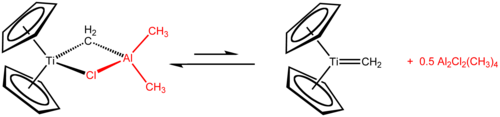
O reagente de Tebbe é o composto organometálico com a fórmula (C 5 H 5 ) 2 TiCH 2 ClAl (CH 3 ) 2 . É usado no metilenação de carbonilo compostos, que é ele converte compostos orgânicos contendo R 2 C = O grupo no relacionada R 2 C = CH 2 derivado. É um sólido vermelho que é pirofórico no ar e, portanto, é normalmente manuseado com técnicas sem ar . Foi originalmente sintetizado por Fred Tebbe na DuPont Central Research .
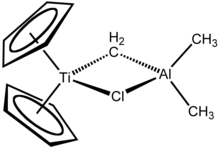
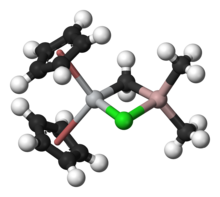
O reagente de Tebbe contém dois centros de metal tetraédricos ligados por um par de ligantes em ponte . O titânio tem dois ciclopentadienil ( [C
5 H
5 ] -
ou Cp) anéis e alumínio tem dois grupos metil. Os átomos de titânio e alumínio estão ligados entre si por uma ponte de metileno (-CH 2 -) e um átomo de cloreto em uma geometria quase quadrada-plana (Ti – CH 2 –Al – Cl). O reagente de Tebbe foi o primeiro composto relatado onde uma ponte de metileno conecta um metal de transição (Ti) e um metal do grupo principal (Al).
Preparação
O reagente de Tebbe é sintetizado a partir de dicloreto de titanoceno e trimetilalumínio em solução de tolueno .
- Cp 2 TiCl 2 + 2 Al (CH 3 ) 3 → CH 4 + Cp 2 TiCH 2 AlCl (CH 3 ) 2 + Al (CH 3 ) 2 Cl
Após cerca de 3 dias, o produto é obtido após recristalização para remover Al (CH 3 ) 2 Cl. Embora as sínteses usando o reagente de Tebbe isolado forneçam um produto mais limpo, procedimentos bem-sucedidos usando o reagente "in situ" foram relatados. Em vez de isolar o reagente de Tebbe, a solução é simplesmente resfriada em um banho de gelo ou banho de gelo seco antes de adicionar o material de partida.
Uma síntese alternativa, mas menos conveniente, envolve o uso de dimetiltitanoceno (reagente Petasis):
- Cp 2 Ti (CH 3 ) 2 + Al (CH 3 ) 2 Cl → Cp 2 TiCH 2 AlCl (CH 3 ) 2 + CH 4
Uma desvantagem deste método, além de requerer Cp 2 Ti (CH 3 ) 2 , é a dificuldade de separar o produto do reagente de partida que não reagiu.
Mecanismo de reação
O reagente de Tebbe em si não reage com compostos carbonílicos, mas deve primeiro ser tratado com uma base de Lewis suave , como a piridina , que gera o carbeno de Schrock ativo .
Também análogo ao reagente de Wittig, a reatividade parece ser impulsionada pela alta oxofilicidade do Ti (IV). O carbeno de Schrock ( 1 ) reage com compostos de carbonila ( 2 ) para dar um intermediário oxatitanaciclobutano postulado ( 3 ). Este intermediário cíclico nunca foi isolado diretamente, presumivelmente porque se decompõe imediatamente para produzir o alceno desejado ( 5 ).
Alcance
O reagente de Tebbe é usado em síntese orgânica para metilenação de carbonil. Esta conversão também pode ser efetuada usando a reação de Wittig , embora o reagente de Tebbe seja mais eficiente, especialmente para carbonilas com carga estérica. Além disso, o reagente de Tebbe é menos básico do que o reagente de Wittig e não fornece os produtos de eliminação β.
As reações de metilenação também ocorrem para aldeídos , bem como ésteres , lactonas e amidas . O reagente de Tebbe converte ésteres e lactonas em éteres enólicos e amidas em enaminas. Em compostos contendo grupos cetona e éster, a cetona reage seletivamente na presença de um equivalente do reagente de Tebbe.
O reagente de Tebbe metilenata carbonilas sem racemizar um carbono α quiral . Por esta razão, o reagente de Tebbe encontrou aplicações em reações de açúcares onde a manutenção da estereoquímica pode ser crítica.
O reagente de Tebbe reage com cloretos de ácido para formar enolatos de titânio, substituindo Cl - .
Modificações
É possível modificar o reagente de Tebbe através do uso de diferentes ligantes. Isso pode alterar a reatividade do complexo, permitindo uma gama mais ampla de reações. Por exemplo, a ciclopropanação pode ser alcançada usando um análogo clorado.
Veja também
Reagentes e reações de organotitânio relacionados
- Reação de Kulinkovich
- Reagente Petasis
- Reagente Lombardo
- Reação de McMurry