Tecnécio - Technetium
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Tecnécio | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Pronúncia |
/ T ɛ k n i ʃ i ə m / ( tek- NEE -shee-əm ) |
||||||||||||||||||||||||||||||||||||||||||||||||||
| Aparência | metal cinza brilhante | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Número de massa | [97] | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Tecnécio na tabela periódica | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Número atômico ( Z ) | 43 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo | grupo 7 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Período | período 5 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Bloquear | bloco d | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuração de elétron | [ Kr ] 4d 5 5s 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Elétrons por camada | 2, 8, 18, 13, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades físicas | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase em STP | sólido | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto de fusão | 2430 K (2157 ° C, 3915 ° F) | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto de ebulição | 4538 K (4265 ° C, 7709 ° F) | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidade (próximo à rt ) | 11 g / cm 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor de fusão | 33,29 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor da vaporização | 585,2 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacidade de calor molar | 24,27 J / (mol · K) | ||||||||||||||||||||||||||||||||||||||||||||||||||
Pressão de vapor (extrapolado)
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades atômicas | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Estados de oxidação | −3, −1, 0, +1, +2, +3, +4 , +5, +6, +7 (um óxido fortemente ácido ) | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Eletro-negatividade | Escala de Pauling: 1,9 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Energias de ionização | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Raio atômico | empírico: 136 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Raio covalente | 147 ± 19h | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Linhas espectrais de tecnécio | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Outras propriedades | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Ocorrência natural | da decadência | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Estrutura de cristal | hexagonal compacta-fim (HCP) | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidade do som haste fina | 16.200 m / s (a 20 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Expansão térmica | 7,1 µm / (m⋅K) (à temperatura ambiente ) | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Condutividade térmica | 50,6 W / (m⋅K) | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Resistividade elétrica | 200 nΩ⋅m (a 20 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordenação magnética | Paramagnético | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Suscetibilidade magnética molar | +270,0 × 10 −6 cm 3 / mol (298 K) | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Número CAS | 7440-26-8 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| História | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Predição | Dmitri Mendeleev (1871) | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Descoberta e primeiro isolamento | Emilio Segrè e Carlo Perrier (1937) | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Principais isótopos de tecnécio | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Tecnécio é um elemento químico com o símbolo Tc e número atômico 43. É o elemento mais leve cujos isótopos são todos radioativos , nenhum dos quais é estável, exceto o estado totalmente ionizado de 97 Tc. Quase todo o tecnécio disponível é produzido como um elemento sintético . O tecnécio de ocorrência natural é um produto da fissão espontânea no minério de urânio e minério de tório , a fonte mais comum, ou o produto da captura de nêutrons nos minérios de molibdênio . O metal de transição cristalino cinza prateado fica entre o manganês e o rênio no grupo 7 da tabela periódica , e suas propriedades químicas são intermediárias entre as de ambos os elementos adjacentes. O isótopo de ocorrência natural mais comum é o 99 Tc, apenas em traços.
Muitas das propriedades do tecnécio foram previstas por Dmitri Mendeleev antes de ser descoberto. Mendeleev observou uma lacuna em sua tabela periódica e deu ao elemento não descoberto o nome provisório de ekamanganese ( Em ). Em 1937, o tecnécio (especificamente o isótopo tecnécio-97 ) tornou-se o primeiro elemento predominantemente artificial a ser produzido, daí o seu nome (do grego τεχνητός , que significa "Ofício, Arte ou Artificial", + -ium ).
Um isômero nuclear emissor de raios gama de curta duração , o tecnécio-99m , é usado na medicina nuclear para uma ampla variedade de testes, como diagnósticos de câncer ósseo. O estado fundamental do nuclídeo tecnécio-99 é usado como uma fonte de partículas beta sem raios gama . Isótopos de tecnécio de longa vida produzidos comercialmente são subprodutos da fissão do urânio-235 em reatores nucleares e são extraídos de barras de combustível nuclear . Como mesmo o isótopo de tecnécio de vida mais longa tem meia-vida relativamente curta (4,21 milhões de anos), a detecção de tecnécio em gigantes vermelhas em 1952 ajudou a provar que as estrelas podem produzir elementos mais pesados .
História
Pesquisar elemento 43
De 1860 a 1871, as primeiras formas da tabela periódica propostas por Dmitri Mendeleev continham uma lacuna entre o molibdênio (elemento 42) e o rutênio (elemento 44). Em 1871, Mendeleev previu que esse elemento ausente ocuparia o lugar vazio abaixo do manganês e teria propriedades químicas semelhantes. Mendeleev deu-lhe o nome provisório de ekamanganês (de eka -, a palavra sânscrita para um ) porque o elemento previsto estava um lugar abaixo do conhecido elemento manganês.
Erros de identificação precoce
Muitos dos primeiros pesquisadores, antes e depois da publicação da tabela periódica, estavam ansiosos para ser os primeiros a descobrir e nomear o elemento que faltava. Sua localização na tabela sugeria que deveria ser mais fácil de encontrar do que outros elementos não descobertos.
| Ano | Requerente | Nome sugerido | Material real |
|---|---|---|---|
| 1828 | Gottfried Osann | Polinium | Iridium |
| 1846 | R. Hermann | Ilmenium | Nióbio - liga de tântalo |
| 1847 | Heinrich Rose | Pelopium | Liga de Nióbio-Tântalo |
| 1877 | Serge Kern | Davyum | Irídio - ródio - liga de ferro |
| 1896 | Prosper Barrière | Lucium | Ítrio |
| 1908 | Masataka Ogawa | Nipônio | Rênio , que era o dvi -manganês desconhecido |
Resultados irreproduzíveis

Os químicos alemães Walter Noddack , Otto Berg e Ida Tacke relataram a descoberta do elemento 75 e do elemento 43 em 1925, e chamaram o elemento 43 de masurium ( em homenagem à Masúria na Prússia oriental , agora na Polônia , a região onde a família de Walter Noddack se originou). O grupo bombardeou a columbita com um feixe de elétrons e o elemento 43 deduzido estava presente examinando espectrogramas de emissão de raios-X . O comprimento de onda dos raios-X produzidos está relacionado ao número atômico por uma fórmula derivada por Henry Moseley em 1913. A equipe afirmou ter detectado um sinal fraco de raios-X em um comprimento de onda produzido pelo elemento 43. Experimentadores posteriores não puderam replicar a descoberta , e foi descartado como um erro por muitos anos. Ainda assim, em 1933, uma série de artigos sobre a descoberta de elementos citou o nome masurium para o elemento 43. Se a equipe de 1925 realmente descobriu o elemento 43 ainda é debatido.
Descoberta oficial e história posterior
A descoberta do elemento 43 foi finalmente confirmada em um experimento de 1937 na Universidade de Palermo, na Sicília, por Carlo Perrier e Emilio Segrè . Em meados de 1936, Segrè visitou os Estados Unidos, primeiro a Columbia University em Nova York e depois o Lawrence Berkeley National Laboratory na Califórnia. Ele convenceu o inventor do ciclotron Ernest Lawrence a deixá-lo pegar de volta algumas partes do ciclotron descartadas que haviam se tornado radioativas . Lawrence enviou-lhe pelo correio uma folha de molibdênio que fazia parte do defletor do ciclotron.
Segrè convocou seu colega Perrier para tentar provar, por meio da química comparativa, que a atividade do molibdênio era de fato de um elemento com o número atômico 43. Em 1937, eles conseguiram isolar os isótopos tecnécio-95m e tecnécio-97 . Funcionários da Universidade de Palermo queriam que batizassem sua descoberta de " panormium ", em homenagem ao nome latino para Palermo , Panormus . Em 1947, o elemento 43 recebeu o nome da palavra grega τεχνητός , que significa "artificial", uma vez que foi o primeiro elemento a ser produzido artificialmente. Segrè voltou para Berkeley e conheceu Glenn T. Seaborg . Eles isolaram o isótopo metaestável tecnécio-99m , que agora é usado em cerca de dez milhões de procedimentos de diagnóstico médico anualmente.
Em 1952, a astronomia Paul W. Merrill na Califórnia detectada a assinatura espectral de tecnécio (especificamente os comprimentos de onda de 403,1 nm , 423,8 nm, 426,2 nm, e 429,7 nm) em função do tipo S- gigantes vermelhas . As estrelas estavam perto do fim de suas vidas, mas eram ricas no elemento de vida curta, o que indicava que estava sendo produzido nas estrelas por reações nucleares . Essa evidência reforçou a hipótese de que os elementos mais pesados são o produto da nucleossíntese nas estrelas. Mais recentemente, essas observações forneceram evidências de que os elementos são formados por captura de nêutrons no processo s .
Desde essa descoberta, tem havido muitas pesquisas em materiais terrestres por fontes naturais de tecnécio. Em 1962, o tecnécio-99 foi isolado e identificado na pechblenda do Congo Belga em quantidades extremamente pequenas (cerca de 0,2 ng / kg), onde se originou como um produto da fissão espontânea do urânio-238 . O reator de fissão nuclear natural de Oklo contém evidências de que quantidades significativas de tecnécio-99 foram produzidas e, desde então, decaíram em rutênio-99 .
Características
Propriedades físicas
O tecnécio é um metal radioativo cinza prateado com uma aparência semelhante à platina , comumente obtido como um pó cinza. A estrutura cristalina do metal puro a granel é hexagonal compactada . A estrutura cristalina do metal puro nanodisperso é cúbica . O tecnécio nanodisperso não tem um espectro de NMR dividido, enquanto o tecnécio hexagonal em massa tem o espectro de NMR Tc-99 dividido em 9 satélites. O tecnécio atômico tem linhas de emissão características em comprimentos de onda de 363,3 nm , 403,1 nm, 426,2 nm, 429,7 nm e 485,3 nm.
A forma do metal é ligeiramente paramagnética , o que significa que seus dipolos magnéticos se alinham com os campos magnéticos externos , mas assumirá orientações aleatórias assim que o campo for removido. Puro, metálico, tecnécio-cristal única torna-se um supercondutor de tipo II a temperaturas abaixo de 7,46 K . Abaixo dessa temperatura, o tecnécio tem uma profundidade de penetração magnética muito alta , maior do que qualquer outro elemento, exceto o nióbio .
Propriedades quimicas
O tecnécio está localizado no sétimo grupo da tabela periódica, entre o rênio e o manganês . Conforme previsto pela lei periódica , suas propriedades químicas estão entre esses dois elementos. Dos dois, o tecnécio se assemelha mais ao rênio, particularmente em sua inércia química e tendência a formar ligações covalentes . Isso é consistente com a tendência dos elementos do período 5 de se parecerem com seus correspondentes no período 6 mais do que no período 4 devido à contração dos lantanídeos . Ao contrário do manganês, o tecnécio não forma cátions ( íons com uma carga líquida positiva) prontamente . O tecnécio exibe nove estados de oxidação de -1 a +7, com +4, +5 e +7 sendo os mais comuns. O tecnécio se dissolve em água régia , ácido nítrico e ácido sulfúrico concentrado , mas não é solúvel em ácido clorídrico em qualquer concentração.
O tecnécio metálico mancha lentamente com o ar úmido e, na forma de pó, queima em oxigênio .
O tecnécio pode catalisar a destruição da hidrazina pelo ácido nítrico , e essa propriedade se deve à sua multiplicidade de valências. Isso causou um problema na separação do plutônio do urânio no processamento de combustível nuclear , onde a hidrazina é usada como um redutor protetor para manter o plutônio no estado trivalente em vez de no estado tetravalente mais estável. O problema foi agravado pela extração mutuamente aprimorada de tecnécio e zircônio por solvente no estágio anterior, e exigiu uma modificação do processo.
Compostos
Pertecnetato e derivados
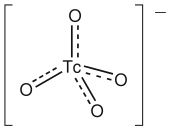
A forma mais prevalente de tecnécio e facilmente acessível é o pertecnetato de sódio, Na [TcO 4 ]. A maior parte deste material é produzida por decaimento radioativo de [ 99 MoO 4 ] 2− :
- [ 99 MoO 4 ] 2− → [ 99m TcO 4 ] - + e -
Pertecnetato (tetroxidotecnetato) TcO-
4comporta-se de forma análoga ao perclorato, ambos tetraédricos . Ao contrário do permanganato ( MnO-
4), é apenas um agente oxidante fraco.
Relacionado ao pertecnetato está o heptoxido . Este sólido volátil amarelo claro é produzido pela oxidação do metal Tc e precursores relacionados:
- 4 Tc + 7 O 2 → 2 Tc 2 O 7
É um exemplo muito raro de óxido de metal molecular, outros exemplos sendo OsO 4 e RuO 4 . Ele adota uma estrutura centrosimétrica com dois tipos de ligações Tc-O com comprimentos de ligação 167 e 184 pm.
Heptoóxido de tecnécio hidrolisa em pertecnetato e ácido pertecnético , dependendo do pH:
- Tc 2 O 7 + 2 OH - → 2 TcO 4 - + H 2 O
- Tc 2 O 7 + H 2 O → 2 HTcO 4
HTcO 4 é um ácido forte. Em ácido sulfúrico concentrado , [TcO 4 ] - converte-se na forma octaédrica TcO 3 (OH) (H 2 O) 2 , a base conjugada do hipotético complexo tri aquo [TcO 3 (H 2 O) 3 ] + .
Outros derivados de calcogeneto
O tecnécio forma um dióxido, dissulfeto , di- seleneto e di telureto . Um Tc 2 S 7 mal definido se forma ao tratar pertecnetato com sulfeto de hidrogênio. Ele se decompõe termicamente em dissulfeto e enxofre elementar. Da mesma forma, o dióxido pode ser produzido pela redução do Tc 2 O 7 .
Ao contrário do caso do rênio, um trióxido não foi isolado para o tecnécio. No entanto, o TcO 3 foi identificado na fase gasosa usando espectrometria de massa .
Complexos de hidreto e haleto simples
O tecnécio forma o complexo simples TcH2−
9. O sal de potássio é isoestrutural com ReH2−
9.
Os seguintes haletos de tecnécio binários (contendo apenas dois elementos) são conhecidos: TcF 6 , TcF 5 , TcCl 4 , TcBr 4 , TcBr 3 , α-TcCl 3 , β-TcCl 3 , TcI 3 , α-TcCl 2 e β- TcCl 2 . Os estados de oxidação variam de Tc (VI) a Tc (II). Os haletos de tecnécio exibem diferentes tipos de estrutura, como complexos octaédricos moleculares, cadeias estendidas, folhas em camadas e aglomerados de metal dispostos em uma rede tridimensional. Esses compostos são produzidos pela combinação do metal e do halogênio ou por reações menos diretas.
TcCl 4 é obtido por cloração de Tc metálico ou Tc 2 O 7. Após aquecimento, TcCl 4 dá os correspondentes cloretos de Tc (III) e Tc (II).
- TcCl 4 → α-TcCl 3 + 1/2 Cl 2
- TcCl 3 → β-TcCl 2 + 1/2 Cl 2
A estrutura do TcCl 4 é composta por infinitas cadeias em zigue-zague de octaedros TcCl 6 que compartilham a borda . É isomorfo aos tetracloretos de metal de transição de zircônio , háfnio e platina .
Existem dois polimorfos de tricloreto de tecnécio , α- e β-TcCl 3 . O polimorfo α também é denominado Tc 3 Cl 9 . Adota uma estrutura bioctaédrica confacial . É preparado tratando o cloroacetato Tc 2 (O 2 CCH 3 ) 4 Cl 2 com HCl. Como Re 3 Cl 9 , a estrutura do α-polimorfo consiste em triângulos com distâncias MM curtas. O β-TcCl 3 apresenta centros octaédricos de Tc, que são organizados em pares, como visto também para o tricloreto de molibdênio . O TcBr 3 não adota a estrutura de nenhuma das fases do tricloreto. Em vez disso, ele tem a estrutura de tribrometo de molibdênio , consistindo em cadeias de octaedros confaciais com contatos alternados de Tc-Tc curtos e longos. TcI 3 tem a mesma estrutura que a fase de alta temperatura de TiI 3 , apresentando cadeias de octaedros confaciais com contatos Tc-Tc iguais.
Vários haletos de tecnécio aniônicos são conhecidos. Os tetrahaletos binários podem ser convertidos em hexahalides [TcX 6 ] 2− (X = F, Cl, Br, I), que adotam geometria molecular octaédrica . Halogenetos mais reduzidos formam aglomerados aniônicos com ligações Tc – Tc. A situação é semelhante para os elementos relacionados de Mo, W, Re. Esses aglomerados têm a nuclearidade Tc 4 , Tc 6 , Tc 8 e Tc 13 . Os aglomerados mais estáveis de Tc 6 e Tc 8 têm formas de prisma em que pares verticais de átomos de Tc são conectados por ligações triplas e os átomos planares por ligações simples. Cada átomo de tecnécio faz seis ligações, e os elétrons de valência restantes podem ser saturados por um átomo de halogênio axial e dois ligantes em ponte , como cloro ou bromo .
Complexos de coordenação e organometálicos

O tecnécio forma uma variedade de complexos de coordenação com ligantes orgânicos. Muitos foram bem investigados devido à sua relevância para a medicina nuclear .
O tecnécio forma uma variedade de compostos com ligações Tc-C, ou seja, complexos organotecnécios. Membros proeminentes desta classe são complexos com ligantes CO, areno e ciclopentadienil. O carbonil binário Tc 2 (CO) 10 é um sólido volátil branco. Nesta molécula, dois átomos de tecnécio estão ligados um ao outro; cada átomo é cercado por octaedros de cinco ligantes carbonil. O comprimento da ligação entre os átomos de tecnécio, 303 pm, é significativamente maior do que a distância entre dois átomos em tecnécio metálico (272 pm). Carbonilos semelhantes são formados pelos congêneres do tecnécio , manganês e rênio. O interesse em compostos organotecnécios também foi motivado por aplicações em medicina nuclear . Incomum para outros carbonilos metálicos, Tc forma complexos aquo-carbonil, sendo proeminentes [Tc (CO) 3 (H 2 O) 3 ] + .
Isótopos
Tecnécio, com número atômico Z = 43, é o elemento de menor numeração na tabela periódica para a qual todos os isótopos são radioativos . O segundo elemento radioativo mais leve, o promécio , tem número atômico 61. Os núcleos atômicos com um número ímpar de prótons são menos estáveis do que aqueles com números pares, mesmo quando o número total de núcleos (prótons + nêutrons ) é par e ímpar elementos têm menos isótopos estáveis .
Os isótopos radioativos mais estáveis são o tecnécio-97 com meia-vida de 4,21 milhões de anos, o tecnécio-98 com 4,2 milhões de anos e o tecnécio-99 com 211.100 anos. Trinta outros radioisótopos foram caracterizados com números de massa variando de 85 a 118. A maioria deles tem meia-vida inferior a uma hora, as exceções sendo tecnécio-93 (2,73 horas), tecnécio-94 (4,88 horas), tecnécio- 95 (20 horas) e tecnécio-96 (4,3 dias).
O modo de decaimento primário para isótopos mais leves que o tecnécio-98 ( 98 Tc) é a captura de elétrons , produzindo molibdênio ( Z = 42). Para o tecnécio-98 e isótopos mais pesados, o modo primário é a emissão beta (a emissão de um elétron ou pósitron ), produzindo rutênio ( Z = 44), com a exceção de que o tecnécio-100 pode decair por emissão beta e captura de elétrons.
O tecnécio também possui numerosos isômeros nucleares , que são isótopos com um ou mais núcleons excitados . Tecnécio-97m ( 97m Tc; "m" significa metaestabilidade ) é o mais estável, com meia-vida de 91 dias e energia de excitação de 0,0965 MeV. Isto é seguido por tecnécio-95m (61 dias, 0,03 MeV) e tecnécio-99m (6,01 horas, 0,142 MeV). O tecnécio-99m emite apenas raios gama e decai em tecnécio-99.
Tecnécio-99 ( 99 Tc) é o principal produto da fissão do urânio-235 ( 235 U), tornando-o o isótopo de tecnécio mais comum e mais facilmente disponível. Um grama de tecnécio-99 produz 6,2 × 10 8 desintegrações por segundo (em outras palavras, a atividade específica de 99 Tc é 0,62 G Bq / g).
Ocorrência e produção
O tecnécio ocorre naturalmente na crosta terrestre em concentrações mínimas de cerca de 0,003 partes por trilhão. O tecnécio é tão raro porque as meias-vidas de 97 Tc e 98 Tc são de apenas 4,2 milhões de anos. Mais de mil desses períodos se passaram desde a formação da Terra , então a probabilidade de sobrevivência de até mesmo um átomo do tecnécio primordial é efetivamente zero. No entanto, pequenas quantidades existem como produtos de fissão espontânea em minérios de urânio . Um quilograma de urânio contém cerca de 1 nanograma (10 -9 g) equivalente a dez trilhões de átomos de tecnécio. Algumas estrelas gigantes vermelhas com os tipos espectrais S-, M- e N contêm uma linha de absorção espectral indicando a presença de tecnécio. Essas gigantes vermelhas são conhecidas informalmente como estrelas de tecnécio .
Produto residual da fissão
Em contraste com a rara ocorrência natural, grandes quantidades de tecnécio-99 são produzidas a cada ano a partir de barras de combustível nuclear usadas , que contêm vários produtos de fissão. A fissão de um grama de urânio-235 em reatores nucleares rende 27 mg de tecnécio-99, dando ao tecnécio um rendimento de produto da fissão de 6,1%. Outros isótopos físseis produzem rendimentos semelhantes de tecnécio, como 4,9% do urânio-233 e 6,21% do plutônio-239 . Estima-se que 49.000 T Bq (78 toneladas métricas ) de tecnécio foram produzidos em reatores nucleares entre 1983 e 1994, de longe a fonte dominante de tecnécio terrestre. Apenas uma fração da produção é usada comercialmente.
O tecnécio-99 é produzido pela fissão nuclear do urânio-235 e do plutônio-239. Portanto, está presente em resíduos radioativos e na precipitação nuclear de explosões de bombas de fissão . Sua decadência, medida em becquerels por quantidade de combustível irradiado, é o contribuinte dominante para a radioatividade do lixo nuclear após cerca de 10 4 a 10 6 anos após a criação do lixo nuclear. De 1945 a 1994, uma estimativa de 160 T Bq (cerca de 250 kg) de tecnécio-99 foi liberada no meio ambiente durante os testes nucleares atmosféricos . A quantidade de tecnécio-99 de reatores nucleares liberada no meio ambiente até 1986 é da ordem de 1000 TBq (cerca de 1600 kg), principalmente por reprocessamento de combustível nuclear ; a maior parte disso foi despejado no mar. Os métodos de reprocessamento reduziram as emissões desde então, mas a partir de 2005 a liberação primária de tecnécio-99 no meio ambiente foi pela planta de Sellafield , que liberou cerca de 550 TBq (cerca de 900 kg) de 1995 a 1999 no Mar da Irlanda . De 2000 em diante, a quantidade foi limitada pela regulamentação a 90 TBq (cerca de 140 kg) por ano. A descarga de tecnécio no mar resultou na contaminação de alguns frutos do mar com quantidades minúsculas deste elemento. Por exemplo, a lagosta europeia e os peixes do oeste de Cumbria contêm cerca de 1 Bq / kg de tecnécio.
Produto de fissão para uso comercial
O isótopo metaestável tecnécio-99m é continuamente produzido como um produto de fissão a partir da fissão de urânio ou plutônio em reatores nucleares :
Como o combustível usado pode permanecer por vários anos antes do reprocessamento, todo o molibdênio-99 e tecnécio-99m é decomposto no momento em que os produtos da fissão são separados dos principais actinídeos no reprocessamento nuclear convencional . O líquido deixado após a extração de plutônio-urânio ( PUREX ) contém uma alta concentração de tecnécio como TcO-
4 mas quase tudo isso é tecnécio-99, não tecnécio-99m.
A grande maioria do tecnécio-99m usado no trabalho médico é produzida irradiando alvos de urânio altamente enriquecido dedicados em um reator, extraindo molibdênio-99 dos alvos em instalações de reprocessamento e recuperando no centro de diagnóstico o tecnécio-99m produzido após a decomposição de molibdênio-99. Molibdênio-99 na forma de molibdato MoO2−
4é adsorvido em alumina ácida ( Al
2O
3) em um cromatógrafo de coluna blindada dentro de um gerador de tecnécio-99m ("vaca com tecnécio", também ocasionalmente chamada de "vaca com molibdênio"). O molibdênio-99 tem meia-vida de 67 horas, portanto, o tecnécio-99m de curta duração (meia-vida: 6 horas), que resulta de sua decomposição, está sendo produzido constantemente. O pertecnetato solúvel TcO -
4pode então ser extraído quimicamente por eluição com uma solução salina . Uma desvantagem desse processo é que ele requer alvos contendo urânio-235, que estão sujeitos às precauções de segurança de materiais físseis.

Quase dois terços do abastecimento mundial vêm de dois reatores; o National Research Universal Reactor da Chalk River Laboratories em Ontário, Canadá, e o High Flux Reactor do Nuclear Research and Consultancy Group em Petten, Holanda. Todos os principais reatores que produzem tecnécio-99m foram construídos na década de 1960 e estão próximos do fim de sua vida útil . Os dois novos reatores canadenses de experimentos em rede de física aplicada multifuncional , planejados e construídos para produzir 200% da demanda de tecnécio-99m, dispensaram todos os outros produtores de construir seus próprios reatores. Com o cancelamento dos reatores já testados em 2008, o futuro fornecimento de tecnécio-99m tornou-se problemático.
Depósito de lixo
A longa meia-vida do tecnécio-99 e seu potencial para formar espécies aniônicas cria uma grande preocupação para o descarte de resíduos radioativos em longo prazo . Muitos dos processos projetados para remover produtos de fissão em plantas de reprocessamento visam espécies catiônicas como césio (por exemplo, césio-137 ) e estrôncio (por exemplo, estrôncio-90 ). Conseqüentemente, o pertecnetato escapa por meio desses processos. As opções de disposição atuais favorecem o soterramento em rochas continentais geologicamente estáveis. O principal perigo com essa prática é a probabilidade de que os resíduos entrem em contato com a água, o que poderia liberar contaminação radioativa para o meio ambiente. O pertecnetato aniônico e o iodeto tendem a não se adsorver nas superfícies dos minerais e provavelmente serão removidos pela água. Em comparação , o plutônio , o urânio e o césio tendem a se ligar às partículas do solo. O tecnécio pode ser imobilizado por alguns ambientes, como a atividade microbiana nos sedimentos do fundo do lago, e a química ambiental do tecnécio é uma área de pesquisa ativa.
Um método alternativo de eliminação, a transmutação , foi demonstrado no CERN para o tecnécio-99. Nesse processo, o tecnécio (tecnécio-99 como alvo de metal) é bombardeado com nêutrons para formar o tecnécio-100 de vida curta (meia-vida = 16 segundos) que decai por decaimento beta em rutênio -100. Se a recuperação de rutênio utilizável for uma meta, um alvo de tecnécio extremamente puro é necessário; se pequenos traços de actinídeos menores , como amerício e cúrio, estiverem presentes no alvo, eles provavelmente sofrerão fissão e formarão mais produtos de fissão que aumentam a radioatividade do alvo irradiado. A formação de rutênio-106 (meia-vida de 374 dias) a partir da 'fissão recente' provavelmente aumentará a atividade do metal rutênio final, que então exigirá um tempo de resfriamento mais longo após a irradiação antes que o rutênio possa ser usado.
A separação real do tecnécio-99 do combustível nuclear usado é um processo longo. Durante o reprocessamento do combustível , ele sai como um componente do líquido residual altamente radioativo. Depois de ficar parado por vários anos, a radioatividade reduz a um nível em que a extração de isótopos de longa vida, incluindo o tecnécio-99, se torna viável. Uma série de processos químicos produz o metal tecnécio-99 de alta pureza.
Ativação de nêutrons
O molibdênio-99 , que decai para formar o tecnécio-99m, pode ser formado pela ativação de nêutrons do molibdênio-98. Quando necessário, outros isótopos de tecnécio não são produzidos em quantidades significativas por fissão, mas são fabricados por irradiação de nêutrons de isótopos originais (por exemplo, o tecnécio-97 pode ser feito por irradiação de nêutrons de rutênio-96 ).
Aceleradores de partículas
A viabilidade da produção de tecnécio-99m com o bombardeio de prótons de 22-MeV de um alvo de molibdênio-100 em ciclotrons médicos após a reação 100 Mo (p, 2n) 99m Tc foi demonstrada em 1971. A recente escassez de tecnécio-99m médico reacendeu o interesse em sua produção por bombardeio de prótons de alvos de molibdênio-100 isotopicamente enriquecidos (> 99,5%). Outras técnicas estão sendo investigadas para a obtenção de molibdênio-99 a partir de molibdênio-100 por meio de reações (n, 2n) ou (γ, n) em aceleradores de partículas.
Formulários
Medicina nuclear e biologia
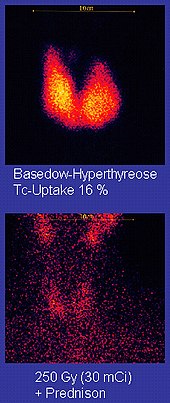
Tecnécio-99m ("m" indica que este é um isômero nuclear metaestável ) é usado em testes médicos de isótopos radioativos . Por exemplo, o Tecnécio-99m é um traçador radioativo que o equipamento de imagens médicas rastreia no corpo humano. É bem adequado para a função porque emite raios gama de 140 keV facilmente detectáveis e sua meia-vida é de 6,01 horas (o que significa que cerca de 94% dele decai para tecnécio-99 em 24 horas). A química do tecnécio permite que ele seja ligado a uma variedade de compostos bioquímicos, cada um dos quais determina como ele é metabolizado e depositado no corpo, e esse único isótopo pode ser usado para uma infinidade de testes diagnósticos. Mais de 50 radiofármacos comuns são baseados em tecnécio-99m para imagens e estudos funcionais do cérebro , músculo cardíaco, tireóide , pulmões , fígado , vesícula biliar , rins , esqueleto , sangue e tumores .
O isótopo de vida mais longa, tecnécio-95m com meia-vida de 61 dias, é usado como um traçador radioativo para estudar o movimento do tecnécio no meio ambiente e em sistemas vegetais e animais.
Industrial e Química
O tecnécio-99 decai quase inteiramente pelo decaimento beta, emitindo partículas beta com energias baixas consistentes e sem raios gama que os acompanham. Além disso, sua meia-vida longa significa que essa emissão diminui muito lentamente com o tempo. Ele também pode ser extraído com alta pureza química e isotópica de resíduos radioativos. Por essas razões, é um emissor beta padrão do Instituto Nacional de Padrões e Tecnologia (NIST) e é usado para calibração de equipamentos. O tecnécio-99 também foi proposto para dispositivos optoeletrônicos e baterias nucleares em nanoescala .
Como o rênio e o paládio , o tecnécio pode servir como catalisador . Em processos como a desidrogenação do álcool isopropílico , é um catalisador muito mais eficaz do que o rênio ou o paládio. No entanto, sua radioatividade é um grande problema em aplicações catalíticas seguras.
Quando o aço é imerso em água, adicionar uma pequena concentração (55 ppm ) de pertecnetato de potássio (VII) à água protege o aço da corrosão, mesmo se a temperatura subir para 250 ° C (523 K). Por esse motivo, o pertecnetato tem sido usado como um inibidor de corrosão anódica para aço, embora a radioatividade do tecnécio apresente problemas que limitam sua aplicação a sistemas independentes. Enquanto (por exemplo) CrO2−
4também pode inibir a corrosão, requer uma concentração dez vezes maior. Em um experimento, uma amostra de aço carbono foi mantida em uma solução aquosa de pertecnetato por 20 anos e ainda não estava corroída. O mecanismo pelo qual o pertecnetato evita a corrosão não é bem compreendido, mas parece envolver a formação reversível de uma fina camada superficial ( passivação ). Uma teoria sustenta que o pertecnetato reage com a superfície do aço para formar uma camada de dióxido de tecnécio que evita mais corrosão; o mesmo efeito explica como o pó de ferro pode ser usado para remover o pertecnetato da água. O efeito desaparece rapidamente se a concentração de pertecnetato cair abaixo da concentração mínima ou se uma concentração muito alta de outros íons for adicionada.
Conforme observado, a natureza radioativa do tecnécio (3 MBq / L nas concentrações exigidas) torna essa proteção contra corrosão impraticável em quase todas as situações. No entanto, a proteção contra corrosão por íons pertecnetato foi proposta (mas nunca adotada) para uso em reatores de água fervente .
Precauções
O tecnécio não desempenha nenhum papel biológico natural e não é normalmente encontrado no corpo humano. O tecnécio é produzido em quantidade por fissão nuclear e se espalha mais prontamente do que muitos radionuclídeos. Parece ter baixa toxicidade química. Por exemplo, nenhuma mudança significativa na fórmula sanguínea, pesos corporais e de órgãos, e consumo de alimentos puderam ser detectados para ratos que ingeriram até 15 µg de tecnécio-99 por grama de alimento por várias semanas. No corpo, o tecnécio é rapidamente convertido no TcO estável-
4íon, que é altamente solúvel em água e rapidamente excretado. A toxicidade radiológica do tecnécio (por unidade de massa) é uma função do composto, do tipo de radiação para o isótopo em questão e da meia-vida do isótopo.
Todos os isótopos de tecnécio devem ser manuseados com cuidado. O isótopo mais comum, o tecnécio-99, é um emissor beta fraco; essa radiação é interrompida pelas paredes dos utensílios de vidro do laboratório. O principal perigo ao trabalhar com tecnécio é a inalação de poeira; essa contaminação radioativa nos pulmões pode representar um risco significativo de câncer. Para a maioria dos trabalhos, o manuseio cuidadoso em uma capela é suficiente, e um porta - luvas não é necessário.
Notas
Referências
Bibliografia
- Emsley, J. (2001). Blocos de construção da natureza: um guia de AZ para os elementos . Oxford, Inglaterra, Reino Unido: Oxford University Press. ISBN 978-0-19-850340-8.
- Greenwood, NN; Earnshaw, A. (1997). Química dos Elementos (2ª ed.). Oxford: Butterworth-Heinemann. ISBN 978-0-7506-3365-9.
- Hammond, CR (2004). "Os elementos" . Handbook of Chemistry and Physics (81ª ed.). CRC press. ISBN 978-0-8493-0485-9.
- Schwochau, K. (2000). Tecnécio: Química e Aplicações Radiofarmacêuticas . Weinheim, Alemanha: Wiley-VCH. ISBN 978-3-527-29496-1.
Leitura adicional
- Choppin, G .; Liljenzin, J.-O. ; Rydberg, J. (2002). "Massa nuclear e estabilidade" . Radiochemistry and nuclearochemical (3ª ed.). Butterworth-Heinemann. pp. 41–57. ISBN 978-0-7506-7463-8.
- Algodão, FA; Wilkinson, G .; Murillo, CA; Bochmann, M. (1999). Advanced Inorganic Chemistry (6ª ed.). Nova York: John Wiley & Sons, Inc. ISBN 978-0-471-19957-1.
- Scerri, ER (2007). A tabela periódica, sua história e seu significado . Imprensa da Universidade de Oxford. ISBN 978-0-19-530573-9.
- Wilson, BJ, ed. (1966). The Radiochemical Manual (2ª ed.). ISBN 978-0-7058-1768-4.
- EnvironmentalChemistry.com - Technetium
- Gráfico de nuclídeos Nudat 2 do National Nuclear Data Center, Brookhaven National Laboratory
links externos
- Tecnécio na Tabela Periódica de Vídeos (University of Nottingham)



![{\ displaystyle {\ ce {^ {238} _ {92} U -> [{\ ce {sf}}] ^ {137} _ {53} I + ^ {99} _ {39} Y + 2 ^ { 1} _ {0} n}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/69e432873016029d0ca91cbd92c76fc15631fd66)
![{\ displaystyle {\ ce {^ {99} _ {39} Y -> [\ beta ^ -] [1,47 \, {\ ce {s}}] ^ {99} _ {40} Zr -> [\ beta ^ -] [2.1 \, {\ ce {s}}] ^ {99} _ {41} Nb -> [\ beta ^ -] [15.0 \, {\ ce {s}}] ^ {99} _ { 42} Mo -> [\ beta ^ -] [65,94 \, {\ ce {h}}] ^ {99} _ {43} Tc -> [\ beta ^ -] [211,100 \, {\ ce {y} }] ^ {99} _ {44} Ru}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/33a9d13cb741fa5c8efce11540847d7deac9654b)