terc-butil- lítio - tert-Butyllithium

|
|
|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
terc-butil- lítio |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| 3587204 | |
| ChemSpider | |
| ECHA InfoCard |
100,008,939 |
| Número EC | |
|
PubChem CID
|
|
| Número ONU | 3394 |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
|
LiC 4H 9 |
|
| Massa molar | 64,055 g mol −1 |
| Aparência | Sólido incolor |
| Densidade | 660 mg cm −3 |
| Ponto de ebulição | 36 a 40 ° C (97 a 104 ° F; 309 a 313 K) |
| Reage | |
| Acidez (p K a ) | 45–53 |
| Perigos | |
| Pictogramas GHS |
    
|
| Palavra-sinal GHS | Perigo |
| H225 , H250 , H260 , H300 , H304 , H310 , H314 , H330 , H336 , H411 | |
| P210 , P222 , P223 , P231 + 232 , P370 + 378 , P422 | |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | -6,6 ° C (20,1 ° F; 266,5 K) |
| Compostos relacionados | |
|
Compostos relacionados
|
n- butil-lítio |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
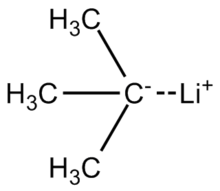
terc-butil- lítio é um composto químico com a fórmula (CH 3 ) 3 CLi. Como composto de organolítio , tem aplicações em síntese orgânica por ser uma base forte, capaz de desprotonar várias moléculas de carbono, incluindo o benzeno . o terc-butil- lítio está disponível comercialmente como soluções de hidrocarbonetos; geralmente não é preparado em laboratório. Sua síntese foi relatada pela primeira vez por RB Woodward em 1941.
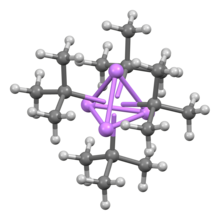
Estrutura e ligação
Como outros compostos de organolítio, o terc- butilítio é um aglomerado. Enquanto o n- butil-lítio existe tanto como hexâmero quanto como tetrâmero, o terc-butil- lítio existe como tetrâmero com uma estrutura cubana . A ligação em aglomerados de organolítio envolve a deslocalização sigma e a ligação Li-Li significativa.
A ligação lítio-carbono no terc- butil-lítio é altamente polarizada, tendo cerca de 40 por cento de caráter iônico . A molécula reage como um carbânion , representado por essas duas estruturas de ressonância . (Dados os cálculos de polaridade na ligação C – Li, a estrutura "real" de uma única molécula de t- butil-lítio é provavelmente uma média próxima dos dois contribuintes de ressonância mostrados, em que o átomo de carbono central tem uma taxa parcial de ~ 50% carga negativa, enquanto o átomo de lítio tem uma carga positiva parcial de ~ 50%.)
Propriedades quimicas
Semelhante ao n- butil-lítio , o terc- butil-lítio pode ser usado para a troca de lítio com halogênios e para a desprotonação de aminas e compostos C — H ativados.
Este composto e outros compostos alquil-lítio são conhecidos por reagir com solventes de éter; a meia-vida do terc- butil-lítio é de 60 minutos a 0 ° C em éter dietílico , 40 minutos a -20 ° C em tetra-hidrofurano (THF) e cerca de 11 minutos a -70 ° C em dimetoxietano . Neste exemplo, a reação de terc- butil-lítio com (THF) é mostrada:
Para minimizar a degradação por esses solventes, as reações envolvendo terc- butil-lítio são frequentemente conduzidas em temperaturas muito baixas em solventes especiais, como a mistura de solventes Trapp .
Segurança
o terc- butil-lítio é uma substância pirofórica , o que significa que se incendeia facilmente ao ser exposto ao ar. (Uma definição precisa de um material pirofórico é aquele "que se inflama espontaneamente no ar a 54,55 ° C (130,19 ° F) ou abaixo".) Os solventes usados em preparações comerciais comuns são eles próprios inflamáveis. Embora seja possível trabalhar com este composto usando a transferência de cânula , vestígios de terc- butil-lítio na ponta da agulha ou cânula podem pegar fogo e obstruir a cânula com sais de lítio. Enquanto alguns pesquisadores tomam este efeito de "luz piloto" como um sinal de que o produto é "fresco" e não se degradou devido ao tempo ou armazenamento / manuseio inadequado, outros preferem envolver a ponta da agulha ou cânula em um tubo de vidro curto, que é lavado com um gás inerte e selado em cada extremidade com septos. Ocorreram acidentes laboratoriais graves envolvendo terc- butil-lítio. Por exemplo, em 2008, um assistente de pesquisa da equipe, Sheharbano Sangji , no laboratório de Patrick Harran na Universidade da Califórnia, Los Angeles , morreu após ser gravemente queimado por um incêndio provocado por terc- butil-lítio.
As reações em grande escala podem levar a reações descontroladas, incêndios e explosões quando o terc- butil-lítio é misturado com éteres como o éter dietílico e o tetra-hidrofurano. O uso de solventes de hidrocarboneto pode ser preferido.
Técnicas sem ar são importantes para evitar que este composto reaja violentamente com o oxigênio e a umidade do ar:
- t -BuLi + O 2 → t -BuOOLi
- t -BuLi + H 2 O → t -BuH + LiOH




