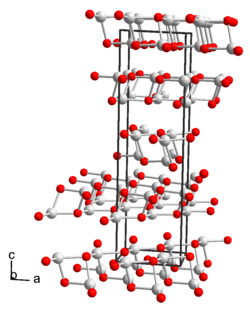
Hidróxido de tálio (I) - Thallium(I) hydroxide
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
hidróxido de tálio (I)
|
|
| Outros nomes
hidróxido taloso
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.031.540 |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| TlOH | |
| Massa molar | 221,390 g / mol |
| Aparência | agulhas amarelas |
| Densidade | 7,44 g / cm 3 |
| Ponto de fusão | decompõe-se a 139 ° C |
| 34,3 g / 100g a 18 ° C | |
| Perigos | |
| Riscos principais | Muito tóxico (T +)
Corrosivo (C) Perigoso para o meio ambiente (N) |
|
|
|
| NFPA 704 (diamante de fogo) | |
| Termoquímica | |
|
Entropia molar padrão ( S |
88,0 J · mol −1 · K −1 |
| -238,9 kJ · mol −1 | |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
Tálio (I), hidróxido , também chamado hidróxido thallous , TlOH, é um hidróxido de tálio , com tálio no estado de oxidação +1.
Síntese
O hidróxido de tálio (I) é obtido a partir da decomposição do etóxido de tálio (I) em água.
- C 2 H 5 OTl + H 2 O → TlOH + C 2 H 5 OH
Isso também pode ser feito pela reação direta do tálio com etanol e gás oxigênio .
- 4 Tl + 2 C 2 H 5 OH + O 2 → 2 C 2 H 5 OTl + 2 TlOH
Outro método é a reação entre sulfato de tálio (I) e hidróxido de bário .
- Tl 2 SO 4 + Ba (OH) 2 → 2 TlOH + BaSO 4
Propriedades
O hidróxido de talo é uma base forte; ele se dissocia ao íon taloso , Tl + , exceto em condições fortemente básicas. Tl + se assemelha a um íon de metal alcalino, A + , como Li + ou K + .
Referências
| Este artigo relacionado a compostos inorgânicos é um esboço . Você pode ajudar a Wikipedia expandindo-a . |

