Tetracloreto de titânio - Titanium tetrachloride

|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Cloreto de titânio (IV)
|
|
| Outros nomes
Tetracloreto de titânio
Tetraclorotitânio |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.028.584 |
| Número EC | |
| Malha | Titânio + tetracloreto |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| Número ONU | 1838 |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
|
TiCl 4 |
|
| Massa molar | 189,679 g / mol |
| Aparência | Líquido incolor |
| Odor | odor ácido penetrante |
| Densidade | 1,726 g / cm 3 |
| Ponto de fusão | −24,1 ° C (−11,4 ° F; 249,1 K) |
| Ponto de ebulição | 136,4 ° C (277,5 ° F; 409,5 K) |
| reage (hidrólise exotérmica) | |
| Solubilidade | solúvel em diclorometano , tolueno , pentano |
| Pressão de vapor | 1,3 kPa (20 ° C) |
| −54,0 · 10 −6 cm 3 / mol | |
|
Índice de refração ( n D )
|
1,61 (10,5 ° C) |
| Viscosidade | 827 μPa s |
| Estrutura | |
| Tetragonal | |
| Tetraédrico | |
| 0 D | |
| Termoquímica | |
|
Entropia molar padrão ( S |
355 J · mol −1 · K −1 |
| −763 kJ · mol −1 | |
| Perigos | |
| Ficha de dados de segurança | MSDS |
| Pictogramas GHS |
  
|
| Palavra-sinal GHS | Perigo |
| H314 , H317 , H318 , H330 , H335 , H370 , H372 | |
| P280 , P301 + 330 + 331 , P304 + 340 , P305 + 351 + 338 , P308 + 310 | |
| NFPA 704 (diamante de fogo) | |
| Compostos relacionados | |
|
Outros ânions
|
Brometo de titânio (IV) Fluoreto de titânio (IV) Iodeto de titânio (IV) |
|
Outros cátions
|
Cloreto de háfnio (IV) Cloreto de zircônio (IV) |
|
Compostos relacionados
|
Cloreto de titânio (II) Cloreto de titânio (III) |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O tetracloreto de titânio é o composto inorgânico com a fórmula TiCl 4 . É um importante intermediário na produção de titânio metálico e do pigmento dióxido de titânio . TiCl 4 é um líquido volátil . Ao entrar em contato com o ar úmido, forma nuvens opacas espetaculares de dióxido de titânio (TiO 2 ) e cloreto de hidrogênio hidratado . Às vezes é referido como "cócegas" ou "cócegas 4" devido à semelhança fonética de sua fórmula molecular (TiCl 4 ) com a palavra.
Propriedades e estrutura
TiCl 4 é um líquido destilável denso e incolor , embora as amostras brutas possam ser amarelas ou mesmo marrom-avermelhadas. É um dos raros halogenetos de metal de transição que é líquido à temperatura ambiente, sendo o VCl 4 outro exemplo. Esta propriedade reflete o fato de que as moléculas de TiCl 4 se autoassociam fracamente. A maioria dos cloretos metálicos são polímeros , em que os átomos de cloreto fazem a ponte entre os metais. Seus pontos de fusão e ebulição são semelhantes aos do CCl 4 .
O Ti 4+ possui uma concha eletrônica "fechada", com o mesmo número de elétrons que o gás inerte argônio . A estrutura tetraédrica do TiCl 4 é consistente com sua descrição como centro metálico ad 0 (Ti 4+ ) rodeado por quatro ligantes idênticos. Essa configuração leva a estruturas altamente simétricas , daí a forma tetraédrica da molécula. TiCl 4 adota estruturas semelhantes a TiBr 4 e TiI 4 ; os três compostos compartilham muitas semelhanças. TiCl 4 e TiBr 4 reagem para dar haletos mistos TiCl 4− x Br x , onde x = 0, 1, 2, 3, 4. As medições de ressonância magnética também indicam que a troca de haleto também é rápida entre TiCl 4 e VCl 4 .
TiCl 4 é solúvel em tolueno e clorocarbonos . Certos arenos formam complexos do tipo [(C 6 R 6 ) TiCl 3 ] + . TiCl 4 reage exotermicamente com solventes doadores , como THF, para dar adutos hexacoordenados . Ligantes mais volumosos (L) dão adutos pentacoordenados TiCl 4 L.
Produção
O TiCl 4 é produzido pelo processo de cloreto , que envolve a redução de minérios de óxido de titânio, tipicamente ilmenita (FeTiO 3 ), com carbono sob fluxo de cloro a 900 ° C. As impurezas são removidas por destilação .
- 2 FeTiO 3 + 7 Cl 2 + 6 C → 2 TiCl 4 + 2 FeCl 3 + 6 CO
A coprodução de FeCl 3 é indesejável, o que tem motivado o desenvolvimento de tecnologias alternativas. Em vez de usar diretamente ilmenita, "escória de rutilo" é usada. Este material, uma forma impura de TiO 2 , é derivado da ilmenita pela remoção do ferro, seja por redução de carbono ou extração com ácido sulfúrico . O TiCl 4 bruto contém uma variedade de outros haletos voláteis, incluindo cloreto de vanadil (VOCl 3 ), tetracloreto de silício (SiCl 4 ) e tetracloreto de estanho (SnCl 4 ), que devem ser separados.
Formulários
Produção de titânio metálico
O suprimento mundial de titânio metálico, cerca de 250.000 toneladas por ano, é feito de TiCl 4 . A conversão envolve a redução do tetracloreto com magnésio metálico. Este procedimento é conhecido como processo Kroll :
- 2 Mg + TiCl 4 → 2 MgCl 2 + Ti
No processo de Hunter , o sódio líquido é o agente redutor em vez do magnésio.
Produção de dióxido de titânio
Cerca de 90% da produção de TiCl 4 é usada para fazer o pigmento dióxido de titânio (TiO 2 ). A conversão envolve a hidrólise de TiCl 4 , um processo que forma cloreto de hidrogênio :
- TiCl 4 + 2 H 2 O → TiO 2 + 4 HCl
Em alguns casos, TiCl 4 é oxidado diretamente com oxigênio :
- TiCl 4 + O 2 → TiO 2 + 2 Cl 2
Telas de fumaça
Tem sido usado para produzir cortinas de fumaça, uma vez que produz uma fumaça branca e densa que tem pouca tendência a subir.
Reações químicas
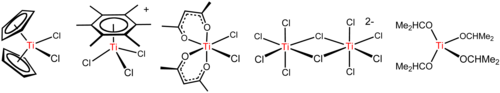
O tetracloreto de titânio é um reagente versátil que forma diversos derivados, incluindo os ilustrados abaixo.
A reação mais notável do TiCl 4 é sua fácil hidrólise , sinalizada pela liberação de cloreto de hidrogênio e formação de óxidos e oxicloretos de titânio , conforme descrito acima para a produção de TiO 2 . O tetracloreto de titânio tem sido usado para criar cortinas de fumaça navais . O cloreto de hidrogênio absorve imediatamente a água para formar um aerossol de ácido clorídrico que espalha a luz de maneira eficiente. Além disso, o dióxido de titânio altamente refrativo também é um dispersor de luz eficiente. Esta fumaça é corrosiva.
Os álcoois reagem com TiCl 4 para dar os alcóxidos correspondentes com a fórmula [Ti (OR) 4 ] n (R = alquil , n = 1, 2, 4). Conforme indicado por sua fórmula, esses alcóxidos podem adotar estruturas complexas que variam de monômeros a tetrâmeros. Esses compostos são úteis na ciência dos materiais , bem como na síntese orgânica . Um derivado bem conhecido é o isopropóxido de titânio , que é um monômero.
As aminas orgânicas reagem com TiCl 4 para dar complexos contendo complexos amido (contendo R 2 N - ) e imido ( contendo RN 2 -). Com a amônia, o nitreto de titânio é formado. Uma reação ilustrativa é a síntese de tetraquis (dimetilamido) titânio Ti (NMe 2 ) 4 , um líquido amarelo solúvel em benzeno: Esta molécula é tetraédrica, com centros de nitrogênio planos.
- 4 LiNMe 2 + TiCl 4 → 4 LiCl + Ti (NMe 2 ) 4
Complexos com ligantes simples
TiCl 4 é um ácido de Lewis como implicado por sua tendência a hidrolisar . Com o éter THF , TiCl 4 reage para dar cristais amarelos de TiCl 4 (THF) 2 . Com sais de cloreto, TiCl 4 reage para formar sequencialmente [Ti 2 Cl 9 ] - , [Ti 2 Cl 10 ] 2− (consulte a figura acima) e [TiCl 6 ] 2− . A reação de íons cloreto com TiCl 4 depende do contraíon. NBu 4 Cl e TiCl 4 dá o complexo pentacoordenado NBu 4 TiCl 5 , enquanto NEt menor +
4 dá (NEt 4 ) 2 Ti 2 Cl 10 . Essas reações destacam a influência da eletrostática nas estruturas de compostos com ligações altamente iônicas.
Redox
A redução de TiCl 4 com resultados de alumínio na redução de um elétron. O tricloreto ( TiCl 3 ) e o tetracloreto têm propriedades contrastantes: o tricloreto é um sólido, sendo um polímero de coordenação , e é paramagnético . Quando a redução é conduzida em solução de THF , o produto Ti (III) se converte no aduto azul claro TiCl 3 (THF) 3 .
Química Organometálica
A química organometálica do titânio normalmente começa com TiCl 4 . Uma reação importante envolve ciclopentadienil de sódio para dar dicloreto de titanoceno , TiCl 2 (C 5 H 5 ) 2 . Este composto e muitos de seus derivados são precursores dos catalisadores Ziegler-Natta . O reagente de Tebbe , útil em química orgânica, é um derivado de titanoceno contendo alumínio que surge da reação do dicloreto de titanoceno com trimetilalumínio . É usado para as reações de "olefinação".
Arenes , como C 6 (CH 3 ) 6 reagem para dar os complexos piano-tamborete [Ti (C 6 R 6 ) Cl 3 ] + (R = H, CH 3 ; ver figura acima). Esta reação ilustra a alta acidez de Lewis do TiCl +
3 entidade, que é gerada pela abstração de cloreto de TiCl 4 por AlCl 3 .
Reagente em síntese orgânica
O TiCl 4 encontra uso ocasional na síntese orgânica , capitalizando sua acidez de Lewis , sua oxofilicidade e as propriedades de transferência de elétrons de seus haletos de titânio reduzidos. É usado na adição de aldol catalisado por ácido de Lewis. A chave para esta aplicação é a tendência do TiCl 4 a ativar aldeídos (RCHO) pela formação de adutos como (RCHO) TiCl 4 OC (H) R.
Considerações de toxicidade e segurança
Os perigos apresentados pelo tetracloreto de titânio geralmente surgem da liberação de cloreto de hidrogênio (HCl). TiCl 4 é um ácido de Lewis forte , formando exotermicamente adutos mesmo com bases fracas como THF e explosivamente com água, liberando HCl.
Referências
Leitura geral
- Holleman, AF; Wiberg, E. (2001). Química Inorgânica . San Diego, CA: Academic Press. ISBN 978-0-12-352651-9 .
- Greenwood, Norman N .; Earnshaw, Alan (1997). Química dos Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8 .