Hidrogenação de transferência - Transfer hydrogenation
A hidrogenação de transferência é a adição de hidrogênio (H 2 ; dihidrogênio em química inorgânica e organometálica ) a uma molécula de uma fonte diferente de H 2 gasoso . Ela é aplicada na indústria e em síntese orgânica , em parte por causa da inconveniência e a despesa da utilização de H gasoso 2 . Uma aplicação em grande escala da hidrogenação por transferência é a liquefação de carvão usando "solventes doadores", como a tetralina .
Catalisadores organometálicos
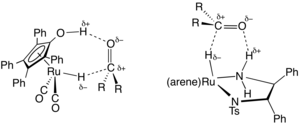
Na área de síntese orgânica , uma família útil de catalisadores de transferência de hidrogênio foi desenvolvida com base em complexos de rutênio e ródio , frequentemente com ligantes diamina e fosfina . Um precursor de catalisador representativo é derivado de dímero de dicloreto de rutênio (cimeno) e difeniletilenodiamina tosilada . Esses catalisadores são empregados principalmente para a redução de cetonas e iminas a álcoois e aminas , respectivamente. O doador de hidrogênio (agente de transferência) é tipicamente isopropanol , que se converte em acetona após a doação de hidrogênio. As hidrogenações de transferência podem prosseguir com altas enantiosseletividades quando o material de partida é pró - viral :
- RR'C = O + Me 2 CHOH → RR'C * H-OH + Me 2 C = O
onde RR'C * H-OH é um produto quiral. Um catalisador típico é (cimeno) R, R -HNCHPhCHPhNTs, em que Ts = SO 2 C 6 H 4 Me e R, R se refere à configuração absoluta dos dois centros de carbono quirais. Este trabalho foi reconhecido com o Prêmio Nobel de Química de 2001 para Ryōji Noyori .
Outra família de agentes de transferência de hidrogênio são aqueles baseados em alcóxidos de alumínio, como o isopropóxido de alumínio na redução de MPV ; no entanto, suas atividades são relativamente baixas em comparação com os sistemas baseados em metais de transição.
Rotas sem metal
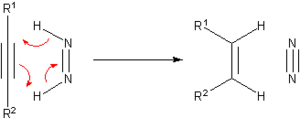
Antes do desenvolvimento da hidrogenação catalítica, muitos métodos foram desenvolvidos para a hidrogenação de substratos insaturados. Muitos desses métodos são apenas de interesse histórico e pedagógico. Um agente de hidrogenação de transferência proeminente é a diimida ou (NH) 2 , também chamada de diazeno . Este se torna oxidado em N 2 muito estável :
A diimida é gerada a partir da hidrazina . Dois hidrocarbonetos que podem servir como doadores de hidrogênio são o ciclohexeno ou o ciclohexadieno . Nesse caso, um alcano é formado, junto com um benzeno . O ganho de energia de estabilização aromática quando o benzeno é formado é a força motriz da reação. Pd pode ser usado como um catalisador e uma temperatura de 100 ° C é empregada. Hidrogenações de transferência mais exóticas foram relatadas, incluindo esta intramolecular:
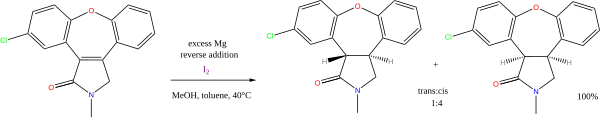
Existem muitas reações com álcool ou aminas como doadores de prótons e metais alcalinos como doadores de elétrons. De valor contínuo é a redução de arenos de bétula mediada por sódio metálico (outro nome para hidrocarbonetos aromáticos ). Menos importante atualmente é a redução de ésteres de Bouveault-Blanc . A combinação de magnésio e metanol é usada em reduções de alceno, por exemplo, a síntese de asenapina :
Hidrogenação por transferência organocatalítica
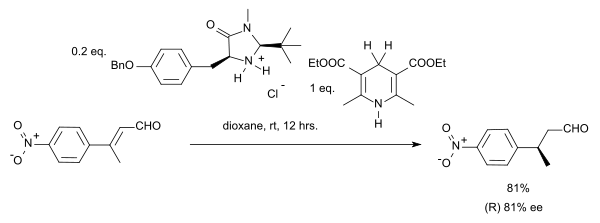
A hidrogenação por transferência organocatalítica foi descrita pelo grupo de List em 2004 em um sistema com um éster de Hantzsch como doador de hidreto e um catalisador de amina:
Nesta reação particular, o substrato é um composto de carbonil α, β-insaturado . O doador de prótons é oxidado à forma de piridina e se assemelha à coenzima bioquimicamente relevante NADH . No ciclo catalítico dessa reação, a amina e o aldeído formam primeiro um íon imínio , depois a transferência de prótons é seguida pela hidrólise da ligação imínio que regenera o catalisador. Ao adotar um organocatalisador de imidazolidinona MacMillan quiral, foi obtida uma enantioseletividade de 81% ee :
Em um caso de stereoconvergence , tanto o isómero E e o isómero Z em esta reacção se obter o (S) - enantiómero .
Estender o escopo desta reação para cetonas ou enonas requer o ajuste fino do catalisador (adicionar um grupo benzil e substituir o grupo t-butil por um furano ) e do éster de Hantzsch (adicionar grupos t-butil mais volumosos):
Com outro organocatalisador, a hidrogenação também pode ser realizada para iminas . Uma reação em cascata é catalisada por um ácido fosfórico quiral :
A reação prossegue por meio de um íon imínio quiral . Os catalisadores tradicionais à base de metal e a hidrogenação de substratos aromáticos ou heteroaromáticos tendem a falhar.
Referências
- ^ Speight, JG "The Chemistry and Technology of Coal" Marcel Dekker; Nova York, 1983; p. 226 ff. ISBN 0-8247-1915-8 .
- ^ Muñiz, Kilian (2005). "Catálise Bifuncional de Ligante Metálico: Hidrogenações e Novas Reações no Scaffold Metal- (Di) amina13". Edição internacional de Angewandte Chemie . 44 (41): 6622–6627. doi : 10.1002 / anie.200501787 . PMID 16187395 .
- ^ T. Ikariya, K. Murata, R. Noyori "Bifunctional Transition Metal-Based Molecular Catalysts for Asymmetric Syntheses" Org. Biomol. Chem., 2006, volume 4, 393-406.
- ^ Shimizu, H., Nagasaki, I., Matsumura, K., Sayo, N., e Saito, T. "Developments in Asymmetric Hydrogenation from an Industrial Perspective" Acc. Chem. Res. 2007, vol. 40, pp. 1385-1393. doi : 10.1021 / ar700101x
- ^ Linden, MVD; Roeters, T .; Harting, R .; Stokkingreef, E .; Gelpke, AS; Kemperman, G. (2008). "Eliminando os gargalos da rota de síntese da Asenapina". Pesquisa e desenvolvimento de processos orgânicos . 12 (2): 196–201. doi : 10.1021 / op700240c .
- ^ Yang; Hechavarria Fonseca, M .; List, B. (2004). "Uma hidrogenação de transferência sem metal: redução de conjugado organocatalítico de alfa, beta-aldeídos insaturados" . Angewandte Chemie International Edition em inglês . 43 (48): 6660–6662. doi : 10.1002 / anie.200461816 . PMID 15540245 .
- ^ Ouellet; Tuttle, J .; MacMillan, D. (2005). "Redução de hidreto organocatalítico enantiosseletiva". Journal of the American Chemical Society . 127 (1): 32–33. doi : 10.1021 / ja043834g . PMID 15631434 .
- ^ Tuttle; Ouellet, S .; MacMillan, D. (2006). "Organocatalytic transfer hydrhydrogenation of cyclic enones" (PDF) . Journal of the American Chemical Society . 128 (39): 12662–12663. doi : 10.1021 / ja0653066 . PMID 17002356 .
- ^ Rueping; Antonchick, A .; Theissmann, T. (2006). "Uma reação em cascata catalisada por ácido de Brønsted altamente enantiosseletiva: hidrogenação por transferência organocatalítica de quinolinas e sua aplicação na síntese de alcalóides". Angewandte Chemie International Edition em inglês . 45 (22): 3683–3686. doi : 10.1002 / anie.200600191 . PMID 16639754 .