Triosefosfato isomerase - Triosephosphate isomerase
| triosefosfato isomerase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
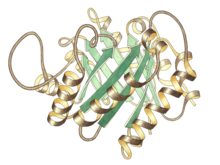 Vista lateral do monômero da triose P isomerase, sítio ativo no centro superior
| |||||||||
| Identificadores | |||||||||
| EC nº | 5.3.1.1 | ||||||||
| CAS no. | 9023-78-3 | ||||||||
| Bancos de dados | |||||||||
| IntEnz | Vista IntEnz | ||||||||
| BRENDA | Entrada BRENDA | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | Entrada KEGG | ||||||||
| MetaCyc | via metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBsum | ||||||||
| Ontologia Genética | AmiGO / QuickGO | ||||||||
| |||||||||
A triose-fosfato isomerase ( TPI ou TIM ) é uma enzima ( EC 5.3.1.1 ) que catalisa a interconversão reversível dos isômeros triose fosfato dihidroxiacetona fosfato e D- gliceraldeído 3-fosfato .
| Fosfato de diidroxiacetona | triose fosfato isomerase | D - gliceraldeído 3-fosfato | |

|

|
||

|
|||
| triose fosfato isomerase | |||
Composto C00111 no banco de dados KEGG Pathway. Enzima 5.3.1.1 no banco de dados KEGG Pathway. Composto C00118 no banco de dados KEGG Pathway.
O TPI desempenha um papel importante na glicólise e é essencial para a produção eficiente de energia. O TPI foi encontrado em quase todos os organismos pesquisados para a enzima, incluindo animais como mamíferos e insetos , bem como em fungos , plantas e bactérias . No entanto, algumas bactérias que não realizam a glicólise, como os ureaplasmas , não têm TPI.
Em humanos, as deficiências de TPI estão associadas a um distúrbio neurológico progressivo e grave denominado deficiência de triose fosfato isomerase . A deficiência de triose fosfato isomerase é caracterizada por anemia hemolítica crônica . Embora existam várias mutações que causam essa doença, a maioria inclui a substituição do ácido glutâmico na posição 104 por um ácido aspártico.
A triose fosfato isomerase é uma enzima altamente eficiente, realizando a reação bilhões de vezes mais rápido do que ocorreria naturalmente em solução. A reação é tão eficiente que é considerada cataliticamente perfeita : é limitada apenas pela taxa de difusão do substrato para dentro e para fora do sítio ativo da enzima.
Mecanismo
O mecanismo envolve a formação intermediária de um "enediol" . A energia livre relativa de cada estado fundamental e estado de transição foi determinada experimentalmente e é exibida na figura.
A estrutura do TPI facilita a conversão entre dihidroxiacetona fosfato (DHAP) e gliceraldeído 3-fosfato (GAP). O resíduo de glutamato 165 nucleofílico de TPI desprotona o substrato e o resíduo de histidina 95 eletrofílico doa um próton para formar o intermediário enodiol. Quando desprotonado, o enediolado então entra em colapso e, abstraindo um próton do glutamato protonado 165, forma o produto GAP. A catálise da reação reversa procede de forma análoga, formando o mesmo enediol, mas com o colapso do enediolato do oxigênio em C2.
TPI é limitado por difusão. Em termos de termodinâmica, a formação de DHAP é favorecida 20: 1 em relação à produção de GAP. No entanto, na glicólise, o uso de GAP nas etapas subsequentes do metabolismo conduz a reação em direção à sua produção. O TPI é inibido por íons sulfato , fosfato e arsenato , que se ligam ao sítio ativo . Outros inibidores incluem 2-fosfoglicolato, um análogo de estado de transição , e D-glicerol-1-fosfato, um análogo de substrato .
Estrutura
| Triosefosfato isomerase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||
| Símbolo | TIM | ||||||||
| Pfam | PF00121 | ||||||||
| Clã Pfam | CL0036 | ||||||||
| InterPro | IPR000652 | ||||||||
| PRÓSITO | PDOC00155 | ||||||||
| SCOP2 | 1tph / SCOPe / SUPFAM | ||||||||
| |||||||||
A triose fosfato isomerase é um dímero de subunidades idênticas , cada uma composta por cerca de 250 resíduos de aminoácidos . A estrutura tridimensional de uma subunidade contém oito hélices α na parte externa e oito fitas β paralelas na parte interna. Na ilustração, a estrutura da fita de cada subunidade é colorida de azul a vermelho do terminal N ao terminal C. Este motivo estrutural é chamado de αβ-barrel, ou TIM-barrel , e é de longe a dobra de proteína mais comumente observada . O sítio ativo desta enzima está no centro do barril. Um resíduo de ácido glutâmico e uma histidina estão envolvidos no mecanismo catalítico . A sequência em torno dos resíduos do sítio ativo é conservada em todas as triose fosfato isomerases conhecidas.
A estrutura da triose fosfato isomerase contribui para a sua função. Além dos resíduos de glutamato e histidina precisamente colocados para formar o enodiol, uma cadeia de dez ou onze aminoácidos de TPI atua como uma alça para estabilizar o intermediário. A alça, formada pelos resíduos 166 a 176, fecha e forma uma ligação de hidrogênio ao grupo fosfato do substrato. Esta ação estabiliza o intermediário enodiol e os outros estados de transição na via de reação.
Além de tornar a reação cineticamente viável, o loop TPI sequestra o intermediário enodiol reativo para evitar a decomposição em metilglioxal e fosfato inorgânico. A ligação de hidrogênio entre a enzima e o grupo fosfato do substrato torna tal decomposição estereeletronicamente desfavorável. O metilglioxal é uma toxina e, se formado, é removido pelo sistema da glioxalase . A perda de uma ligação de fosfato de alta energia e o substrato para o resto da glicólise tornam a formação de metilglioxal ineficiente.
Estudos sugerem que uma lisina próxima ao sítio ativo (na posição 12) também é crucial para a função enzimática. A lisina, protonada em pH fisiológico, pode ajudar a neutralizar a carga negativa do grupo fosfato. Quando este resíduo de lisina é substituído por um aminoácido neutro, o TPI perde todas as funções, mas as variantes com um aminoácido carregado positivamente diferente retêm alguma função.
Veja também
- Barril TIM
- Deficiência de Triose Fosfato Isomerase
- TPI1
- Triosefosfato isomerase em 3D interativo na Proteopedia
- Família triosefosfato isomerase (TIM) em PRÓSITO
Referências
links externos
- PDBe-KB fornece uma visão geral de todas as informações de estrutura disponíveis no PDB para Triosefosfato isomerase humano












