O catalisador de Wilkinson - Wilkinson's catalyst

|
|
|
|

|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
( SP -4) -cloridotris
|
|
| Outros nomes
Cloreto
de tris (trifenilfosfina) de ródio (I) , catalisador de Wilkinson , cloreto de tris (trifenilfosfina) de ródio (I) |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ECHA InfoCard |
100.035.207 |
| Número EC | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
| Propriedades | |
| C 54 H 45 ClP 3 Rh | |
| Massa molar | 925,22 g / mol |
| Aparência | sólido vermelho |
| Ponto de fusão | 245 a 250 ° C (473 a 482 ° F; 518 a 523 K) |
| Insolúvel em água | |
| Solubilidade em outros solventes | 20 g / L (CHCl 3 , CH 2 Cl 2 ), 2 g / L ( benzeno , tolueno ) |
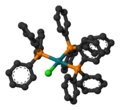
| Estrutura | |
planar quadrado
Magnetic nature :- Diamagnetic(d8configaration) Hibridização: -dsp2 |
|
| Perigos | |
| Riscos principais | Nenhum |
| Frases R (desatualizado) | Nenhum |
| Frases S (desatualizado) | S22 S24 / 25 |
| Compostos relacionados | |
|
Compostos relacionados
|
trifenilfosfina Pd (PPh 3 ) 4 IrCl (CO) [P (C 6 H 5 ) 3 ] 2 |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O catalisador de Wilkinson é o nome comum para chloridotris (trifenilfosfina) ródio (I) , um complexo de coordenação de ródio com a fórmula [RhCl (PPh 3 ) 3 ] (Ph = fenil ). É um sólido de cor vermelha acastanhada que é solúvel em solventes de hidrocarboneto, como benzeno, e mais ainda em tetra - hidrofurano ou solventes clorados, como diclorometano . O composto é amplamente utilizado como catalisador para hidrogenação de alquenos . É o nome em homenagem ao químico e Prêmio Nobel Sir Geoffrey Wilkinson , que primeiro popularizou seu uso.
Historicamente, o catalisador de Wilkinson tem sido um paradigma em estudos catalíticos levando a vários avanços no campo, como a implementação de alguns dos primeiros estudos de ressonância magnética heteronuclear para sua elucidação estrutural em solução ( 31 P), espectroscopia de polarização induzida por parahidrogênio para determinar o natureza de espécies reativas transitórias, ou uma das primeiras investigações cinéticas detalhadas por Halpern para elucidar o mecanismo. Além disso, os estudos catalíticos e organometálicos do catalisador de Wilkinson também desempenharam um papel significativo no desenvolvimento subsequente de catalisadores catiônicos de transferência de hidrogenação assimétricos baseados em Rh- e Ru que estabeleceram as bases para a catálise assimétrica moderna.
Estrutura e propriedades básicas
De acordo com a difração de raios-X de cristal único, o composto adota uma estrutura plana quadrada ligeiramente distorcida.
Ao analisar a ligação, é um complexo de Rh (I), um íon de metal de transição d 8 . Da perspectiva da regra dos 18 elétrons , os quatro ligantes fornecem, cada um, dois elétrons, para um total de 16 elétrons. Como tal, o composto é coordenativamente insaturado , ou seja, suscetível a substratos de ligação (alquenos e H 2 ). Em contraste, IrCl (PPh 3 ) 3 sofre ciclometalação para dar HIrCl (PPh 3 ) 2 (PPh 2 C 6 H 4 ), um complexo de Ir (III) coordenativamente saturado que não é cataliticamente ativo.
Síntese
O catalisador de Wilkinson é geralmente obtido tratando o cloreto de ródio (III) hidratado com um excesso de trifenilfosfina em etanol em refluxo. A trifenilfosfina atua como um agente redutor de dois elétrons que se oxida do estado de oxidação (III) para (V). Na síntese, três equivalentes da trifenilfosfina tornam-se ligantes no produto, enquanto o quarto reduz o ródio (III) a ródio (I).
- RhCl 3 (H 2 O) 3 + 4 PPh 3 → RhCl (PPh 3 ) 3 + OPPh 3 + 2 HCl + 2 H 2 O
Aplicações catalíticas
O catalisador de Wilkinson é mais conhecido por catalisar a hidrogenação de olefinas com hidrogênio molecular. O mecanismo dessa reação envolve a dissociação inicial de um ou dois ligantes de trifenilfosfina para dar complexos de 14 ou 12 elétrons, respectivamente, seguido pela adição oxidativa de H 2 ao metal. A subsequente complexação π de alcano, inserção migratória (transferência de hidreto intramolecular ou inserção de olefina) e eliminação redutiva completam a formação do produto alcano , por exemplo:
Em termos de suas taxas de hidrogenação, o grau de substituição no substrato de olefina é o fator chave, uma vez que a etapa de limitação de taxa no mecanismo é a inserção na olefina, que é limitada pelo impedimento estérico severo em torno do centro do metal. Na prática, alcenos terminais e di-substituídos são bons substratos, mas mais alcenos impedidos são mais lentos para hidrogenar. A hidrogenação de alcinos é difícil de controlar, uma vez que os alcinos tendem a ser reduzidos a alcanos, por intermédio do cis-alceno. O etileno reage com o catalisador de Wilkinson para dar RhCl (C 2 H 4 ) (PPh 3 ) 2 , mas não é um substrato para hidrogenação.
Processos catalíticos relacionados
O catalisador de Wilkinson também catalisa muitas outras reações de hidrofuncionalização , incluindo hidroacilação , hidroboração e hidrossililação de alcenos. Hydroborations têm sido estudados com o catecolborano e pinacolborano . Também é ativo para a hidrossililação de alquenos.
Na presença de base forte e hidrogênio, o catalisador de Wilkinson forma espécies Rh (I) reativas com atividades catalíticas superiores na hidrogenação de alcinos internos e alcenos tri-substituídos funcionalizados.
Reações
RhCl (PPh 3 ) 3 reage com monóxido de carbono para dar cloreto de bis (trifenilfosfina) ródio carbonil , trans- RhCl (CO) (PPh 3 ) 2 . O mesmo complexo surge da descarbonilação de aldeídos :
- RhCl (PPh 3 ) 3 + RCHO → RhCl (CO) (PPh 3 ) 2 + RH + PPh 3
Após agitação em solução de benzeno, RhCl (PPh 3 ) 3 se converte no dímero de cor vermelha pouco solúvel [RhCl (PPh 3 ) 2 ] 2 . Esta conversão demonstra ainda a labilidade dos ligantes de trifenilfosfina.
Na presença de base, H 2 e trifenilfosfina adicional, o complexo de Wilkinson se converte em hidridotetraquis (trifenilfosfina) ródio (I) , HRh (PPh 3 ) 4 . Este complexo 18e também é um catalisador de hidrogenação ativo.

