Trióxido de xenônio - Xenon trioxide
|
|
|
|
| Nomes | |
|---|---|
|
Nomes IUPAC
Trióxido de
xenônio Óxido de xenônio (VI) |
|
| Outros nomes
Anidrido xênico
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| XeO 3 | |
| Massa molar | 179,288 g / mol |
| Aparência | sólido cristalino incolor |
| Densidade | 4,55 g / cm 3 , sólido |
| Ponto de fusão | 25 ° C (77 ° F; 298 K) Decomposição violenta |
| Solúvel (com reação) | |
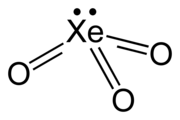
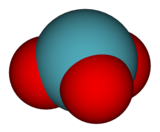
| Estrutura | |
| piramidal trigonal (C 3v ) | |
| Termoquímica | |
| 402 kJ · mol −1 | |
| Perigos | |
| NFPA 704 (diamante de fogo) | |
| Compostos relacionados | |
|
Compostos relacionados
|
Tetróxido de xenônio ácido xênico |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O trióxido de xenônio é um composto instável do xenônio em seu estado de oxidação +6 . É um agente oxidante muito poderoso e libera oxigênio da água lentamente, acelerado pela exposição à luz solar. É perigosamente explosivo em contato com materiais orgânicos. Quando ele detona, ele libera gás xenônio e oxigênio.
Química
O trióxido de xenônio é um forte agente oxidante e pode oxidar a maioria das substâncias que são oxidáveis. No entanto, é de ação lenta e isso reduz sua utilidade.
Acima de 25 ° C, o trióxido de xenônio é muito sujeito a explosões violentas:
Quando se dissolve em água, uma solução ácida de ácido xenico é formada:
- XeO 3 (aq) + H 2 O → H 2 XeO 4 ⇌ H + + HXeO-
4
Esta solução é estável à temperatura ambiente e não possui as propriedades explosivas do trióxido de xenônio. Oxida os ácidos carboxílicos quantitativamente em dióxido de carbono e água .
Alternativamente, ele se dissolve em soluções alcalinas para formar xenatos . O HXeO-
4ânion é a espécie predominante em soluções de xenato. Estes não são estáveis e começam a se desproporcionalmente em perxenatos (estado de oxidação +8) e gás xenônio e oxigênio. Perxenatos sólidos contendo XeO4−
6foram isolados pela reação de XeO
3com uma solução aquosa de hidróxidos. O trióxido de xenônio reage com fluoretos inorgânicos, como KF, RbF ou CsF para formar sólidos estáveis na forma MXeO
3F .
Propriedades físicas
A hidrólise de hexafluoreto de xénon ou tetrafluoreto de xénon produz uma solução a partir da qual incolor Xeo 3 cristais pode ser obtido por evaporação. Os cristais são estáveis por dias ao ar seco, mas absorvem prontamente a água do ar úmido para formar uma solução concentrada. A estrutura cristalina é ortorrômbica com a = 6,163 Å, b = 8,115 Å, c = 5,234 Å e 4 moléculas por célula unitária. A densidade é de 4,55 g / cm 3 .
 |
 |

|
| modelo ball-and-stick de parte da estrutura cristalina de XeO 3 |
modelo de preenchimento de espaço | geometria de coordenação de Xe |
Segurança
XeO 3 deve ser manuseado com muito cuidado. As amostras detonaram sem serem perturbadas à temperatura ambiente. Os cristais secos reagem explosivamente com a celulose.

