Cloreto de zircônio (IV) - Zirconium(IV) chloride

|
|
|
|

|
|
| Nomes | |
|---|---|
|
Nomes IUPAC
Tetracloreto de
zircônio Cloreto de zircônio (IV) |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100.030.041 |
| Número EC | |
|
PubChem CID
|
|
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| ZrCl 4 | |
| Massa molar | 233,04 g / mol |
| Aparência | cristais brancos higroscópicos |
| Densidade | 2,80 g / cm 3 |
| Ponto de fusão | 437 ° C (819 ° F; 710 K) (ponto triplo) |
| Ponto de ebulição | 331 ° C (628 ° F; 604 K) (sublimes) |
| hidrólise | |
| Solubilidade | HCl concentrado (com reação) |
| Estrutura | |
| Monoclínico , mP10 | |
| P12 / c1, No. 13 | |
| Termoquímica | |
|
Capacidade de calor ( C )
|
125,38 J K −1 mol −1 |
|
Entropia molar padrão ( S |
181,41 J K −1 mol −1 |
| -980,52 kJ / mol | |
| Perigos | |
| Ficha de dados de segurança | MSDS |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | Não inflamável |
| Dose ou concentração letal (LD, LC): | |
|
LD 50 ( dose mediana )
|
1688 mg / kg (oral, rato) 655 mg / kg (camundongo, oral) |
| Compostos relacionados | |
|
Outros ânions
|
Zircônio (IV) fluoreto Zircônio (IV) brometo Zircônio (IV) iodeto |
|
Outros cátions
|
Tetracloreto de titânio Tetracloreto de háfnio |
|
Compostos relacionados
|
Cloreto de zircônio (II) , cloreto de zircônio (III) |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O cloreto de zircônio (IV) , também conhecido como tetracloreto de zircônio , ( Zr Cl 4 ) é um composto inorgânico freqüentemente usado como precursor de outros compostos de zircônio. Este sólido branco de ponto de fusão alto hidrolisa rapidamente no ar úmido.
Estrutura
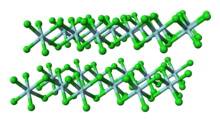
Ao contrário do TiCl 4 molecular , o ZrCl 4 sólido adota uma estrutura polimérica em que cada Zr é coordenado octaedricamente. Essa diferença de estruturas é responsável pela disparidade em suas propriedades: TiCl
4 é destilável, mas ZrCl
4 é um sólido. No estado sólido, o ZrCl 4 adota uma estrutura polimérica linear semelhante a uma fita - a mesma estrutura adotada pelo HfCl 4 . Este polímero degrada-se prontamente após tratamento com bases de Lewis , que clivam as ligações Zr-Cl-Zr.
Síntese
Esta conversão acarreta o tratamento do óxido com carbono como óxido "absorvente" e cloro.
- ZrO 2 + 2 C + 2 Cl 2 → ZrCl 4 + 2 CO
Um processo em escala de laboratório usa tetracloreto de carbono no lugar de carbono e cloro:
- ZrO 2 + 2 CCl 4 → ZrCl 4 + 2 COCl 2
Formulários
Precursor do metal Zr
O ZrCl 4 é um intermediário na conversão de minerais de zircônio em zircônio metálico pelo processo Kroll . Na natureza, os minerais de zircônio existem invariavelmente como óxidos (refletidos também pela tendência de hidrólise de todos os cloretos de zircônio). Para sua conversão em metal a granel, esses óxidos refratários são primeiro convertidos em tetracloreto, que pode ser destilado em altas temperaturas. O ZrCl 4 purificado pode ser reduzido com Zr metálico para produzir cloreto de zircônio (III) .
Outros usos
ZrCl 4 é o precursor mais comum para a deposição química de vapor de dióxido de zircônio e diboreto de zircônio .
Na síntese orgânica, o tetracloreto de zircônio é usado como um ácido de Lewis fraco para a reação de Friedel-Crafts , a reação de Diels-Alder e as reações de ciclização intramolecular. Ele também é usado para fazer tratamento repelente de água de têxteis e outros materiais fibrosos.
Propriedades e reações
A hidrólise do ZrCl 4 dá o aglomerado de hidroxicloreto hidratado denominado cloreto de zirconila . Esta reação é rápida e virtualmente irreversível, consistente com a alta oxofilicidade do zircônio (IV). Por esse motivo, as manipulações de ZrCl 4 normalmente requerem técnicas sem ar .
ZrCl 4 é o principal composto inicial para a síntese de muitos complexos organometálicos de zircônio. Devido à sua estrutura polimérica, o ZrCl 4 é geralmente convertido em um complexo molecular antes do uso. Forma um complexo 1: 2 com tetra - hidrofurano : CAS [21959-01-3], p.f. 175–177 ° C. NaC 5 H 5 reage com ZrCl 4 (THF) 2 para dar dicloreto de zirconoceno, ZrCl 2 (C 5 H 5 ) 2 , um complexo de organozircônio versátil. Uma das propriedades mais curiosas do ZrCl 4 é sua alta solubilidade na presença de benzenos metilados, como o durene . Esta solubilização surge através da formação de complexos π.
O log (base 10) da pressão de vapor de tetracloreto de zircónio (480-689 K) é dada pela equação: log 10 (P) = -5400 / T + 11,766, onde a pressão é medida em torr e a temperatura em graus Kelvin . O log (base 10) da pressão de vapor do tetracloreto de zircônio sólido (de 710 a 741 K) é dado pela equação log 10 (P) = −3427 / T + 9,088. A pressão no ponto de fusão é de 14.500 torrs.

