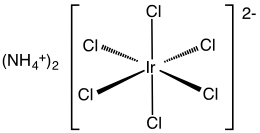
Hexacloroiridato de amônio (IV) - Ammonium hexachloroiridate(IV)
|
|

|
|
| Identificadores | |
|---|---|
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100.037.264 |
| Número EC | |
|
PubChem CID
|
|
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| H 8 N 2 Cl 6 Ir | |
| Massa molar | 441,01 |
| Aparência | cristais marrons |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
| Referências da Infobox | |
Hexacloroiridato de amônio (IV) é o composto inorgânico com a fórmula (NH 4 ) 2 [IrCl 6 ]. Este sólido marrom escuro é o sal de amônio do complexo de irídio (IV) [IrCl 6 ] 2− . É um composto de irídio comercialmente importante, um dos complexos mais comuns de irídio (IV). Um composto relacionado, mas mal definido, é o tetracloreto de irídio , que muitas vezes é usado alternadamente.
Estrutura
O composto foi caracterizado por cristalografia de raios-X . O sal cristaliza em um motivo cúbico como o do hexacloroplatinato de amônio . Os centros [IrCl 6 ] 2− adotam a geometria molecular octaédrica .
Usos
É um intermediário chave no isolamento de irídio de minérios. A maioria dos outros metais forma sulfetos insolúveis quando as soluções aquosas de seus cloretos são tratadas com sulfeto de hidrogênio , mas [IrCl 6 ] 2− resiste à substituição do ligante. Após o aquecimento sob hidrogênio, o sal sólido se converte no metal:
- (NH 4 ) 2 [IrCl 6 ] + 2 H 2 → Ir + 6 HCl + 2 NH 3
União
A estrutura eletrônica do hexacloroiridato de amônio (IV) tem atraído muita atenção. Seu momento magnético é menor do que o calculado para um elétron. Este resultado é interpretado como o resultado do acoplamento antiferromagnético entre centros Ir mediado por interações Cl-Cl. Ressonância do spin do elétron , estudos revelam que mais da metade da densidade do spin reside no cloreto, portanto, a descrição do complexo como Ir (IV) é uma simplificação excessiva.
