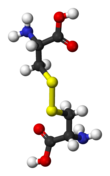
cistina - Cystine
|
| |||
| identificadores | |||
|---|---|---|---|
|
Modelo 3D ( JSmol )
|
|||
| Chebi | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.270 | ||
| KEGG | |||
|
PubChem CID
|
|||
| UNII | |||
| |||
| |||
| propriedades | |||
| C 6 H 12 N 2 O 4 S 2 | |||
| Massa molar | 240,29 g · mol -1 | ||
| Riscos | |||
| Ficha de segurança | MSDS External | ||
|
Excepto quando indicado de outra maneira, os dados são dados para materiais no seu estado normal (a 25 ° C [77 ° F], 100 kPa). | |||
|
<Ver TFM> verificar ( o que é <Ver TFM> ?)
| |||
| referências de Infobox | |||
Cistina é a forma dímero oxidado do aminoácido cisteína e tem a fórmula (SCH 2 CH (NH 2 ) CO 2 H) 2 . É um sólido branco que é ligeiramente solúvel em água. Ele serve duas funções biológicas: um local de redox reacções e uma ligação mecânica que permite que as proteínas conservam a sua estrutura tridimensional .
Conteúdo
Formação e reacções
É comum em muitos alimentos, como ovos, carne, produtos lácteos e grãos integrais, bem como de pele, chifres e cabelo. Não foi reconhecido como sendo derivados de proteínas , até que foi isolado a partir do chifre de uma vaca em 1899. O cabelo humano e pele contêm cerca de 10-14%, em massa, cistina. Ele foi descoberto em 1810 por William Hyde Wollaston .
redox
É formada a partir da oxidação de duas moléculas de cisteína, através da formação de uma ligação dissulfureto . Em biologia celular, cistina (encontrado em proteínas) só podem existir em organelos não-redutoras (oxidativas), tais como a via secretora (ER, Golgi, lisossomas, vesículas e ECM). Sob condições redutoras (no citoplasma, núcleo, etc.) cisteína é predominante. A ligação de dissulfureto é facilmente reduzida para se obter o correspondente tiol de cisteína . Tióis típicos para esta reacção são mercaptoetanol e o ditiotreitol :
- (SCH 2 CH (NH 2 ) CO 2 H) 2 + 2 RSH → 2 HSCH 2 CH (NH 2 ) CO 2 H + RSSR
Por causa da facilidade da troca tiol-dissulfeto, os benefícios nutricionais e fontes de cistina são idênticos àqueles para os mais-comum cisteína . As ligações dissulfureto clivar mais rapidamente a temperaturas mais elevadas.
distúrbios baseados em cistina
A presença de cistina na urina é frequentemente indicativa de defeitos de reabsorção de aminoácidos. Cistinúria foi relatado para ocorrer em cães. Nos seres humanos a excreção de níveis elevados de cristais de cistina pode ser indicativo de cistinose , uma doença genética rara.
transporte biológica
Cistina serve como um substrato para o antiportador cistina-glutamato . Este sistema de transporte, o qual é altamente específico para a cistina e glutamato, aumenta a concentração de cistina no interior da célula. Neste sistema, a forma aniônica de cistina é transportado em troca de glutamato. Cistina é rapidamente reduzido a cisteína. Pró-fármacos cisteinicos, por exemplo acetilcisteína , induzir a libertação de glutamato no espaço extracelular.
cabelo cistina suplementos nutricionais
suplementos de cisteína são por vezes comercializados como produtos anti-envelhecimento com reivindicações de melhoria da elasticidade da pele. Cisteína é mais facilmente absorvido pelo organismo do que cistina, por isso a maioria dos suplementos contêm cisteína em vez de cistina. N-acetil-cisteína (NAC) é melhor absorvidos do que os outros de cisteína ou cistina suplementos.
Veja também
- Lantionina , semelhante com mono ligação sulfureto
- estrutura terciária das proteínas
- reacção Sullivan
- cistinose
Referências
- ^ Nelson, DL; Cox, MM; Lehninger, Principies of Biochemistry . 3ª Ed. Worth Publishing: New York, 2000. ISBN 1-57259-153-6 .
- ^ "Cistina". Encyclopædia Britannica . 2007. Encyclopædia Britannica Online. 27 de julho de 2007 www.britannica.com/eb/article-9028437/cystine
- ^ Gortner, RA; WF Hoffman, WF (1941). "L-cistina" . Sínteses orgânicas .; Volume Collective , 1 , p. 194
- ^ MA Aslaksena; OH Romarheima; T. Storebakkena; A. Skrede (28 Junho de 2006). "Avaliação de conteúdo e digestibilidade de ligações dissulfureto e tis livres em dietas unextruded e extrudidos contendo farinha de peixe e fontes de proteína de soja". Animal Feed Science and Technology . 128 (3-4): 320-330. doi : 10.1016 / j.anifeedsci.2005.11.008 .
- ^ Gahl, William A .; Thoene, Jess G .; Schneider, Jerry A. (2002). "A cistinose". New England Journal of Medicine . 347 (2): 111-121. doi : 10,1056 / NEJMra020552 . ISSN 0028-4793 . PMID 12110740 .