Óxido de manganês (II, III) - Manganese(II,III) oxide
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
óxido de dimanganês (III) de manganês (II)
|
|
| Outros nomes
Tetróxido de manganês; Óxido de manganês, óxido manganomanganês, tetraóxido de trimanganês, tetróxido de trimanganês
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ECHA InfoCard |
100.013.879 |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| Mn 3 O 4 MnO · Mn 2 O 3 |
|
| Massa molar | 228,812 g / mol |
| Aparência | pó preto acastanhado |
| Densidade | 4,86 g / cm 3 |
| Ponto de fusão | 1.567 ° C (2.853 ° F; 1.840 K) |
| Ponto de ebulição | 2.847 ° C (5.157 ° F; 3.120 K) |
| insolúvel | |
| Solubilidade | solúvel em HCl |
| + 12.400 · 10 −6 cm 3 / mol | |
| Estrutura | |
| Espinélio (tetragonal), tI 28 | |
| I 4 1 / amd, No. 141 | |
| Perigos | |
| NIOSH (limites de exposição à saúde dos EUA): | |
|
PEL (permitido)
|
C 5 mg / m 3 |
|
REL (recomendado)
|
Nenhum estabelecido |
|
IDLH (perigo imediato)
|
WL |
| Termoquímica | |
|
Entropia molar padrão ( S |
149 J · mol −1 · K −1 |
| −1387 kJ · mol −1 | |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O óxido de manganês (II, III) é o composto químico com a fórmula Mn 3 O 4 . O manganês está presente em dois estados de oxidação +2 e +3 e a fórmula às vezes é escrita como MnO · Mn 2 O 3 . O Mn 3 O 4 é encontrado na natureza como o mineral hausmanita .
Preparação
Mn 3 O 4 formado quando qualquer óxido de manganês é aquecido ao ar acima de 1000 ° C. Uma pesquisa considerável tem se concentrado na produção de Mn 3 O 4 nanocristalino e várias sínteses que envolvem a oxidação de Mn II ou a redução de Mn VI .
Reações
Verificou-se que o Mn 3 O 4 atua como um catalisador para uma série de reações, por exemplo, a oxidação do metano e do monóxido de carbono; a decomposição do NO, a redução do nitrobenzeno e a combustão catalítica de compostos orgânicos.
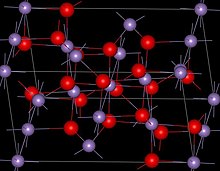
Estrutura
O Mn 3 O 4 tem a estrutura espinélica , onde os íons óxido são compactados cúbicos e o Mn II ocupa sítios tetraédricos e os sítios octaédricos Mn III . A estrutura está distorcida devido ao efeito Jahn – Teller . À temperatura ambiente, o Mn 3 O 4 é paramagnético , abaixo de 41-43 K, é ferrimagnético, embora tenha sido relatado como uma redução em amostras nanocristalinas para cerca de 39 K.
Usos
O Mn 3 O 4 é às vezes usado como matéria-prima na produção de ferritas moles, por exemplo, ferrita de zinco e manganês e óxido de lítio-manganês, usados em baterias de lítio.
O tetróxido de manganês também pode ser usado como um agente de ponderação durante a perfuração de seções de reservatório em poços de petróleo e gás.
