Tetrametilbutano - Tetramethylbutane
|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
2,2,3,3-Tetrametilbutano |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100,008,961 |
| Número EC | |
|
PubChem CID
|
|
| UNII | |
| Número ONU | 13: 25h |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 8 H 18 | |
| Massa molar | 114,232 g · mol −1 |
| Aparência | Cristais brancos, opacos e cerosos |
| Odor | Inodoro |
| Ponto de fusão | 98 a 104 ° C; 208 a 219 ° F; 371 a 377 K |
| Ponto de ebulição | 106,0 a 107,0 ° C; 222,7 a 224,5 ° F; 379,1 a 380,1 K |
|
Constante da lei de Henry ( k H ) |
2,9 nmol Pa −1 kg −1 |
| Termoquímica | |
|
Capacidade de calor ( C )
|
232,2 JK −1 mol −1 (a 2,8 ° C) |
|
Entropia molar padrão ( S |
273,76 JK −1 mol −1 |
| −270,3 - −267,9 kJ mol −1 | |
| −5,4526 - −5,4504 MJ mol −1 | |
| Perigos | |
|
|
|
| Frases R (desatualizado) | R11 , R38 , R65 , R67 , R50 / 53 |
| Frases S (desatualizado) | (S2) , S16 , S29 , S33 |
| Ponto de inflamação | 4 ° C (39 ° F; 277 K) |
| Limites explosivos | 1 -?% |
| Compostos relacionados | |
|
Alcanos relacionados
|
|
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
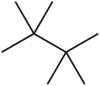
O tetrametilbutano , às vezes denominado hexametiletano , é um hidrocarboneto com a fórmula C 8 H 18 ou (H 3 C-) 3 C-C (-CH 3 ) 3 . É o mais ramificado e mais compacto dos muitos isômeros de octanagem , o único com um backbone de butano (C4). Por causa de sua estrutura altamente simétrica, tem um ponto de fusão muito alto e um curto alcance de líquido; na verdade, é o menor hidrocarboneto acíclico saturado que aparece como um sólido a uma temperatura ambiente de 25 ° C. (Entre os hidrocarbonetos cíclicos, o cubano , C 8 H 8 é ainda menor e também é sólido à temperatura ambiente.) É também o isômero C 8 H 18 mais estável , com um calor de formação 4,18 kcal / mol menor que o de n - octano, fato que tem sido atribuído às interações dispersivas estabilizadoras ( correlação eletrônica ) entre os grupos metil (protobranqueamento).
O composto pode ser obtido por reação do reagente de Grignard brometo de terc- butilmagnésio com brometo de etila , ou de brometo de etilmagnésio com brometo de terc- butila na presença de íons manganês ( II ). Acredita-se que essa transformação passe pela dimerização de dois radicais terc-butila, que são gerados pela decomposição dos compostos organomanganês gerados in situ.
O nome IUPAC completo do composto é 2,2,3,3-tetrametilbutano , mas os números são supérfluos neste caso porque não há outro arranjo possível de "tetrametilbutano".
