AGGF1 - AGGF1
O fator angiogênico com patch G e domínios FHA 1 é uma proteína que em humanos é codificada pelo gene AGGF1 .
AGGF1 é um gene humano que funciona como um fator angiogênico com um patch G e domínio associado a forkhead . Este gene é predominantemente expresso em células endoteliais rechonchudas ativadas e atua regulando a angiogênese e o desenvolvimento vascular. AGGF1 é conhecido por interagir com uma ampla gama de proteínas envolvidas no desenvolvimento vascular. Mutações em AGGF1 foram implicadas em vários tipos de câncer e é conhecido por causar a rara condição congênita, a síndrome de Klippel-Trenaunay .
Gene
O gene foi originalmente denominado VG5Q, indicando que era um gene vascular no cromossomo 5, mas o nome foi alterado posteriormente para refletir sua função, em vez de apenas sua localização.
O promotor do gene AGGF1 não contém uma caixa TATA e contém 2 locais de início da transcrição que são -367 e -364 pares de bases à frente do local de início da tradução de base. O promotor do gene contém mais de 50 ilhas CpG , o que o torna um alvo de metilação do DNA . AGGF1 é regulado por 2 locais repressores e 2 locais ativadores. Embora a presença de 2 locais repressores e 2 ativadores seja clara, o único fator de transcrição conhecido que regula AGGF1 é o GATA1. GATA1 se liga a montante do promotor do gene AGGF1 em -295 e -300, e a ligação de GATA1 levará ao aumento da expressão de AGGF1. Para que o gene seja totalmente expresso, ambos os sítios ativadores devem ser ligados pelos fatores de transcrição, GATA1 e outro fator desconhecido.
Proteína
Para formar uma proteína, um transcrito de mRNA deve ser transcrito a partir do DNA. Para AGGF1, o transcrito do mRNA contém 14 exons e 34 807 nucleotídeos.
Esta proteína contém 714 aminoácidos e tem um peso molecular de 80997 Da. Ele contém um domínio em espiral enrolada nas posições 18-88 e um domínio OCRE no terminal N . O domínio do patch G está localizado nos aminoácidos 619-663, enquanto o domínio associado à forkhead está localizado nos aminoácidos 435-508. Embora seja conhecido que esses domínios estão presentes na proteína, seu papel na função da proteína permanece obscuro.
AGGF1 foi o terceiro gene humano haploinsuficiente identificado. Haploinsuficiência significa que AGGF1 é "dependente da dose", portanto, quaisquer reduções no produto proteico podem ter consequências fenotípicas no desenvolvimento vascular do organismo.
Expressão
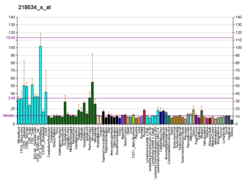
AGGF1 é amplamente expresso durante a especificação inicial da veia embrionária e a expressão aumenta quando as células endoteliais são ativadas. Embora AGGF1 seja predominantemente funcional em células endoteliais , células do músculo liso vascular e osteoblastos , também tem atividade em mastócitos , células cardíacas, células de Kupffer e células-tronco hematopoiéticas . O mRNA de AGGF1 foi detectado no coração, rins e membros, o que indica que a proteína provavelmente também funciona nesses órgãos. A proliferação de células do músculo liso vascular é inibida quando o AGGF1 é expresso. Foi descoberto que AGGF1 é altamente expresso em alguns tumores malignos que implicaram AGGF1 no câncer. Modelos in vitro mostraram que AGGF1 se localiza na periferia da célula e diretamente fora da célula.
Dependendo do tipo de mutação, as mutações de AGGF1 podem ser letais no genótipo heterozigoto ou homozigoto devido à sua haploinsuficiência. Os modelos de camundongos mostraram que as mutações heterozigotas podem causar fatalidade devido à hemorragia, enquanto as mutações homozigotas podem impedir a diferenciação adequada das células-tronco.
Homologia
Aggf1 não é exclusivo para humanos. Este gene é conservado em muitas espécies, como chimpanzés, macacos Rhesus, cães, vacas, camundongos, ratos, galinhas e sapos. Existem 212 organismos que possuem genes que são ortólogos para AGGF1.
Dentro do cromossomo humano, existem pseudogenes relacionados ao AGGF1 localizados nos cromossomos 3, 4, 10 e 16 que provavelmente surgiram devido a eventos de translocação .
Função
AGGF1 funciona para regular a angiogênese e o desenvolvimento vascular. A ontologia genética também implicou AGGF1 na adesão celular, regulação positiva da angiogênese e proliferação de células endoteliais. Além disso, foi demonstrado que o AGGF1 protege contra inflamação e lesões isquêmicas. Durante a embriogênese, o AGGF1 é necessário para a especificação de células-tronco hematopoéticas e a diferenciação de linhagens de células hematopoiéticas e endoteliais. Especificamente, ele regula a caderina endotelial vascular (VE-caderina) inibindo a fosforilação da caderina e aumentando sua presença na membrana plasmática das células endoteliais. AGGF1 é crítico para a especificação de veias e hemanigioblastos multipotentes , anti-inflamatórios, angiogênese tumoral e inibição da permeabilidade vascular. Além disso, ativa a autofagia em tipos específicos de células, como células endoteliais , células cardíacas HL1 e H9C2 e células do músculo liso vascular .
Interações
AGGF1 interage direta e indiretamente com muitas proteínas. Existem interações diretas entre AGGF1 e TNFSF12 , outro fator angiogênico secretado, que leva ao aumento da angiogênese. AGGF1 atua a montante de genes de hemangioblast, como scl, fil1 e etsrp. AGGF1 atua de forma semelhante ao VEGF - outro gene implicado no crescimento vascular. Além disso, o AGGF1 é conhecido por ativar as subunidades catalíticas e regulatórias da PI3K . Isso leva à ativação a jusante da via de sinalização AKT , GSK3b e p70S6K que leva à especificação da veia e angiogênese. AGGF1 também interage com marcadores específicos da veia, como em flt4 , dab2 e ephB4 . Ccl2 também demonstrou interagir com AGGF1 em hepatócitos através do bloqueio de NF-κB / p65 de ligação a Ccl2. A atividade AGGF1 é eliminada quando Elk é superexpresso. AGGF1 regula a autofagia regulando a expressão de genes JNK. SMAD7 e Aggf1 directamente interagem no fígado a fibrogénese inibição. A presença de DNMT3b irá reprimir AGGF1 agindo na região promotora do gene.
Significado clínico
Síndrome de Klippel-Trenaunay
Mutações heterogêneas neste gene, causando desregulação da expressão, podem levar às malformações vasculares associadas à síndrome de Klippel-Trenaunay (KTS). Devido à natureza haploinsuficiente do AGGF1, os indivíduos que possuem até mesmo um alelo mutante podem ter KTS. Estudos feitos em modelos de camundongos mostraram hemorragias frequentes e aumento da permeabilidade vascular em camundongos que são heterozigotos para Aggf1. Uma translocação entre o braço q do cromossomo 5 na região 13 na banda 3 e o braço p do cromossomo 11 na região 15 na banda 1 foi implicada no KTS. Esta translocação afeta o promotor AGGF1, portanto, há um aumento de 3 vezes na produção de proteína. Polimorfismos de nucleotídeo único no íntron 11 e exon 7 foram associados à suscetibilidade a KTS, embora nenhum desses SNPs resultou em uma mudança de aminoácido. Em um ponto, o alelo E133K foi pensado para ser um hotspot mutacional - devido à fosforilação alterada - causando KTS, mas desde então foi descoberto que até 3,3% da população são portadores da mutação.
Doença cardíaca
AGGF1 também foi implicado no tratamento após dano às células do músculo liso vascular devido à doença arterial coronariana e infarto do miocárdio . Ao bloquear a permeabilidade vascular e regular a troca fenotípica das células do músculo liso vascular, a terapia com proteína AGGF1 está sendo investigada como um novo método de tratamento de ambas as doenças.
Câncer
O AGGF1 aberrante tem sido implicado em vários cânceres e funções na iniciação e progressão tumoral. Por exemplo, a sobrevivência do carcinoma hepatocelular e do câncer gástrico está relacionada aos níveis de expressão de AGGF1 em tumores. Foi descoberto que AGGF1 tem maior expressão em tumores do que nos tecidos circundantes, e níveis mais altos de AGGF1 estão associados a um prognóstico ruim do paciente.
Veja também
Referências
Leitura adicional
- Timur AA, Driscoll DJ, Wang Q (julho de 2005). "Biomedicina e doenças: a síndrome de Klippel-Trenaunay, anomalias vasculares e morfogênese vascular" . Cellular and Molecular Life Sciences . 62 (13): 1434–47. doi : 10.1007 / s00018-005-4523-7 . PMC 1579804 . PMID 15905966 .
- Kihiczak GG, Meine JG, Schwartz RA, Janniger CK (agosto de 2006). "Síndrome de Klippel-Trenaunay: uma doença multissistêmica possivelmente resultante de um gene patogênico para crescimento excessivo de tecido e vascular". International Journal of Dermatology . 45 (8): 883–90. doi : 10.1111 / j.1365-4632.2006.02940.x . PMID 16911369 . S2CID 7238399 .
- Dias Neto E, Correa RG, Verjovski-Almeida S, Briones MR, Nagai MA, da Silva W, Zago MA, Bordin S, Costa FF, Goldman GH, Carvalho AF, Matsukuma A, Baia GS, Simpson DH, Brunstein A, de Oliveira PS, Bucher P, Jongeneel CV, O'Hare MJ, Soares F, Brentani RR, Reis LF, de Souza SJ, Simpson AJ (março de 2000). "Sequenciamento Shotgun do transcriptoma humano com marcadores de sequência expressos de ORF" . Anais da Academia Nacional de Ciências dos Estados Unidos da América . 97 (7): 3491–6. doi : 10.1073 / pnas.97.7.3491 . PMC 16267 . PMID 10737800 .
- Tian XL, Kadaba R, You SA, Liu M, Timur AA, Yang L, Chen Q, Szafranski P, Rao S, Wu L, Housman DE, DiCorleto PE, Driscoll DJ, Borrow J, Wang Q (fevereiro de 2004). "Identificação de um fator angiogênico que, quando mutado, causa suscetibilidade à síndrome de Klippel-Trenaunay" . Nature . 427 (6975): 640–5. doi : 10.1038 / nature02320 . PMC 1618873 . PMID 14961121 .
- Callebaut I, Mornon JP (março de 2005). "OCRE: um novo domínio feito de repetições de octâmero imperfeitas e ricas em aromáticos" . Bioinformática . 21 (6): 699–702. doi : 10.1093 / bioinformática / bti065 . PMID 15486042 .
- Rual JF, Venkatesan K, Hao T, Hirozane-Kishikawa T, Dricot A, Li N, Berriz GF, Gibbons FD, Dreze M, Ayivi-Guedehoussou N, Klitgord N, Simon C, Boxem M, Milstein S, Rosenberg J, Goldberg DS, Zhang LV, Wong SL, Franklin G, Li S, Albala JS, Lim J, Fraughton C, Llamosas E, Cevik S, Bex C, Lamesch P, Sikorski RS, Vandenhaute J, Zoghbi HY, Smolyar A, Bosak S, Sequerra R, Doucette-Stamm L, Cusick ME, Hill DE, Roth FP, Vidal M (outubro de 2005). "Rumo a um mapa em escala de proteoma da rede de interação proteína-proteína humana". Nature . 437 (7062): 1173–8. doi : 10.1038 / nature04209 . PMID 16189514 . S2CID 4427026 .
- Barker KT, Foulkes WD, Schwartz CE, Labadie C, Monsell F, Houlston RS, Harper J (julho de 2006). "O alelo E133K de VG5Q está associado a Klippel-Trenaunay e outras síndromes de supercrescimento?" . Journal of Medical Genetics . 43 (7): 613–4. doi : 10.1136 / jmg.2006.040790 . PMC 2564558 . PMID 16443853 .
links externos
- Localização do genoma humano AGGF1 e página de detalhes do gene AGGF1 no navegador do genoma UCSC .