Sulfeto de cobre (I) - Copper(I) sulfide
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Sulfeto de cobre (I)
|
|
| Outros nomes | |
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100.040.751 |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| Cu 2 S | |
| Massa molar | 159,16 g / mol |
| Densidade | 5,6 g / cm 3 |
| Ponto de fusão | 1.130 ° C (2.070 ° F; 1.400 K) |
| Insolúvel | |
| Solubilidade | ligeiramente solúvel em HCl ; solúvel em NH 4 OH ; dissolve-se em KCN ; decompõe-se em HNO 3 , H 2 SO 4 |
| Perigos | |
| Ponto de inflamação | Não inflamável |
| NIOSH (limites de exposição à saúde dos EUA): | |
|
PEL (permitido)
|
TWA 1 mg / m 3 (como Cu) |
|
REL (recomendado)
|
TWA 1 mg / m 3 (como Cu) |
|
IDLH (perigo imediato)
|
TWA 100 mg / m 3 (como Cu) |
| Compostos relacionados | |
|
Outros ânions
|
Óxido de cobre (I) Seleneto de cobre (I) |
|
Outros cátions
|
Sulfeto de níquel (II) Sulfeto de cobre (II) Sulfeto de zinco |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O sulfeto de cobre (I) é um sulfeto de cobre , um composto químico de cobre e enxofre . Possui o composto químico Cu 2 S. É encontrado na natureza como o mineral calcocita . Possui uma faixa estreita de estequiometria variando de Cu 1.997 S a Cu 2.000 S.
Preparação e reações
O Cu 2 S pode ser preparado aquecendo fortemente o cobre em vapor de enxofre ou H 2 S. A reação do pó de cobre no enxofre fundido produz rapidamente Cu 2 S, enquanto os pellets de cobre requerem uma temperatura muito mais alta. Cu 2 S reage com oxigênio para formar SO 2 :
- 2 Cu 2 S + 3 O 2 → 2 Cu 2 O + 2 SO 2
Na produção de cobre, dois terços do sulfeto de cobre fundido são oxidados como acima, e o Cu 2 O reage com o Cu 2 S não oxidado para dar o metal Cu:
- Cu 2 S + 2 Cu 2 O → 6 Cu + SO 2
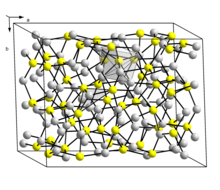
Estrutura
Existem duas formas de Cu 2 S: uma forma monoclínica de baixa temperatura ("calcocita baixa") que possui uma estrutura complexa com 96 átomos de cobre na célula unitária e uma forma hexagonal estável acima de 104 ° C. Nesta estrutura existem 24 átomos de Cu cristalograficamente distintos e a estrutura foi descrita como se aproximando de uma matriz hexagonal compacta de átomos de enxofre com átomos de Cu em coordenação planar 3. Esta estrutura foi inicialmente atribuída a uma célula ortorrômbica devido à geminação do cristal da amostra.
Há também uma fase cristalograficamente distinta (o mineral djurleita ) com estequiometria Cu 1,96 S que é não estequiométrica (intervalo Cu 1,934 S-Cu 1,965 S) e tem uma estrutura monoclínica com 248 átomos de cobre e 128 átomos de enxofre na célula unitária. Cu 2 S e Cu 1,96 S são semelhantes em aparência e difíceis de distinguir um do outro.
Veja também
- Sulfeto de cobre para uma visão geral de todas as fases de sulfeto de cobre
- Monossulfeto de cobre , CuS
- Calcocite
- Djurleite
