Reação de Gattermann - Gattermann reaction
| Formilação Gattermann | |
|---|---|
| Nomeado após | Ludwig Gattermann |
| Tipo de reação | Reação de substituição |
| Identificadores | |
| ID de ontologia RSC | RXNO: 0000139 |
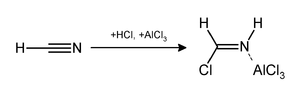
A reação Gattermann (também conhecida como formilação Gattermann e síntese de salicilaldeído Gattermann ) é uma reação química na qual compostos aromáticos são formilados por uma mistura de cianeto de hidrogênio (HCN) e cloreto de hidrogênio (HCl) na presença de um catalisador ácido de Lewis como AlCl 3 . É nomeado para o químico alemão Ludwig Gattermann e é semelhante à reação de Friedel-Crafts .
A reação pode ser simplificada substituindo a combinação HCN / AlCl 3 por cianeto de zinco . Embora também seja altamente tóxico, o Zn (CN) 2 é um sólido, tornando-o mais seguro de se trabalhar do que o HCN gasoso. O Zn (CN) 2 reage com o HCl para formar o reagente HCN chave e o Zn (Cl) 2 que serve como catalisador ácido de Lewis in-situ . Um exemplo do método Zn (CN) 2 é a síntese de mesitaldeído a partir de mesitileno .
Reação Gattermann-Koch
| Formilação Gattermann-Koch | |
|---|---|
| Nomeado após |
Ludwig Gattermann Julius Arnold Koch |
| Tipo de reação | Reação de substituição |
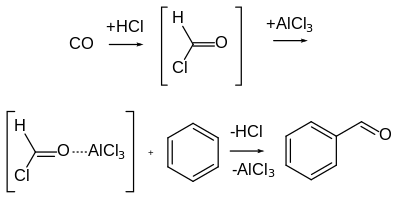
A reação Gattermann-Koch , em homenagem aos químicos alemães Ludwig Gattermann e Julius Arnold Koch , é uma variante da reação Gattermann na qual monóxido de carbono (CO) é usado em vez de cianeto de hidrogênio.
Ao contrário da reação de Gattermann, esta reação não é aplicável a substratos de fenol e éter de fenol . Embora o cloreto de formila altamente instável tenha sido inicialmente postulado como um intermediário, o cátion formila (isto é, monóxido de carbono protonado), [HCO] + , é agora pensado para reagir diretamente com o areno sem a formação inicial de cloreto de formila. Além disso, quando o cloreto de zinco é usado como o ácido de Lewis em vez de cloreto de alumínio, por exemplo, ou quando o monóxido de carbono não é usado em alta pressão, a presença de vestígios de cloreto de cobre (I) ou co-catalisador de cloreto de níquel (II) é frequentemente necessário. O cocatalisador de metal de transição pode servir como um "transportador", primeiro formando a reação com CO para formar um complexo de carbonila, que é então transformado no eletrófilo ativo.