Proteína de ligação de retinol 4 - Retinol binding protein 4
A proteína 4 de ligação ao retinol , também conhecida como RBP4 , é uma proteína transportadora do retinol (álcool de vitamina A). RBP4 tem um peso molecular de aproximadamente 21 kDa e é codificado pelo gene RBP4 em humanos. É principalmente, embora não exclusivamente, sintetizado no fígado e circula na corrente sanguínea ligado ao retinol em um complexo com a transtirretina . RBP4 tem sido um alvo de drogas para pesquisas oftalmológicas devido ao seu papel na visão. O RBP4 também pode estar envolvido em doenças metabólicas, conforme sugerido por estudos recentes.
Função
Essa proteína pertence à família das lipocalinas e é a transportadora específica do retinol (vitamina A) no sangue. Ele distribui retinol das reservas do fígado para os tecidos periféricos. No plasma, o complexo RBP-retinol interage com a transtirretina , o que impede sua perda por filtração através dos glomérulos renais . Uma deficiência de vitamina A bloqueia a secreção da proteína de ligação pós-tradução e resulta em entrega e fornecimento defeituosos às células epidérmicas.
Estrutura
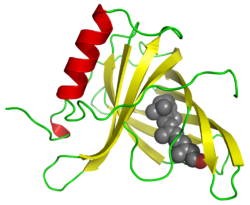
RBP4 é uma única cadeia polipeptídica com uma bolsa hidrofóbica onde o retinol se liga. O complexo RBP4-retinol então se liga à transtirretina na circulação para prevenir a filtração renal de RBP4.
No soro, TTR e RBP4 ligam-se em uma estequiometria de 1 para 1 (duas moléculas de TTR combinam-se com duas moléculas de RBP4 para formar um complexo com um peso molecular total de aproximadamente 80.000 Daltons ).
Significado clínico
A proteína 4 de ligação ao retinol tem sido um alvo de drogas para doenças oculares, pois a RBP4 é o único transportador do retinol, que é um nutriente essencial para o ciclo visual. Estudos em animais usando antagonistas de RBP4 mostraram que a redução de RBP4 pode levar à redução no acúmulo de lipofuscina que leva à perda de visão em doenças oculares como doença de Stargardt e degeneração macular . Um estudo em animais usando camundongos knockout para ABCA4 provou que a redução no nível sérico de RBP4 pode inibir a lipofuscina sem inibir o ciclo visual. [Ref] Um estudo clínico em degeneração macular relacionada à idade (DMRI) foi conduzido usando fenretinida . O estudo mostrou tendências na redução da taxa de crescimento da lesão na DMRI e na taxa de conversão de DMRI em estágio inicial (DMRI seca) para DMRI em estágio tardio (DMRI úmida) sem efeitos colaterais graves.
RBP4 foi recentemente descrito como uma adipocina que contribui para a resistência à insulina e diabetes no modelo de camundongo AG4KO. Além do fígado, a RBP4 também é secretada pelos adipócitos do tecido adiposo em uma porção menor e atua como um sinal para as células vizinhas, quando há diminuição da concentração plasmática de glicose. Suspeita-se que um nível elevado de RBP4 atrai macrófagos para o tecido adiposo, causa inflamação local e leva à resistência à insulina.
Mutações no gene RBP4 foram recentemente associadas a uma forma de microftalmia autossômica dominante, anoftalmia e doença coloboma (MAC). Uma característica única desta doença é o efeito de herança materna, quando um feto herda uma cópia mutada do gene RBP4 de sua mãe, mas não de seu pai. A base fisiológica está na gravidez, em que o produto do gene mutado, a proteína de ligação ao retinol (RBP), tem efeitos negativos na transferência de vitamina A dos locais de armazenamento do fígado materno para a placenta e, novamente, no lado da circulação fetal ao fornecer vitamina A da placenta para o desenvolvimento de tecidos fetais, principalmente o olho em desenvolvimento. Este efeito de 'golpe duplo' não existe quando o gene RBP4 mutante é herdado do pai. O mecanismo acima é separado dos tipos previamente conhecidos de efeitos de herança materna, como impressão genômica, herança mitocondrial ou transferência de mRNA de oócito materno. Os autores do estudo acima citam o potencial da suplementação de vitamina A em mulheres grávidas que são conhecidas por serem portadoras de uma mutação RBP4 com éster retinílico, que utiliza uma via independente de RBP para fornecer retinóides dos intestinos maternos diretamente para a placenta e, finalmente, é absorvida por o feto. A chave seria suplementar durante os primeiros meses de vida, quando o olho começa a se desenvolver, pois a suplementação mais tarde na gravidez seria tarde demais para evitar qualquer doença potencial por MAC.
Veja também
Referências
Leitura adicional
- Quadro L, Hamberger L, Colantuoni V, Gottesman ME, Blaner WS (dezembro de 2003). "Compreendendo o papel fisiológico da proteína de ligação ao retinol no metabolismo da vitamina A usando modelos de camundongos transgênicos e knockout". Aspectos moleculares da medicina . 24 (6): 421–30. doi : 10.1016 / S0098-2997 (03) 00038-4 . PMID 14585313 .
- Newcomer ME, Ong DE (outubro de 2000). "Plasma retinol binding protein: structure and function of the prototypic lipocalin". Biochimica et Biophysica Acta (BBA) - Estrutura de Proteínas e Enzimologia Molecular . 1482 (1–2): 57–64. doi : 10.1016 / s0167-4838 (00) 00150-3 . PMID 11058747 .
- Fex G, Hansson B (fevereiro de 1979). "Proteína de ligação ao retinol da urina humana e sua interação com retinol e pré-albumina". European Journal of Biochemistry . 94 (1): 307–13. doi : 10.1111 / j.1432-1033.1979.tb12896.x . PMID 571335 .
- Rask L, Anundi H, Peterson PA (agosto de 1979). "A estrutura primária da proteína de ligação ao retinol humano" . FEBS Letters . 104 (1): 55–8. doi : 10.1016 / 0014-5793 (79) 81084-4 . PMID 573217 . S2CID 8540537 .
- Fex G, Albertsson PA, Hansson B (setembro de 1979). "Interação entre a pré-albumina e a proteína de ligação ao retinol estudada por cromatografia de afinidade, filtração em gel e partição bifásica" . European Journal of Biochemistry . 99 (2): 353–60. doi : 10.1111 / j.1432-1033.1979.tb13263.x . PMID 574085 .
- Monaco HL, Zanotti G (abril de 1992). "Estrutura tridimensional e sítio ativo de três proteínas de ligação a moléculas hidrofóbicas com similaridade de sequência de aminoácidos significativa". Biopolímeros . 32 (4): 457–65. doi : 10.1002 / bip.360320425 . PMID 1623143 . S2CID 34994569 .
- Cowan SW, Newcomer ME, Jones TA (1990). "Refinamento cristalográfico da proteína de ligação ao retinol de soro humano na resolução 2A". Proteínas . 8 (1): 44–61. doi : 10.1002 / prot.340080108 . PMID 2217163 . S2CID 21613341 .
- D'Onofrio C, Colantuoni V, Cortese R (agosto de 1985). "Estrutura e expressão específica da célula de um gene da proteína de ligação ao retinol humano clonado: a região flanqueadora 5 'contém sinais de transcrição específicos do hepatoma" . The EMBO Journal . 4 (8): 1981–9. doi : 10.1002 / j.1460-2075.1985.tb03881.x . PMC 554451 . PMID 2998779 .
- Pfeffer BA, Clark VM, Flannery JG, Bok D (julho de 1986). "Receptores de membrana para proteína de ligação de retinol em cultura de epitélio pigmentar da retina humana". Oftalmologia Investigativa e Ciências Visuais . 27 (7): 1031–40. PMID 3013795 .
- Kameko M, Ichikawa M, Katsuyama T, Kanai M, Kato M, Akamatsu T (abril de 1986). "Immunohistochemical localization of plasma retinol-binding protein and prealbumin in human pancreático ilhéus". The Histochemical Journal . 18 (4): 164-8. doi : 10.1007 / BF01676116 . PMID 3525470 . S2CID 2959823 .
- Siegenthaler G, Saurat JH (abril de 1987). "Perda de propriedades de ligação ao retinol para a proteína plasmática de ligação ao retinol na epiderme humana normal" . The Journal of Investigative Dermatology . 88 (4): 403–8. doi : 10.1111 / 1523-1747.ep12469731 . PMID 3559267 .
- Rask L, Vahlquist A, Peterson PA (novembro de 1971). "Estudos sobre duas formas fisiológicas da proteína de ligação ao retinol humano diferindo no teor de vitamina A e arginina". The Journal of Biological Chemistry . 246 (21): 6638–46. PMID 5132677 .
- Colantuoni V, Romano V, Bensi G, Santoro C, Costanzo F, Raugei G, Cortese R (novembro de 1983). "Clonagem e sequenciação de uma codificação de cDNA de comprimento total para a proteína de ligação ao retinol humano" . Nucleic Acids Research . 11 (22): 7769–76. doi : 10.1093 / nar / 11.22.7769 . PMC 326530 . PMID 6316270 .
- Recém-chegado ME, Jones TA, Aqvist J, Sundelin J, Eriksson U, Rask L, Peterson PA (julho de 1984). "A estrutura tridimensional da proteína de ligação ao retinol" . The EMBO Journal . 3 (7): 1451–4. doi : 10.1002 / j.1460-2075.1984.tb01995.x . PMC 557543 . PMID 6540172 .
- Rask L, Anundi H, Böhme J, Eriksson U, Ronne H, Sege K, Peterson PA (fevereiro de 1981). "Estudos estruturais e funcionais das proteínas de ligação da vitamina A". Anais da Academia de Ciências de Nova York . 359 : 79–90. doi : 10.1111 / j.1749-6632.1981.tb12739.x . PMID 6942701 . S2CID 5781208 .
- Jaconi S, Rose K., Hughes GJ, Saurat JH, Siegenthaler G (junho de 1995). "Caracterização de duas formas pós-traducionais processadas de proteína de ligação ao retinol de soro humano: proporções alteradas na insuficiência renal crônica". Journal of Lipid Research . 36 (6): 1247–53. PMID 7666002 .
- Berni R, Malpeli G, Folli C, Murrell JR, Liepnieks JJ, Benson MD (setembro de 1994). “A substituição do aminoácido Ile-84 -> Ser na transtirretina interfere na interação com a proteína plasmática de ligação ao retinol”. The Journal of Biological Chemistry . 269 (38): 23395–8. PMID 8089102 .
- Seeliger MW, Biesalski HK, Wissinger B, Gollnick H, Gielen S, Frank J, Beck S, Zrenner E (janeiro de 1999). "Fenótipo na deficiência de retinol devido a um defeito hereditário na síntese de proteínas de ligação ao retinol". Oftalmologia Investigativa e Ciências Visuais . 40 (1): 3–11. PMID 9888420 .
links externos
- RBP4 + proteína + humano na Biblioteca Nacional de Medicina dos EUA Medical Subject Headings (MeSH)
- Visão geral de todas as informações estruturais disponíveis no PDB para UniProt : P02753 (proteína 4 de ligação ao retinol) no PDBe-KB .