Proteína secretase do precursor beta-amilóide - Amyloid-beta precursor protein secretase
Secretases são enzimas que "cortam" pedaços de uma proteína mais longa que está embutida na membrana celular .
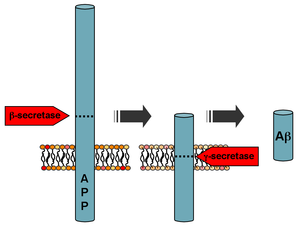
Entre outras funções na célula , as secretases atuam na proteína precursora de beta-amilóide (APP) para clivar a proteína em três fragmentos. A clivagem sequencial pela beta-secretase 1 (BACE) e gama-secretase (γ-secretase) produz o fragmento do peptídeo beta-amilóide que se agrega em aglomerados chamados placas amilóides nos cérebros afetados pela doença de Alzheimer . Se a alfa-secretase (α-secretase) atua primeiro em APP em vez de BACE, nenhuma beta amilóide é formada porque a α-secretase reconhece uma sequência de proteína alvo mais próxima da superfície celular do que BACE. O fragmento do meio não patogênico formado por uma sequência de clivagem α / γ é denominado P3.
Estrutura
A estrutura das três secretases varia amplamente.
- O gene da α-secretase não foi identificado de forma conclusiva, mas acredita-se que seja uma metaloproteinase .
- BACE é uma proteína transmembrana com um domínio de protease de ácido aspártico extracelular .
- A γ-secretase é, na verdade, um complexo proteico contendo presenilina , nicastrina , APH-1 e PEN-2 . Acredita-se que a presenilina abrigue o domínio da protease e representa um exemplo importante de um tipo incomum de protease que cliva os alvos dentro da membrana celular.
Função
Além de seu envolvimento na patogênese do Alzheimer, essas proteínas também desempenham outros papéis funcionais na célula.
A γ-secretase desempenha um papel crítico na sinalização do desenvolvimento pelo receptor transmembrana Notch , liberando a cauda citoplasmática de Notch para viajar para o núcleo da célula para atuar como um fator de transcrição .
Embora BACE cliva os domínios extracelulares de várias proteínas transmembrana, sua função fisiológica permanece desconhecida.
Referências
links externos
- Secretase nos títulos de assuntos médicos da Biblioteca Nacional de Medicina dos EUA (MeSH)