Carga de superfície - Surface charge
A carga superficial é uma superfície bidimensional com carga elétrica diferente de zero . Essas cargas elétricas são restringidas nesta superfície 2-D e a densidade de carga da superfície , medida em coulombs por metro quadrado (C • m −2 ), é usada para descrever a distribuição de carga na superfície. O potencial elétrico é contínuo através de uma carga superficial e o campo elétrico é descontínuo, mas não infinito; isto é, a menos que a carga superficial consista em uma camada dipolo. Em comparação, o potencial e o campo elétrico divergem em qualquer carga pontual ou carga linear.
Em física, em equilíbrio, um condutor ideal não tem carga em seu interior; em vez disso, a totalidade da carga do condutor reside na superfície. No entanto, isso só se aplica ao caso ideal de condutividade elétrica infinita ; A maior parte da carga de um condutor real reside na profundidade da pele da superfície do condutor. Para materiais dielétricos , mediante a aplicação de um campo elétrico externo, as cargas positivas e negativas no material irão se mover ligeiramente em direções opostas, resultando em densidade de polarização no corpo a granel e carga ligada na superfície.
Em química, existem muitos processos diferentes que podem levar a uma superfície sendo carregada, incluindo adsorção de íons, protonação / desprotonação e, como discutido acima, a aplicação de um campo elétrico externo. A carga superficial emite um campo elétrico, que causa repulsão e atração das partículas, afetando muitas propriedades coloidais .
A carga superficial quase sempre aparece na superfície da partícula quando ela é colocada em um fluido . A maioria dos fluidos contém íons , positivos ( cátions ) e negativos ( ânions ). Esses íons interagem com a superfície do objeto. Essa interação pode levar à adsorção de alguns deles na superfície. Se o número de cátions adsorvidos exceder o número de ânions adsorvidos, a superfície terá uma carga elétrica positiva líquida .
A dissociação do grupo químico de superfície é outro mecanismo possível que leva à carga de superfície.
Densidade
A densidade de carga superficial é definida como a quantidade de carga elétrica , q, que está presente em uma superfície de determinada área, A:
Condutores
De acordo com a lei de Gauss , um condutor em equilíbrio carregando uma corrente aplicada não tem carga em seu interior. Em vez disso, a totalidade da carga do condutor reside na superfície e pode ser expressa pela equação:
onde E é o campo elétrico causado pela carga no condutor e é a permissividade do espaço livre. Esta equação é estritamente precisa apenas para condutores com área infinitamente grande, mas fornece uma boa aproximação se E for medido a uma distância euclidiana infinitesimalmente pequena da superfície do condutor.
Coloides e objetos imersos
| Composto | Fórmula química | Ponto de Carga Zero |
|---|---|---|
| óxido de tungstênio (VI) | WO 3 | 0,2–0,5 |
| carboneto de silício (alfa) | SiC | 2-3,5 |
| óxido de manganês (IV) | MnO 2 | 4-5 |
| nitreto de silício | Si 3 N 4 | 6-7 |
| óxido de tálio (I) | Tl 2 O | 8 |
| óxido de cobre (II) | CuO | 9,5 |
| óxido de níquel (II) | NiO | 10-11 |
Quando uma superfície é imersa em uma solução contendo eletrólitos , ela desenvolve uma carga superficial líquida. Isso geralmente ocorre por causa da adsorção iônica. Soluções aquosas universalmente contêm íons positivos e negativos ( cátions e ânions , respectivamente), que interagem com cargas parciais na superfície, adsorvendo e ionizando a superfície e criando uma carga superficial líquida. Essa carga líquida resulta em um potencial de superfície [L], que faz com que a superfície seja cercada por uma nuvem de contra-íons, que se estende da superfície para a solução, e também geralmente resulta em repulsão entre as partículas. Quanto maiores as cargas parciais no material, mais íons são adsorvidos à superfície e maior é a nuvem de contraíons. Uma solução com uma concentração mais alta de eletrólitos também aumenta o tamanho da nuvem de contra-íons. Essa camada íon / contra-íon é conhecida como camada dupla elétrica .
O pH de uma solução também pode afetar muito a carga superficial porque os grupos funcionais presentes na superfície das partículas podem freqüentemente conter oxigênio ou nitrogênio, dois átomos que podem ser protonados ou desprotonados para se tornarem carregados. Assim, à medida que a concentração de íons de hidrogênio muda, o mesmo ocorre com a carga superficial das partículas. Em um certo pH, a carga superficial média será igual a zero; isso é conhecido como o ponto de carga zero (PZC). Uma lista de substâncias comuns e seus PZCs associados é mostrada à direita.
Potencial interfacial
Uma interface é definida como o limite comum formado entre duas fases diferentes, como entre um sólido e um gás. Potencial elétrico , ou carga, é o resultado da capacidade de um objeto se mover em um campo elétrico. Um potencial interfacial é, portanto, definido como uma carga localizada no limite comum entre duas fases (por exemplo, um aminoácido como o glutamato na superfície de uma proteína pode ter seu ácido carboxílico de cadeia lateral desprotonado em ambientes com pH superior a 4,1 para produzir um aminoácido carregado na superfície, o que criaria um potencial interfacial). O potencial interfacial é responsável pela formação da dupla camada elétrica, que possui uma ampla gama de aplicações nos denominados fenômenos eletrocinéticos . O desenvolvimento da teoria da dupla camada elétrica é descrito a seguir.
Helmholtz
O modelo apelidado de 'camada dupla elétrica' foi apresentado pela primeira vez por Hermann von Helmholtz . Ele assume que uma solução é composta apenas de eletrólitos, nenhuma reação ocorre perto do eletrodo que poderia transferir elétrons, e que as únicas interações de Van der Waals estão presentes entre os íons em solução e o eletrodo. Essas interações surgem apenas devido à densidade de carga associada ao eletrodo, que surge de um excesso ou deficiência de elétrons na superfície do eletrodo. Para manter a neutralidade elétrica, a carga do eletrodo será equilibrada por uma redistribuição de íons perto de sua superfície. Os íons atraídos formam, portanto, uma camada que equilibra a carga do eletrodo. A distância mais próxima que um íon pode chegar ao eletrodo será limitada ao raio do íon mais uma única esfera de solvatação em torno de um íon individual. No geral, duas camadas de carga e uma queda de potencial do eletrodo para a borda da camada externa (plano de Helmholtz externo) são observadas. Dada a descrição acima, o modelo de Helmholtz é equivalente em natureza a um capacitor elétrico com duas placas de carga separadas, para o qual uma queda de potencial linear é observada à medida que aumenta a distância das placas.
O modelo de Helmholtz, embora seja uma boa base para a descrição da interface, não leva em conta vários fatores importantes: difusão / mistura em solução, a possibilidade de adsorção na superfície e a interação entre os momentos dipolares do solvente e o eletrodo.
Gouy-Chapman
A teoria de Gouy-Chapman descreve o efeito de uma carga de superfície estática no potencial de uma superfície. " Gouy sugeriu que o potencial interfacial na superfície carregada poderia ser atribuído à presença de um número de íons de determinada carga ligados à sua superfície, e a um número igual de íons de carga oposta na solução." Uma carga superficial positiva formará uma camada dupla, uma vez que íons negativos em solução tendem a equilibrar a carga superficial positiva. Os contra-íons não são retidos rigidamente, mas tendem a se difundir na fase líquida até que o contra-potencial criado por sua partida restrinja essa tendência. A energia cinética dos contra-íons afetará, em parte, a espessura da camada dupla difusa resultante. A relação entre C, a concentração de contra-íons na superfície e a concentração de contra-íons na solução externa é o fator de Boltzmann:
Onde z é a carga do íon, e é a carga de um próton, k é a constante de Boltzmann e ψ é o potencial da superfície carregada.
Isso, entretanto, é impreciso próximo à superfície, porque assume que a concentração molar é igual à atividade. Ele também assume que os íons foram modelados como cargas pontuais e posteriormente modificados. Um aprimoramento dessa teoria, conhecido como teoria modificada de Gouy-Chapman, incluiu o tamanho finito dos íons em relação à sua interação com a superfície na forma de um plano de abordagem mais próxima.
Potencial de superfície
A relação entre carga superficial e potencial superficial pode ser expressa pela equação de Grahame, derivada da teoria de Gouy-Chapman, assumindo a condição de eletroneutralidade, que afirma que a carga total da camada dupla deve ser igual ao negativo da carga superficial. Usando a equação de Poisson unidimensional e assumindo que, a uma distância infinitamente grande, o gradiente de potencial é igual a 0, a equação de Grahame é obtida:
Para o caso de potenciais mais baixos, pode ser expandido para = , e é definido como o comprimento de Debye . O que leva à expressão simples:
popa
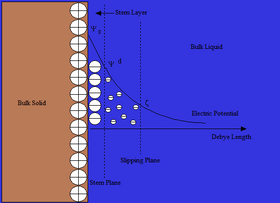
O modelo de Otto Stern da camada dupla é essencialmente uma combinação das teorias de Helmholtz e Gouy-Chapman. Sua teoria afirma que os íons têm tamanho finito, portanto, não podem se aproximar da superfície além de alguns nanômetros. Através de uma distância conhecida como Camada Stern, os íons podem ser adsorvidos na superfície até um ponto referido como o plano de deslizamento, onde os íons adsorvidos encontram o líquido a granel. No plano deslizante, o potencial Ψ diminuiu para o que é conhecido como potencial zeta . Embora o potencial zeta seja um valor intermediário, às vezes é considerado mais significativo do que o potencial de superfície no que diz respeito à repulsão eletrostática.
Formulários
As superfícies carregadas são extremamente importantes e são usadas em muitas aplicações. Por exemplo, soluções de grandes partículas coloidais dependem quase inteiramente da repulsão devido à carga superficial para permanecerem dispersas. Se essas forças repulsivas fossem interrompidas, talvez pela adição de um sal ou polímero, as partículas coloidais não seriam mais capazes de sustentar a suspensão e, subsequentemente, floculariam .
Fenômenos eletrocinéticos
Os fenômenos eletrocinéticos referem-se a uma variedade de efeitos resultantes de uma dupla camada elétrica . Um exemplo notável é a eletroforese , em que uma partícula carregada suspensa em um meio se move como resultado de um campo elétrico aplicado. A eletroforese é amplamente utilizada em bioquímica para distinguir moléculas, como proteínas, com base no tamanho e na carga. Outros exemplos incluem eletro-osmose , potencial de sedimentação e potencial de fluxo .
Proteínas
As proteínas frequentemente têm grupos presentes em suas superfícies que podem ser ionizados ou desionizados dependendo do pH, tornando relativamente fácil alterar a carga superficial de uma proteína. Isso tem ramificações particularmente importantes na atividade de proteínas que funcionam como enzimas ou canais de membrana, principalmente, que o sítio ativo da proteína deve ter a carga superficial certa para ser capaz de se ligar a um substrato específico.
Adesivos / revestimentos
As superfícies carregadas são frequentemente úteis na criação de superfícies que não irão adsorver certas moléculas (por exemplo, para evitar a adsorção de proteínas básicas, uma superfície carregada positivamente deve ser usada). Os polímeros são muito úteis a este respeito porque podem ser funcionalizados de modo a conterem grupos ionizáveis, que servem para fornecer uma carga superficial quando submersos numa solução aquosa.
Referências
- ^ "Polarização dielétrica, cargas limitadas e o campo de deslocamento elétrico" (PDF) .
- ^ a b c d e f g Hans-Jurgen, Butt; Graf, Karlheinz; Kappl, Michael (2006). Física e química de interfaces . Alemanha: Wiley-VCH. pp. 45, 55, 56, 76-82. ISBN 978-3-527-40629-6 .
-
^ Weisstein,
Ausente ou vazio
|title=( ajuda ) - ^ Nave, Carl R. (2010). "Superfícies gaussianas" . Georgia State University . Página visitada em 27 de abril de 2011 .
- ^ a b Kosmulski, Marek (2001), propriedades químicas das superfícies materiais, Marcel Dekker
- ^ a b c Lewis, JA (2000). "Processamento coloidal de cerâmica". Jornal da American Ceramic Society . 83 (10): 2341–2359. CiteSeerX 10.1.1.514.1543 . doi : 10.1111 / j.1151-2916.2000.tb01560.x .
- ^ Jolivet JP (2000), Metal óxido química e síntese. Da solução ao estado sólido , John Wiley & Sons Ltd., ISBN 0-471-97056-5 (Tradução para o inglês do texto original em francês, De la solution à l'oxyde InterEditions et CNRS Editions, Paris, 1994)
- ^ Kosmulski, M; Saneluta, C (2004). “Ponto de carga zero / ponto isoelétrico de óxidos exóticos: Tl2O3”. Journal of Colloid and Interface Science . 280 (2): 544–545. Bibcode : 2004JCIS..280..544K . doi : 10.1016 / j.jcis.2004.08.079 . PMID 15533430 .
- ^ "Origens da carga superficial" . Silver Colloids. 2010 . Página visitada em 27 de abril de 2011 .
- ^ "A dupla camada elétrica" . Silver Colloids. 2010 . Página visitada em 27 de abril de 2011 .
- ^ "A dupla camada elétrica" . 2011. Arquivado do original em 31 de maio de 2011 . Página visitada em 27 de abril de 2011 .
- ^ Ehrenstein, Gerald (200). "Carga superficial" (PDF) . Arquivado do original (PDF) em 28 de setembro de 2011 . Página visitada em 30 de maio de 2011 .
- ^ Smirnov, Gerald (2011). "Bicamada dupla" . Página visitada em 30 de maio de 2011 .
- ^ Greathouse, Jeffery A .; Feller, Scott E .; McQuarrie, Donald A. (1994). "A teoria modificada de Gouy-Chapman: Comparações entre modelos elétricos de camada dupla de intumescimento de argila". Langmuir . 10 (7): 2125. doi : 10.1021 / la00019a018 .
- ^ "Medição do potencial Zeta" . Brookhaven Instruments Ltd. 2007. Arquivo do original em 19 de julho de 2003 . Retirado em 16 de abril de 2011 .
- ^ Hubbe, Martin (2007). “Floculação de colóides ou de pastas de fibras” . Universidade Estadual da Carolina do Norte . Retirado em 16 de abril de 2011 .
- ^ "Capítulo 4: Eletroforese - Introdução" . Dr. William H. Heidcamp, Departamento de Biologia, Gustavus Adolphus College. 1995 . Página visitada em 30 de maio de 2011 .
- ^ Escobar, Laura; Root, Michael J .; MacKinnon, Robert (julho de 1993). "Influência da carga da superfície da proteína na cinética bimolecular de um inibidor de peptídeo do canal de potássio". Bioquímica . 32 (27): 6982–6987. doi : 10.1021 / bi00078a024 . PMID 7687466 .
- ^ Haselberg, Rob; van der Sneppen, Lineke; Ariese, Freek; Ubachs, Wim; Gooijer, Cees; de Jong, Gerhardus J .; Somsen, Govert W. (18 de novembro de 2009). "Eficácia de revestimentos de polímeros não covalentes carregados contra a adsorção de proteínas a superfícies de sílica estudada por espectroscopia de anel de cavidade evanescente e eletroforese capilar". Química Analítica . 81 (24): 10172–10178. doi : 10.1021 / ac902128n . PMID 19921852 .














