Cloreto de bis (trifenilfosfina) paládio - Bis(triphenylphosphine)palladium chloride
|
|
|
|

|
|
| Identificadores | |
|---|---|
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.034.299 |
|
PubChem CID
|
|
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 36 H 30 Cl 2 P 2 Pd | |
| Massa molar | 701,90 g · mol −1 |
| Aparência | pó amarelo |
| Ponto de fusão | 260 ° C (decomposto em torno de 300 ° C) |
| Insolúvel em água, acetona, éter, tetracloreto de carbono e n-heptano // Solúvel em CHCl 3 e CH 2 Cl 2 , clorofórmio (ligeiramente), metanol (ligeiramente, aquecido) | |
| Perigos | |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | 181,7 ° C |
| Compostos relacionados | |
|
Compostos relacionados
|
Cloreto de bis (trifenilfosfina) platina |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
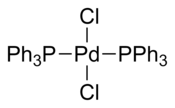
Cloreto de bis (trifenilfosfina) paládio é um composto de coordenação de paládio contendo duas trifenilfosfinas e dois ligantes de cloreto . É um sólido amarelo solúvel em alguns solventes orgânicos. É usado para reações de acoplamento catalisadas por paládio , por exemplo, a reação Sonogashira – Hagihara . O complexo é quadrado plano . Muitos complexos análogos são conhecidos com diferentes ligantes de fosfina.
Preparação e reações
Este composto pode ser preparado tratando cloreto de paládio (II) com trifenilfosfina :
- PdCl 2 + 2 PPh 3 → PdCl 2 (PPh 3 ) 2
Após a redução com hidrazina na presença de excesso de trifenilfosfina, o complexo é um precursor de tetraquis (trifenilfosfina) paládio , Pd (PPh 3 ) 4 :
- 2 PdCl 2 (PPh 3 ) 2 + 4 PPh 3 + 5 N 2 H 4 → 2 Pd (PPh 3 ) 4 + N 2 + 4 N 2 H 5 + Cl -
Estrutura
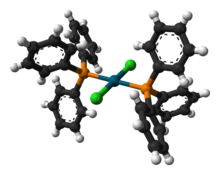
Várias estruturas cristalinas contendo PdCl 2 (PPh 3 ) 2 foram relatadas. Em todas as estruturas, o PdCl 2 (PPh 3 ) 2 adota uma geometria de coordenação plana quadrada e a forma isomérica trans .
Formulários
O complexo é usado como um pré-catalisador para uma variedade de reações de acoplamento.
A reação de Suzuki já foi limitada por altos níveis de catalisador e pela disponibilidade limitada de ácidos borônicos. Substituições para haletos também foram encontradas, aumentando o número de parceiros de acoplamento para haletos ou pseudo-haletos. Usando cloreto de bis (trifenilfosfina) paládio como catalisador, triflatos e ácidos borônicos foram acoplados em uma escala de 80 quilogramas com bom rendimento. O mesmo catalisador é eficaz para o acoplamento Sonogashira .
Veja também
Referências
- ^ Norio Miyaura e Akira Suzuki (1990). "Palladium-Catalyzed Reaction of 1-Alkenylboronates with Vinylic Halides: (1Z, 3E) -1-Phenyl-1,3-octadiene". Sínteses orgânicas . 68 : 130. doi : 10.15227 / orgsyn.068.0130 . CS1 maint: usa o parâmetro de autores ( link )
- ^ Hiroshi Itatani, JCBailar (1967). "Homogeneous Catalysis in the Reactions of olefinic Substances. V.Hydrogenation of Soybean Oil Methyl ester with trifhenylphosphine and trifhenylarsine Palladium Catalysts". Jornal da American Oil Chemists 'Society . 44 : 147. doi : 10.1007 / BF02558176 . CS1 maint: usa o parâmetro de autores ( link )
- ^ DR Coulson (1972). Tetraquis (trifenilfosfina) paládio (0) . Inorg. Synth. Sínteses inorgânicas. 13 . pp. 121–124. doi : 10.1002 / 9780470132449.ch23 . ISBN 9780470132449 .
- ^ G. Ferguson, R. McCrindle, AJ McAlees e M. Parvez (1982). " trans- Diclorobis (trifenilfosfina) paládio (II)" . Acta Crystallogr . B38 (10): 2679–2681. doi : 10.1107 / S0567740882009583 . CS1 maint: usa o parâmetro de autores ( link )
- ^ G. Steyl (2006). " Solvato de diclorometano trans- Diclorobis (trifenilfosfina) paládio (II)". Acta Crystallogr. E . 62 : m1324 – m1325. doi : 10.1107 / S1600536806017521 .
- ^ J. Pons, J. García-Antón, X. Solans, M. Font-Bardia, J. Ros (2008). " trans- Dicloridobis (trifenilfosfina) paládio (II)" . Acta Crystallogr. E . 64 : m621. doi : 10.1107 / S1600536808008337 . CS1 maint: usa o parâmetro de autores ( link )
- ^ A. Naghipour, A. Ghorbani-Choghamarani, H. Babaee, M. Hashemi, B. Notash (2017). "Estrutura cristalina de um novo polimorfo de trans- diclorobis (trifenilfosfina) paládio (II) e sua aplicação como um novo, eficiente e recuperável catalisador para a aminação de haletos de arila e reações de acoplamento cruzado de estiletes". J. Organomet. Chem. 841 : 31–38. doi : 10.1016 / j.jorganchem.2016.10.002 . CS1 maint: usa o parâmetro de autores ( link )
- ^ René Severin, Jessica Reimer, Sven Doye (2010). "One-Pot Procedure for the Synthesis of Unsymmetrical Diarylalkynes". J. Org. Chem . 75 (10): 3518–352. doi : 10.1021 / jo100460v . PMID 20420397 . CS1 maint: usa o parâmetro de autores ( link )
- ^ Jacks, TE; Belmont, Daniel T .; Briggs, Christopher A .; Horne, Nicole M .; Kanter, Gerald D .; Karrick, Greg L .; Krikke, James J .; McCabe, Richard J .; Mustakis; Nanninga, Thomas N. (2004). "Desenvolvimento de um processo escalonável para CI-1034, um antagonista de endotelina". Pesquisa e Desenvolvimento de Processos Orgânicos . 8 (2): 201–212. doi : 10.1021 / op034104g . CS1 maint: usa o parâmetro de autores ( link )
- ^ Chinchila, R .; Nájera, C. (2007). "A reação de Sonogashira: uma metodologia em expansão em química orgânica sintética". Chem. Rev . 107 (3): 874–922. doi : 10.1021 / cr050992x . PMID 17305399 . CS1 maint: usa o parâmetro de autores ( link )


