Dióxido de bromo - Bromine dioxide
|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Dióxido de bromo
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
|
PubChem CID
|
|
|
|
|
|
| Propriedades | |
| BrO 2 | |
| Massa molar | 111,903 g / mol |
| Aparência | cristais amarelos instáveis |
| Ponto de fusão | decompõe-se em torno de 0 ° C
|
| Compostos relacionados | |
|
Outros ânions
|
Monóxido de bromo Trifluoreto de bromo Pentafluoreto de bromo |
|
Outros cátions
|
Difluoreto de oxigênio Monóxido de dicloro Dióxido de cloro Dióxido de iodo |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
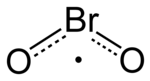
O dióxido de bromo é o composto químico composto de bromo e oxigênio com a fórmula BrO 2 . Forma cristais instáveis de amarelo a amarelo-laranja. Foi isolado pela primeira vez por R. Schwarz e M. Schmeißer em 1937 e acredita-se que seja importante na reação atmosférica do bromo com o ozônio . É semelhante ao dióxido de cloro , o dióxido de seu vizinho halogênio um período acima na tabela periódica .
Reações
O dióxido de bromo é formado quando uma corrente elétrica passa por uma mistura de gases bromo e oxigênio a baixa temperatura e pressão.
O dióxido de bromo também pode ser formado pelo tratamento do gás bromo com ozônio em triclorofluorometano a −50 ° C.
Quando misturado com uma base , o dióxido de bromo dá os ânions brometo e bromato :
Referências
| Este artigo relacionado a compostos inorgânicos é um esboço . Você pode ajudar a Wikipedia expandindo-a . |
