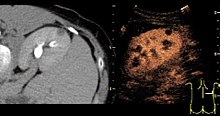
Ultra-som com contraste - Contrast-enhanced ultrasound
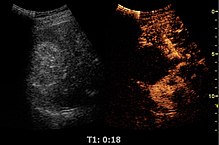
O ultrassom com contraste aprimorado ( CEUS ) é a aplicação do meio de contraste de ultrassom à ultrassonografia médica tradicional . Os agentes de contraste de ultrassom dependem das diferentes maneiras pelas quais as ondas sonoras são refletidas nas interfaces entre as substâncias. Pode ser a superfície de uma pequena bolha de ar ou uma estrutura mais complexa. Os meios de contraste disponíveis comercialmente são microbolhas cheias de gás que são administradas por via intravenosa na circulação sistêmica . As microbolhas têm um alto grau de ecogenicidade (a capacidade de um objeto de refletir ondas de ultrassom). Há uma grande diferença na ecogenicidade entre o gás nas microbolhas e os tecidos moles circundantes do corpo. Assim, a imagem ultrassônica usando agentes de contraste de microbolhas aumenta o retroespalhamento do ultrassom , (reflexão) das ondas de ultrassom, para produzir um ultrassom com contraste aumentado devido à alta diferença de ecogenicidade. O ultrassom com contraste pode ser usado para obter imagens da perfusão sanguínea em órgãos, medir a taxa de fluxo sanguíneo no coração e em outros órgãos e para outras aplicações.
Os ligantes de direcionamento que se ligam a receptores característicos de doenças intravasculares podem ser conjugados a microbolhas , permitindo que o complexo de microbolhas se acumule seletivamente em áreas de interesse, como tecidos doentes ou anormais. Essa forma de imagem molecular, conhecida como ultrassom com contraste direcionado, só gerará um sinal de ultrassom forte se as microbolhas direcionadas se ligarem na área de interesse. O ultrassom com contraste direcionado pode ter muitas aplicações em diagnósticos médicos e terapêuticas médicas. No entanto, a técnica direcionada ainda não foi aprovada pelo FDA para uso clínico nos Estados Unidos.
A ultrassonografia com contraste é considerada segura em adultos, comparável à segurança dos agentes de contraste de ressonância magnética e melhor do que os agentes de radiocontraste usados em exames de TC de contraste . Os dados de segurança mais limitados em crianças sugerem que tal uso é tão seguro quanto na população adulta.
Ecocardiograma de bolha
Um ecocardiograma é um estudo do coração por meio de ultrassom. Um ecocardiograma com bolhas é uma extensão deste que usa bolhas de ar simples como meio de contraste durante este estudo e muitas vezes deve ser solicitado especificamente.
Embora o Doppler colorido possa ser usado para detectar fluxos anormais entre as câmaras do coração (por exemplo, forame oval persistente (patente) ), ele tem uma sensibilidade limitada . Ao procurar especificamente por um defeito como este, pequenas bolhas de ar podem ser usadas como meio de contraste e injetadas por via intravenosa, onde viajam para o lado direito do coração. O teste seria positivo para uma comunicação anormal se as bolhas fossem vistas passando para o lado esquerdo do coração. (Normalmente, eles sairiam do coração através da artéria pulmonar e seriam interrompidos pelos pulmões.) Esta forma de meio de contraste de bolha é gerada em uma base ad hoc pelo médico de teste agitando solução salina normal (por exemplo, pela transferência rápida e repetida do solução salina entre duas seringas conectadas) imediatamente antes da injeção.
Agentes de contraste de microbolhas
Características gerais
Existem vários agentes de contraste de microbolhas. As microbolhas diferem em sua composição de concha, composição de núcleo de gás e se são ou não o alvo.
- Concha da microbolha : a seleção do material da concha determina a facilidade com que a microbolha é absorvida pelo sistema imunológico . Um material mais hidrofílico tende a ser absorvido mais facilmente, o que reduz o tempo de residência da microbolha na circulação. Isso reduz o tempo disponível para imagens de contraste. O material da casca também afeta a elasticidade mecânica das microbolhas. Quanto mais elástico o material, mais energia acústica ele pode suportar antes de estourar. Atualmente, as conchas das microbolhas são compostas de albumina , galactose , lipídio ou polímeros .
- Núcleo de gás de microbolhas : O núcleo de gás é a parte mais importante da microbolha de contraste de ultrassom porque determina a ecogenicidade. Quando bolhas de gás são capturadas em um campo de frequência ultrassônica , elas se comprimem , oscilam e refletem um eco característico - isso gera um ultrassom forte e único em ultrassom com contraste aprimorado. Os núcleos de gás podem ser compostos de ar ou gases pesados como perfluorocarbono ou nitrogênio . Gases pesados são menos solúveis em água, portanto, são menos propensos a vazar da microbolha, levando à dissolução da microbolha. Como resultado, microbolhas com núcleos de gás pesado duram mais tempo em circulação.
Independentemente da composição do invólucro ou do núcleo do gás, o tamanho da microbolha é bastante uniforme. Eles estão dentro de uma faixa de 1–4 micrômetros de diâmetro. Isso os torna menores do que os glóbulos vermelhos , o que permite que eles fluam facilmente através da circulação, bem como da microcirculação.
Agentes específicos
- Hexafluoreto de enxofre microbolhas ( SonoVue Bracco (empresa) ). É usado principalmente para caracterizar lesões hepáticas que não podem ser devidamente identificadas com ultrassom convencional (modo b). Ele permanece visível no sangue por 3 a 8 minutos e expira pelos pulmões.
- Núcleo de gás octafluoropropano com um invólucro de albumina ( microbolhas aprovadas pela GE Healthcare , Optison , Food and Drug Administration (FDA) ).
- Ar dentro de uma camada de lipídio / galactose (Levovist, uma microbolha aprovada pelo FDA feita pela Schering ).
- As microesferas perflexane lipídicas (nome comercial Imagent ou anteriormente Imavist) é uma suspensão injetável desenvolvida pela Alliance Pharmaceutical aprovada pelo FDA (em junho de 2002) para melhorar a visualização da câmara ventricular esquerda do coração, o delineamento das bordas endocárdicas em pacientes com subótima ecocardiogramas. Além de ser usado para avaliar a função cardíaca e a perfusão, também é usado como um intensificador de imagens da próstata, fígado, rim e outros órgãos.
- As microesferas lipídicas de perflutreno (nomes comerciais Definity, Luminity) são compostas de octafluoropropano encapsulado em um invólucro lipídico externo .
Microbolhas direcionadas
Microbolhas direcionadas estão em desenvolvimento pré-clínico. Eles mantêm as mesmas características gerais das microbolhas não direcionadas, mas são equipados com ligantes que se ligam a receptores específicos expressos por tipos de células de interesse, como células inflamadas ou células cancerosas. As microbolhas atuais em desenvolvimento são compostas por um invólucro de monocamada lipídica com um núcleo de gás perfluorocarbono. A casca lipídica também é coberta com uma camada de polietilenoglicol (PEG). O PEG evita a agregação de microbolhas e torna as microbolhas mais não reativas. Ele temporariamente “esconde” a microbolha da absorção do sistema imunológico, aumentando a quantidade de tempo de circulação e, portanto, o tempo de imagem. Além da camada de PEG, a casca é modificada com moléculas que permitem a fixação de ligantes que se ligam a certos receptores . Esses ligantes são ligados às microbolhas usando carbodiimida , maleimida ou acoplamento biotina-estreptavidina. Biotina-estreptavidina é a estratégia de acoplamento mais popular porque a afinidade da biotina pela estreptavidina é muito forte e é fácil marcar os ligantes com biotina. Atualmente, esses ligantes são anticorpos monoclonais produzidos a partir de culturas de células animais que se ligam especificamente a receptores e moléculas expressas pelo tipo de célula alvo. Como os anticorpos não são humanizados, eles desencadearão uma resposta imune quando usados em terapia humana. Humanizar anticorpos é um processo caro e demorado, por isso seria ideal encontrar uma fonte alternativa de ligantes, como peptídeos de direcionamento fabricados sinteticamente que desempenham a mesma função, mas sem os problemas imunológicos.
Tipos
Existem duas formas de ultrassom com contraste, não direcionado (usado na clínica hoje) e direcionado (em desenvolvimento pré-clínico). Os dois métodos diferem ligeiramente um do outro.
CEUS não direcionado
Microbolhas não direcionadas, como as já mencionadas SonoVue, Optison ou Levovist, são injetadas por via intravenosa na circulação sistêmica em um pequeno bolus. As microbolhas permanecerão na circulação sistêmica por um determinado período de tempo. Durante esse tempo, as ondas de ultrassom são direcionadas para a área de interesse. Quando as microbolhas no sangue passam pela janela de imagem, os núcleos de gás compressível das microbolhas oscilam em resposta ao campo de energia sônica de alta frequência, conforme descrito no artigo de ultrassom . As microbolhas refletem um eco único que contrasta fortemente com o tecido circundante devido à incompatibilidade de ordens de magnitude entre a microbolha e a ecogenicidade do tecido. O sistema de ultrassom converte a forte ecogenicidade em uma imagem com contraste da área de interesse. Desta forma, o eco da corrente sanguínea é aumentado, permitindo ao médico distinguir o sangue dos tecidos circundantes.
CEUS direcionado
O ultrassom com contraste direcionado funciona de maneira semelhante, com algumas alterações. Microbolhas direcionadas a ligantes que se ligam a determinados marcadores moleculares que são expressos pela área de interesse de imagem ainda são injetadas sistemicamente em um pequeno bolus. As microbolhas teoricamente viajam através do sistema circulatório, eventualmente encontrando seus respectivos alvos e se ligando especificamente. As ondas de ultrassom podem então ser direcionadas à área de interesse. Se um número suficiente de microbolhas se ligou na área, seus núcleos de gás compressível oscilam em resposta ao campo de energia sônica de alta frequência, conforme descrito no artigo de ultrassom . As microbolhas direcionadas também refletem um eco único que contrasta fortemente com o tecido circundante devido à incompatibilidade de ordens de magnitude entre a microbolha e a ecogenicidade do tecido. O sistema de ultrassom converte a forte ecogenicidade em uma imagem com contraste da área de interesse, revelando a localização das microbolhas ligadas. A detecção de microbolhas ligadas pode, então, mostrar que a área de interesse está expressando aquele marcador molecular particular, que pode ser indicativo de um determinado estado de doença, ou identificar células específicas na área de interesse.
Formulários
A ultrassonografia com contraste não direcionado é atualmente aplicada em ecocardiografia e radiologia . O ultrassom com contraste direcionado está sendo desenvolvido para uma variedade de aplicações médicas.
CEUS não direcionado
Microbolhas não direcionadas como Optison e Levovist são atualmente usadas em ecocardiografia. Além disso, o agente de contraste para ultrassom SonoVue é usado em radiologia para caracterização de lesões.
- Delineamento da borda do órgão : microbolhas podem aumentar o contraste na interface entre o tecido e o sangue. Uma imagem mais clara dessa interface oferece ao clínico uma imagem melhor da estrutura de um órgão. A estrutura do tecido é crucial em ecocardiogramas, onde um adelgaçamento, espessamento ou irregularidade na parede do coração indica uma condição cardíaca séria que requer monitoramento ou tratamento.
- Volume sanguíneo e perfusão : a ultrassonografia com contraste é uma promessa para (1) avaliar o grau de perfusão sanguínea em um órgão ou área de interesse e (2) avaliar o volume sanguíneo em um órgão ou área de interesse. Quando usadas em conjunto com o ultrassom Doppler , as microbolhas podem medir a taxa de fluxo do miocárdio para diagnosticar problemas de válvula. E a intensidade relativa dos ecos das microbolhas também pode fornecer uma estimativa quantitativa do volume de sangue.
- Caracterização da lesão : a ultrassonografia com contraste desempenha um papel na diferenciação entre lesões hepáticas focais benignas e malignas. Essa diferenciação depende da observação ou processamento do padrão vascular dinâmico em uma lesão em relação ao parênquima do tecido circundante .
CEUS direcionado
-
Inflamação : os agentes de contraste podem ser projetados para se ligarem a certas proteínas que se expressam em doenças inflamatórias, como doença de Crohn , aterosclerose e até ataques cardíacos . As células de interesse em tais casos são células endoteliais de vasos sanguíneos e leucócitos :
- Os vasos sanguíneos inflamados expressam especificamente certos receptores, funcionando como moléculas de adesão celular , como VCAM-1, ICAM-1, E-selectina . Se as microbolhas forem direcionadas a ligantes que ligam essas moléculas, elas podem ser usadas em ecocardiografia de contraste para detectar o início da inflamação. A detecção precoce permite o desenho de melhores tratamentos. Têm sido feitas tentativas para equipar microbolhas com anticorpos monoclonais que se ligam a P-selectina , ICAM-1 e VCAM-1 , mas a adesão ao alvo molecular foi pobre e uma grande fração de microbolhas que se ligaram ao alvo se separaram rapidamente, especialmente em altas tensões de cisalhamento de relevância fisiológica.
- Os leucócitos possuem alta eficiência de adesão, em parte devido a uma selectina de ligante duplo - sistema de parada celular de integrina . Um ligante: par receptor ( PSGL-1 : selectina) tem uma taxa de ligação rápida para retardar o leucócito e permite o segundo par (integrina: superfamília de imunoglobulinas ), que tem uma taxa de ativação mais lenta, mas uma taxa de desativação lenta para interromper o leucócito, aumentando cineticamente a adesão. Têm sido feitas tentativas para fazer os agentes de contraste se ligarem a tais ligantes, com técnicas como direcionamento de ligante duplo de receptores distintos para microesferas de polímero e biomimética do sistema de retenção de células de integrina-selectina do leucócito, tendo mostrado uma eficiência de adesão aumentada, mas ainda não eficiente o suficiente para permitir o uso clínico de ultra-som com contraste direcionado para a inflamação.
- Trombose e trombólise : as plaquetas ativadassão os principais componentes dos coágulos sanguíneos (trombos). As microbolhas podem ser conjugadas a um fragmento variável recombinante de cadeia única específico para a glicoproteína IIb / IIIa ativada(GPIIb / IIIa), que é o receptor de superfície plaquetária mais abundante. Apesar do alto estresse de cisalhamento na área do trombo, as microbolhas direcionadas a GPIIb / IIIa se ligarão especificamente às plaquetas ativadas e permitirão imagens moleculares em tempo real da trombose, como no infarto do miocárdio , bem como monitorar o sucesso ou falha da trombólise farmacológica.
- Câncer : as células cancerosas também expressam um conjunto específico de receptores, principalmente receptores que estimulam a angiogênese , ou o crescimento de novos vasos sanguíneos. Se as microbolhas forem direcionadas a ligantes que se ligam a receptores como VEGF ou glicoproteína IIb / IIIa ativada, elas podem identificar áreas de câncer de forma não invasiva e específica.
- Entrega do gene : o DNA do vetor pode ser conjugado às microbolhas. Microbolhas podem ser direcionadas com ligantes que se ligam a receptores expressos pelo tipo de célula de interesse. Quando a microbolha alvo se acumula na superfície da célula com sua carga útil de DNA, o ultrassom pode ser usado para estourar a microbolha. A força associada ao estouro pode permeabilizar temporariamente os tecidos circundantes e permitir que o DNA entre mais facilmente nas células. Microbolhas teranósticas direcionadas (direcionadas a VCAM-1 ) foram empregadas para entregar miR126 em um ambiente pré-clínico para interromper o desenvolvimento de AAA in vivo.
- Entrega de medicamentos: os medicamentos podem ser incorporados à casca lipídica da microbolha. O tamanho grande da microbolha em relação a outros veículos de distribuição de drogas, como lipossomas, pode permitir que uma maior quantidade de droga seja distribuída por veículo. Ao direcionar a microbolha carregada de droga com ligantes que se ligam a um tipo de célula específico, a microbolha não só entregará a droga especificamente, mas também pode fornecer a verificação de que a droga é entregue se a área for capturada por ultrassom.
Vantagens
Além dos pontos fortes mencionados na entrada da ultrassonografia médica, a ultrassonografia com contraste acrescenta estas vantagens adicionais:
- O corpo é 73% de água e, portanto, acusticamente homogêneo. O sangue e os tecidos circundantes têm ecogenicidade semelhante, por isso também é difícil discernir claramente o grau de fluxo sanguíneo, perfusão ou a interface entre o tecido e o sangue usando o ultrassom tradicional.
- A imagem de ultrassom permite a avaliação em tempo real do fluxo sanguíneo.
- A destruição das microbolhas por ultrassom no plano da imagem permite a quantificação absoluta da perfusão do tecido.
- A imagem molecular ultrassônica é mais segura do que as modalidades de imagem molecular, como a imagem por radionuclídeo, porque não envolve radiação.
- Modalidades alternativas de imagem molecular, como ressonância magnética , PET e SPECT são muito caras. O ultrassom, por outro lado, é muito econômico e amplamente disponível.
- Uma vez que as microbolhas podem gerar esses sinais fortes, uma dosagem intravenosa mais baixa é necessária, microgramas de microbolhas são necessários em comparação com os miligramas para outras modalidades de imagem molecular, como agentes de contraste de ressonância magnética .
- As estratégias de direcionamento para microbolhas são versáteis e modulares. Visar uma nova área envolve apenas a conjugação de um novo ligante.
- O direcionamento ativo pode ser aumentado (adesão aprimorada de microbolhas) pela força da radiação acústica usando um sistema de imagem de ultrassom clínico em modo 2D e modo 3D.
Desvantagens
Além dos pontos fracos mencionados na entrada da ultrassonografia médica, a ultrassonografia com contraste apresenta as seguintes desvantagens:
- As microbolhas não duram muito em circulação. Eles têm tempos de residência de baixa circulação porque são absorvidos pelas células do sistema imunológico ou pelo fígado ou baço, mesmo quando revestidos com PEG.
- O ultrassom produz mais calor à medida que a frequência aumenta, portanto, a frequência ultrassônica deve ser monitorada cuidadosamente.
- As microbolhas explodem em baixas frequências de ultrassom e em altos índices mecânicos (MI), que é a medida da pressão acústica negativa do sistema de imagem de ultrassom. Aumentar o MI aumenta a qualidade da imagem, mas há compensações com a destruição das microbolhas. A destruição das microbolhas pode causar rupturas locais da microvasculatura e hemólise .
- Os ligantes de direcionamento podem ser imunogênicos, uma vez que os ligantes de direcionamento atuais usados em experimentos pré-clínicos são derivados de cultura animal .
- Baixa eficiência de adesão de microbolhas direcionadas, o que significa que uma pequena fração das microbolhas injetadas se ligam à área de interesse. Esse é um dos principais motivos pelos quais o ultrassom com contraste direcionado permanece nos estágios de desenvolvimento pré-clínico.