Redução eletroquímica do dióxido de carbono - Electrochemical reduction of carbon dioxide
A redução eletroquímica do dióxido de carbono é a conversão do dióxido de carbono ( CO
2) para espécies químicas mais reduzidas usando energia elétrica. É uma etapa possível no amplo esquema de captura e utilização de carbono ; no entanto, é considerada uma das abordagens mais promissoras.
A redução eletroquímica do dióxido de carbono representa um meio possível de produção de produtos químicos ou combustíveis, convertendo o dióxido de carbono ( CO
2) Para matérias primas orgânicas, tais como ácido fórmico (HCOOH) , monóxido de carbono (CO) , metano (CH 4 ) , etileno (C 2 H 4 ) e etanol (C 2 H 5 OH) . Entre os catalisadores metálicos mais seletivos neste campo estão o estanho para o ácido fórmico, a prata para o monóxido de carbono e o cobre para o metano, etileno ou etanol. Metanol, propanol e 1-butanol também têm sido produzidos via redução eletroquímica de CO 2 , embora em pequenas quantidades.
Os primeiros exemplos de redução eletroquímica do dióxido de carbono datam do século 19, quando o dióxido de carbono foi reduzido a monóxido de carbono usando um cátodo de zinco . As pesquisas nesse campo se intensificaram na década de 1980, após os embargos do petróleo da década de 1970. A partir de 2021, a redução eletroquímica de dióxido de carbono em escala piloto está sendo desenvolvida por várias empresas, incluindo a Siemens , Dioxide Materials e Twelve .
Produtos químicos do dióxido de carbono
Na fixação de carbono , as plantas convertem o dióxido de carbono em açúcares, dos quais se originam muitas vias biossintéticas. O catalisador responsável por esta conversão, RuBisCO , é a proteína mais comum na terra. Alguns organismos anaeróbicos empregam enzimas para converter CO 2 em monóxido de carbono , a partir do qual os ácidos graxos podem ser produzidos.
Na indústria, alguns produtos são feitos de CO 2 , incluindo ureia , ácido salicílico , metanol e certos carbonatos inorgânicos e orgânicos. No laboratório, o dióxido de carbono às vezes é usado para preparar ácidos carboxílicos em um processo conhecido como carboxilação . Nenhum eletrolisador eletroquímico de CO 2 que opera em temperatura ambiente foi comercializado. Células eletrolisadoras de óxido sólido de temperatura elevada (SOECs) para redução de CO 2 a CO estão disponíveis comercialmente. Por exemplo, a Haldor Topsoe oferece SOECs para redução de CO 2 com um relatado de 6-8 kWh por Nm 3 CO produzido e pureza de até 99,999% CO.
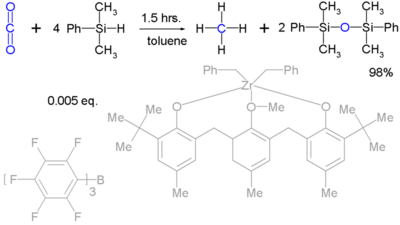
Os hidrosilanos reduzem o dióxido de carbono (para metano ): Infelizmente, essas reações são estequiométricas e de interesse exclusivamente acadêmico.
Eletrocatálise
A redução eletroquímica do dióxido de carbono a vários produtos é geralmente descrita como:
| Reação | Potencial de redução
E o (V) |
|---|---|
| CO 2 + 2 H + + 2 e - → HCOOH | -0,61 |
| CO 2 + 2 H + + 2 e - → CO + H 2 O | -0,53 |
| CO 2 + 8 H + + 8 e - → CH 4 + 2 H 2 O | -0,24 |
| 2 CO 2 + 12 H + + 12 e - → C 2 H 4 + 4 H 2 O | -0,349 |
| 2 CO 2 + 12 H + + 12 e - → C 2 H 5 OH + 3 H 2 O | -0,329 |
Os potenciais redox para essas reações são semelhantes aos da evolução de hidrogênio em eletrólitos aquosos, portanto, a redução eletroquímica de CO 2 é geralmente competitiva com a reação de evolução de hidrogênio.
Os métodos eletroquímicos têm recebido atenção significativa: 1) à pressão e à temperatura ambiente; 2) em conexão com fontes de energia renováveis (veja também combustível solar ) 3) controlabilidade competitiva, modularidade e aumento de escala são relativamente simples. A redução eletroquímica ou conversão eletrocatalítica de CO 2 pode produzir produtos químicos de valor agregado, como metano, etileno, etanol, etc., e os produtos são principalmente dependentes dos catalisadores selecionados e potenciais operacionais (aplicando tensão de redução).
Uma variedade de catalisadores homogêneos e heterogêneos foram avaliados. Supõe-se que muitos desses processos operam por intermédio de complexos metálicos de dióxido de carbono . Muitos processos sofrem de alto potencial, baixa eficiência de corrente, baixa seletividade, cinética lenta e / ou baixa estabilidade do catalisador.
A composição do eletrólito pode ser decisiva. Eletrodos de difusão de gás são benéficos.
Veja também
- Eletrometanogênese
- Biobateria
- Eletrocombustível
- Bateria de limão
- Redução fotoeletroquímica de dióxido de carbono
- Redução fotoquímica do dióxido de carbono
- Conversão de energia eletroquímica
- Reator bioeletroquímico
Notas
Referências
Leitura adicional
- LaConti AB, Molter TM, Zagaja JA (maio de 1986). Redução eletroquímica de dióxido de carbono . Online: Informações para a Indústria de Defesa . Arquivado do original em 27 de março de 2012.
- Fujita E (janeiro de 2000). Dióxido de carbono (redução) . Upton, NY (Estados Unidos): Brookhaven National Lab. (BNL).
- Neelameggham NR. "Tecnologias de redução de dióxido de carbono: uma sinopse do simpósio em TMS 2008" . The Minerals, Metals & Materials Society (TMS) .