Fumarase - Fumarase
Fumarase (ou fumarato hidratase ) é uma enzima que catalisa a hidratação / desidratação reversível de fumarato em malato . Fumarase vem em duas formas: mitocondrial e citosólica . A isoenzima mitocondrial está envolvida no Ciclo de Krebs (também conhecido como Ciclo do Ácido Tricarboxílico [TCA] ou Ciclo do Ácido Cítrico), e a isoenzima citosólica está envolvida no metabolismo de aminoácidos e fumarato. A localização subcelular é estabelecida pela presença de uma sequência sinal no terminal amino na forma mitocondrial, enquanto a localização subcelular na forma citosólica é estabelecida pela ausência da sequência sinal encontrada na variedade mitocondrial.
Esta enzima participa em 2 vias metabólicas : ciclo do ácido cítrico , redutora ciclo do ácido cítrico (CO 2 de fixação), e também é importante em carcinoma de células renais . Mutações nesse gene foram associadas ao desenvolvimento de leiomiomas na pele e no útero em combinação com carcinoma de células renais.
Nomenclatura
Esta enzima pertence à família das liases , especificamente as hidro-liases, que clivam as ligações carbono-oxigênio. O nome sistemático desta classe de enzimas é (S) -malato hidro-liase (formadora de fumarato) . Outros nomes de uso comum incluem:
- fumarase
- L-malato hidro-liase
- (S) -malato hidro-liase
Estrutura
Gene
O gene FH está localizado na posição cromossômica 1q42.3-q43. O gene FH contém 10 exões.
Proteína
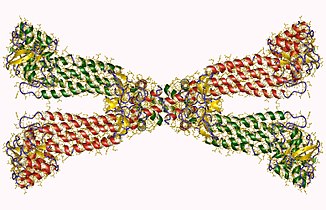
Observou-se que as estruturas de cristal da fumarase C de Escherichia coli têm dois sítios de ligação de dicarboxilato ocupados . Eles são conhecidos como site ativo e site B. O sítio ativo e o sítio B são ambos identificados como tendo áreas não ocupadas por um ligante ligado . Esta estrutura de cristal chamada 'livre' demonstra a conservação da água do local ativo. Orientação semelhante foi descoberta em outras estruturas de cristal de fumarase C. A pesquisa cristalográfica no local B da enzima observou que há uma mudança em His129. Essas informações sugerem que a água é um componente permanente do local ativo. Também sugere que o uso de um imidazol - imidazólio controlos de conversão aceder ao site B alostérico.
Função
Mecanismo
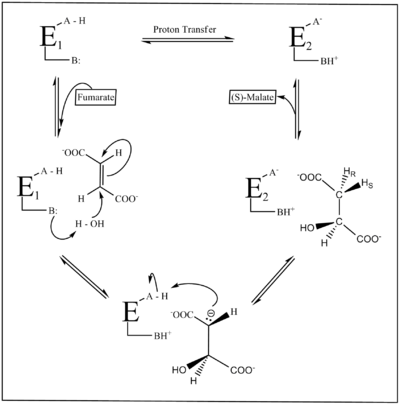
A Figura 2 mostra o mecanismo de reação da fumarase. Dois grupos ácido-base catalisam a transferência de prótons, e o estado de ionização desses grupos é em parte definido por duas formas das enzimas E 1 e E 2 . Em E 1 , os grupos existem em um estado AH / B: neutralizado internamente, enquanto em E 2 , eles ocorrem em um estado A- / BH + zwitteriônico . E 1 se liga ao fumarato e facilita sua transformação em malato, e E 2 se liga ao malato e facilita sua transformação em fumarato. As duas formas devem sofrer isomerização com cada turnover catalítico.
Apesar de seu significado biológico, o mecanismo de reação da fumarase não é completamente compreendido. A própria reação pode ser monitorada em qualquer direção; no entanto, é a formação do fumarato a partir de S-malato em particular, que é menos compreendido, devido ao elevado pKa um valor de a H R átomo (Fig. 1) que é removido sem a ajuda de quaisquer co-factores ou coenzimas . No entanto, a reação de fumarato em L-malato é melhor compreendida e envolve uma hidratação estereoespecífica de fumarato para produzir S-malato por trans-adição de um grupo hidroxila e um átomo de hidrogênio através de uma adição trans 1,4 de um grupo hidroxila. As primeiras pesquisas sobre essa reação sugeriram que a formação do fumarato a partir do S-malato envolvia a desidratação do malato em um intermediário carbocátio, que então perde o próton alfa para formar o fumarato. Isso levou à conclusão de que, na formação de S-malato a partir da eliminação do fumarato E1 , a protonação do fumarato para o carbocátion foi seguida pela adição de um grupo hidroxila de H 2 O. No entanto, ensaios mais recentes forneceram evidências de que o mecanismo realmente ocorre através de uma eliminação catalisada por ácido-base por meio de uma eliminação E1CB intermediária carbaniônica (Figura 2).
Via bioquímica
A função da fumarase no ciclo do ácido cítrico é facilitar uma etapa de transição na produção de energia na forma de NADH . No citosol, a enzima metaboliza o fumarato, que é um subproduto do ciclo da ureia e também do catabolismo dos aminoácidos. Estudos revelaram que o sítio ativo é composto de resíduos de aminoácidos de três das quatro subunidades da enzima tetramérica.
O principal local de ligação na fumarase é conhecido como local catalítico A. Estudos revelaram que o local catalítico A é composto de resíduos de aminoácidos de três das quatro subunidades da enzima tetramérica. Dois potenciais resíduos catalíticos de ácido-base na reação incluem His 188 e Lys 324.
Subtipos
Existem duas classes de fumarases. As classificações dependem da disposição de sua subunidade relativa, de seus requisitos de metal e de sua estabilidade térmica. Isso inclui a classe I e a classe II. As fumarases de classe I são capazes de mudar de estado ou se tornarem inativas quando submetidas a calor ou radiação, são sensíveis ao ânion superóxido, são dependentes de Ferro II (Fe2 +) e são proteínas diméricas com cerca de 120 kD. As fumarases de classe II, encontradas tanto em procariotos quanto em eucariotos, são enzimas tetraméricas de 200.000 D que contêm três segmentos distintos de aminoácidos significativamente homólogos. Eles também são independentes do ferro e estáveis termicamente. Os procariotos são conhecidos por terem três formas diferentes de fumarase: Fumarase A, Fumarase B e Fumarase C. Fumarase C é uma parte das fumarases classe II, enquanto Fumarase A e Fumarase B de Escherichia coli ( E. coli ) são classificadas como classe EU.
Outros substratos
Os principais substratos da fumarase são malato e fumarato. No entanto, a enzima também pode catalisar a desidratação do D- tartarato, que resulta em enol- oxaloacetato . O enol-oxaloacetato pode então izomerizar em ceto-oxaloacetato. Tanto a Fumarase A quanto a Fumarase B têm essencialmente a mesma cinética para a conversão reversível de malato em fumarase, mas a Fumarase B tem uma eficiência catalítica muito maior para a conversão de D-tartarato em oxaloacetato em comparação com a Fumarase A. Isso permite bactérias como a E. coli use D-tartarato para o seu crescimento; o crescimento de mutantes com um gene disruptivo fumB que codifica Fumarase B em D-tartarato foi severamente prejudicado.
Significado clínico
Deficiência de fumarase é caracterizada por polihidrâmnio e anormalidades cerebrais fetais. No período do recém-nascido, os achados incluem anormalidades neurológicas graves, alimentação inadequada, deficiência de crescimento e hipotonia . Suspeita-se de deficiência de fumarase em bebês com múltiplas anormalidades neurológicas graves na ausência de uma crise metabólica aguda. A inatividade das formas citosólica e mitocondrial da fumarase são causas potenciais. Concentração elevada isolada de ácido fumárico na análise de ácido orgânico na urina é altamente sugestiva de deficiência de fumarase. O teste genético molecular para a deficiência de fumarase está atualmente disponível.
A fumarase é prevalente em tecidos fetais e adultos. Uma grande porcentagem da enzima é expressa na pele , na paratireóide , na linfa e no cólon . Mutações na produção e desenvolvimento de fumarase levaram à descoberta de várias doenças relacionadas com fumarase em humanos. Estes incluem tumores mesenquimais benignos do útero, leiomiomatose e carcinoma de células renais e deficiência de fumarase . Mutações germinais na fumarase estão associadas a duas condições distintas. Se a enzima tem mutação missense e deleções in-frame da extremidade 3 ', resulta a deficiência de fumarase. Se contiver mutação missense 5 ' heterozigótica e deleções (variando de um par de bases a todo o gene), pode ocorrer leiomiomatose e carcinoma de células renais / síndrome de Reed ( leiomiomatose cutânea múltipla e uterina ).
Mapa de caminho interativo
Clique nos genes, proteínas e metabólitos abaixo para acessar os respectivos artigos.
Veja também
Referências
links externos
- Fumarase nos títulos de assuntos médicos da Biblioteca Nacional de Medicina dos EUA (MeSH)
- Estrutura de Fumarato
- Estrutura de S-malato
- Link para a repartição do ciclo do ácido cítrico
- Vídeo de Fumarate → (S) L-Malato