Acetato de mercúrio (II) - Mercury(II) acetate

|
|
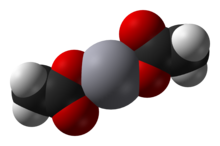
|
|
| Nomes | |
|---|---|
| Outros nomes
mercuriacetato de acetato de mercúrio |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard |
100.014.993 |
| Número EC | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
| Número ONU | 1629 |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| C 4 H 6 O 4 Hg | |
| Massa molar | 318,678 g / mol |
| Aparência | sólido branco |
| Odor | odor suave de vinagre |
| Densidade | 3,28 g / cm 3 , sólido |
| Ponto de fusão | 179 ° C (354 ° F; 452 K) (decompõe-se) |
| 25 g / 100 mL (10 ° C) 100 g / 100 mL (100 ° C) |
|
| Solubilidade | solúvel em álcool , éter dietílico |
| −100 · 10 −6 cm 3 / mol | |
| Perigos | |
| Pictogramas GHS |
  
|
| Palavra-sinal GHS | Perigo |
| H300 , H310 , H330 , H373 , H400 , H410 | |
| P260 , P262 , P264 , P270 , P271 , P273 , P280 , P284 , P301 + 310 , P302 + 350 , P304 + 340 , P310 , P314 , P320 , P321 , P322 , P330 , P361 , P363 , P391 , P403 + 233 , P405 , P501 | |
| NFPA 704 (diamante de fogo) | |
| Dose ou concentração letal (LD, LC): | |
|
LD 50 ( dose mediana )
|
40,9 mg / kg (rato, oral) 23,9 mg / kg (camundongo, oral) |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O acetato de mercúrio (II) é o composto químico com a fórmula Hg ( O 2 C C H 3 ) 2 . Comumente abreviado Hg (OAc) 2 , este composto é empregado como um reagente para gerar compostos organomercúrio a partir de precursores orgânicos insaturados. É um sólido branco solúvel em água, mas as amostras aparecem amareladas com o tempo devido à decomposição.
Estrutura
O acetato de mercúrio (II) é um sólido cristalino que consiste em moléculas de Hg (OAc) 2 isoladas com distâncias de Hg-O de 2,07 Å. Três longas e fracas ligações intermoleculares de Hg ··· O de cerca de 2,75 Å também estão presentes, resultando em uma geometria de coordenação piramidal quadrada ligeiramente distorcida em Hg.
Síntese e reações
O acetato de mercúrio (II) pode ser produzido pela reação do óxido de mercúrio com o ácido acético.
Reações inorgânicas
O acetato de mercúrio (II) em solução de ácido acético reage com H 2 S para precipitar rapidamente o polimorfo preto (β) de HgS. Com o aquecimento suave da pasta, o sólido preto se converte na forma vermelha. O mineral cinábrio é HgS vermelho. A precipitação do HgS, bem como de alguns outros sulfetos, usando sulfeto de hidrogênio, é uma etapa da análise inorgânica qualitativa .
Química orgânica
Os arenos ricos em elétrons sofrem "mercuração" após o tratamento com Hg (OAc) 2 . Este comportamento é ilustrado com fenol :
- C 6 H 5 OH + Hg (OAc) 2 → C 6 H 4 (OH) -2-HgOAc + HOAc
O grupo acetato (OAc) que permanece no mercúrio pode ser deslocado pelo cloreto:
- C 6 H 4 (OH) -2-HgOAc + NaCl → C 6 H 4 (OH) -2-HgCl + NaOAc
O centro do Hg 2+ liga-se aos alcenos , induzindo a adição de hidróxido e alcóxido . Por exemplo, o tratamento de acrilato de metila com acetato de mercúrio em metanol dá um éster α-mercúrio:
- Hg (OAc) 2 + CH 2 = CHCO 2 CH 3 + CH 3 OH → CH 3 OCH 2 CH (HgOAc) CO 2 CH 3 + HOAc
Explorando a alta afinidade do mercúrio (II) para ligantes de enxofre, Hg (OAc) 2 pode ser usado como um reagente para desproteger grupos tiol em síntese orgânica . Da mesma forma, o Hg (OAc) 2 tem sido usado para converter ésteres de tiocarbonato em ditiocarbonatos:
- (RS) 2 C = S + H 2 O + Hg (OAc) 2 → (RS) 2 C = O + HgS + 2 HOAc
O acetato de mercúrio (II) é usado para reações de oximercuração .
Um famoso uso de Hg (OAc) 2 foi na síntese de Idoxuridina .

