Olefinação Takai - Takai olefination
| Olefinação Takai | |
|---|---|
| Nomeado após | Kazuhiko Takai |
| Tipo de reação | Reação de formação de ligação carbono-carbono |
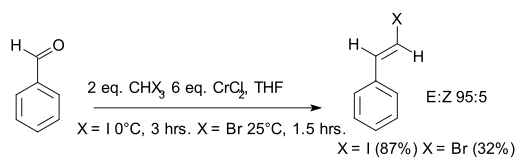
A olefinação Takai em química orgânica descreve a reação orgânica de um aldeído com um composto de diorganocromio para formar um alceno . É um nome de reação , referenciando Kazuhiko Takai , que a relatou pela primeira vez em 1986. Na reação original, a espécie organocromática é gerada a partir de iodofórmio ou bromofórmio e um excesso de cloreto de cromo (II) e o produto é um haleto de vinila . Uma vantagem principal dessa reação é a configuração E da ligação dupla que é formada. De acordo com o relatório original, alternativas existentes, como a reação de Wittig, forneciam apenas misturas.
No mecanismo de reação proposto por Takai, o cromo (II) é oxidado a cromo (III) eliminando dois equivalentes de um haleto. O complexo de carbodianião geminal assim formado (determinado como [Cr 2 Cl 4 (CHI) (THF) 4 ]) reage com o aldeído em uma adição 1,2 ao longo de uma das ligações de carbono para cromo e na próxima etapa ambos tendo cromo grupos se envolvem em uma reação de eliminação . Na projeção de Newman , pode-se ver como os volumes estéricos dos grupos de cromo e os volumes estéricos dos grupos alquil e halogênio conduzem essa reação em direção à anti-eliminação.
História da reação
Antes da introdução deste protocolo à base de cromo, as reações de olefinação geralmente geravam alcenos Z ou misturas de isômeros. Reações de olefinação semelhantes foram realizadas usando uma variedade de reagentes como zinco e cloreto de chumbo; no entanto, essas reações de olefinação geralmente levam à formação de dióis - a reação de McMurry - em vez da metilação ou alquilidenação de aldeídos. Para contornar esse problema, o grupo Takai examinou o potencial sintético dos sais de cromo (II).
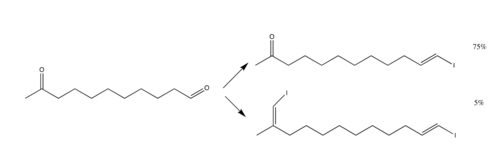
A reação emprega principalmente o uso de aldeídos, mas podem ser usadas cetonas. No entanto, as cetonas não reagem tão bem quanto os aldeídos; assim, para um composto com grupos aldeído e cetona, a reação pode ter como alvo apenas o grupo aldeído e deixar o grupo cetona intacto.
As desvantagens da reação incluem o fato de que estequiometricamente, devem ser utilizados 4 equivalentes de cloreto de cromo, uma vez que ocorre uma redução de dois átomos de halogênio. Existem maneiras de limitar a quantidade de cloreto de cromo, nomeadamente através da utilização do equivalente de zinco, mas este método continua impopular.
Olefinação Takai-Utimoto
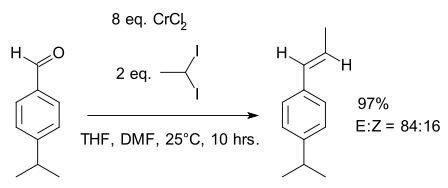
Em uma segunda publicação, o escopo da reação foi estendido para intermediários de diorganocromio contendo grupos alquil em vez de halogênios: