Tetraiodeto de titânio - Titanium tetraiodide
|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Iodeto de titânio (IV)
|
|
| Outros nomes
Tetraiodeto de titânio
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.028.868 |
| Número EC | |
|
PubChem CID
|
|
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| TiI 4 | |
| Massa molar | 555,485 g / mol |
| Aparência | cristais marrom-avermelhados |
| Densidade | 4,3 g / cm 3 |
| Ponto de fusão | 150 ° C (302 ° F; 423 K) |
| Ponto de ebulição | 377 ° C (711 ° F; 650 K) |
| hidrólise | |
| Solubilidade em outros solventes | solúvel em CH 2 Cl 2 CHCl 3 CS 2 |
| Estrutura | |
| cúbico ( a = 12,21 Å) | |
| tetraédrico | |
| 0 D | |
| Perigos | |
| Riscos principais | hidrólise violenta corrosiva |
| Frases R (desatualizado) | 34-37 |
| Frases S (desatualizado) | 26-36 / 37 / 39-45 |
| Compostos relacionados | |
|
Outros ânions
|
Brometo de titânio (IV) Cloreto de titânio (IV) Fluoreto de titânio (IV) |
|
Outros cátions
|
Tetraiodeto de silício Zircônio (IV) iodeto de Háfnio (IV) iodeto |
|
Compostos relacionados
|
Iodeto de titânio (III) |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
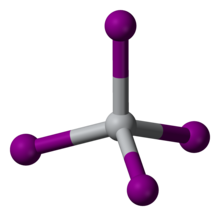
O tetraiodeto de titânio é um composto inorgânico com a fórmula TiI 4 . É um sólido volátil preto, relatado pela primeira vez por Rudolph Weber em 1863. É um intermediário no processo van Arkel – de Boer para a purificação de titânio.
Propriedades físicas
TiI 4 é um iodeto de metal binário molecular raro, que consiste em moléculas isoladas de centros tetraédricos de Ti (IV). As distâncias Ti-I são 261 pm . Refletindo seu caráter molecular, TiI 4 pode ser destilado sem decomposição em uma atmosfera; esta propriedade é a base de seu uso no processo van Arkel – de Boer. A diferença no ponto de fusão entre TiCl 4 (mp -24 ° C) e TiI 4 (mp 150 ° C) é comparável à diferença entre os pontos de fusão de CCl 4 (mp -23 ° C) e CI 4 (mp 168 ° C), refletindo a ligação intermolecular de van der Waals mais forte nos iodetos.
Existem dois polimorfos de TiI 4 , um dos quais é altamente solúvel em solventes orgânicos. Na forma cúbica menos solúvel, as distâncias Ti-I são 261 pm .
Produção
Três métodos são bem conhecidos: 1) A partir dos elementos, normalmente usando um forno tubular a 425 ° C:
- Ti + 2 I 2 → TiI 4
Esta reação pode ser revertida para produzir filmes altamente puros de metal Ti.
2) Reação de troca de tetracloreto de titânio e HI.
- TiCl 4 + 4 HI → TiI 4 + 4 HCl
3) Troca de óxido-iodeto de iodeto de alumínio .
- 3 TiO 2 + 4 AlI 3 → 3 TiI 4 + 2 Al 2 O 3
Reações
Como o TiCl 4 e o TiBr 4 , o TiI 4 forma adutos com bases de Lewis e também pode ser reduzido. Quando a redução é realizada na presença do metal Ti, obtém-se derivados poliméricos de Ti (III) e Ti (II), como CsTi 2 I 7 e a cadeia CsTiI 3 , respectivamente.
TiI 4 exibe ampla reatividade para alcenos e alcinos resultando em derivados de organoiodo. Também afeta os acoplamentos de pinacol e outras reações de formação de ligações CC.
