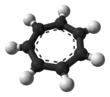
Catião Tropylium - Tropylium cation
 |
|||
|
|
|||
| Nomes | |||
|---|---|---|---|
|
Nome IUPAC preferido
Cicloheptatrienílio |
|||
| Outros nomes
cyc - C
7H+ 7, Cyclohepta-2,4,6-trienylium, Cyclohepta-1,3,5-triene, 2,4,6-Cycloheptatrienylium |
|||
| Identificadores | |||
|
Modelo 3D ( JSmol )
|
|||
| 1902352 | |||
| ChemSpider | |||
|
PubChem CID
|
|||
|
|||
|
|||
| Propriedades | |||
|
C 7H+ 7 |
|||
| Massa molar | 91,132 g · mol −1 | ||
| Estrutura | |||
| D 7h | |||
| heptágono regular | |||
| Compostos relacionados | |||
|
Outros ânions
|
Tetrafluoroborato de tropílio | ||
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|||
| Referências da Infobox | |||
Em química orgânica , o íon tropílio ou cátion cicloheptatrienil é uma espécie aromática com uma fórmula de [C 7 H 7 ] + . Seu nome deriva da molécula tropina a partir da qual o cicloheptatrieno (tropilideno) foi sintetizado pela primeira vez em 1881. Os sais do cátion tropílio podem ser estáveis, mesmo com nucleófilos de força moderada, por exemplo, tetrafluoroborato de tropílio e brometo de tropílio ( ver abaixo ). Seus sais de brometo e cloreto podem ser feitos de cicloheptatrieno e bromo ou pentacloreto de fósforo , respectivamente.
É um íon regular heptagonal , planar e cíclico. Possui 6 elétrons π (4 n + 2, onde n = 1), o que cumpre a regra de aromaticidade de Hückel . Ele pode se coordenar como um ligante para átomos de metal . A estrutura mostrada é um composto de sete contribuintes de ressonância em que cada átomo de carbono carrega parte da carga positiva.
História
Em 1891 G. Merling obteve um composto contendo bromo solúvel em água a partir da reação de cicloheptatrieno e bromo . Ao contrário da maioria dos brometos de hidrocarbil, este composto, mais tarde denominado brometo de tropílio, é solúvel em água, mas insolúvel em muitos solventes orgânicos. É purificado por cristalização em etanol quente. A reação com nitrato de prata aquoso deu imediatamente brometo de prata, indicando brometo lábil. O brometo de tropílio foi deduzido como um sal, C
7H+
7Br-
, por Doering e Knox em 1954 pela análise de seus espectros infravermelho e ultravioleta. As estruturas iônicas do perclorato de tropílio ( C
7H+
7ClO-
4) e iodeto de tropílio ( C
7H+
7eu-
) foram confirmados por cristalografia de raios-X . O comprimento da ligação das ligações carbono-carbono é maior (147 pm) do que aquelas do benzeno (140 pm), mas ainda mais curto do que aquelas de uma espécie de ligação simples típica como o etano (154 pm).
Acidez
O íon tropílio é um ácido em solução aquosa (ou seja, um ácido de Arrhenius ) como consequência de sua acidez de Lewis: ele primeiro atua como um ácido de Lewis para formar um aduto com água, que pode então doar um próton para outra molécula de água:
-
C
7H+
7+ 2 H
2O ⇌ C
7H
7OH + H
3O+
( O ácido bórico fornece soluções aquosas ácidas da mesma maneira.) A constante de equilíbrio é1,8 × 10 −5 , tornando-o quase tão ácido em água quanto o ácido acético .
Espectrometria de massa
O íon tropílio é freqüentemente encontrado na espectrometria de massa na forma de um sinal em m / z = 91 e é usado na análise de espectro de massa . Este fragmento é freqüentemente encontrado para compostos aromáticos contendo uma unidade benzila. Após a ionização , o fragmento de benzil forma um cátion ( PhCH+
2), que se reorganiza no cátion tropílio altamente estável ( C
7H+
7)
Reações
O cátion tropílio reage com nucleófilos para formar cicloheptatrienos substituídos, por exemplo:
-
C
7H+
7+ CN-
→ C
7H
7CN
A redução por hidreto de alumínio e lítio produz cicloheptatrieno .
A reação com um sal ciclopentadienida de sódio ou lítio produz 7-ciclopentadienilciclohepta-1,3,5-trieno :
-
C
7H+
7X-
+ C
5H-
5N / D+
→ C
7H
7C
5H
5+ NaX
Quando tratado com agentes oxidantes, como ácido crômico , o cátion tropílio sofre rearranjo em benzaldeído :
-
C
7H+
7+ HCrO-
4→ C
6H
5CHO + CrO
2+ H
2O
Muitos complexos metálicos de íon tropílio são conhecidos. Um exemplo é [Mo ( η 7- C 7 H 7 ) (CO) 3 ] + , que é preparado por abstração de hidreto de tricarbonil de cicloheptatrienemolibdênio .