Trissulfeto de arsênico - Arsenic trisulfide

|
|
|
|
|
|
|
| Nomes | |
|---|---|
|
Nome IUPAC preferido
Trissulfeto de arsênico |
|
| Outros nomes
Sulfeto de arsênio (III)
Orpiment |
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.013.744 |
| Número EC | |
|
PubChem CID
|
|
| Número RTECS | |
| UNII | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| Como 2 S 3 | |
| Massa molar | 246,02 g · mol −1 |
| Aparência | Cristais laranja |
| Densidade | 3,43 g cm -3 |
| Ponto de fusão | 310 ° C (590 ° F; 583 K) |
| Ponto de ebulição | 707 ° C (1.305 ° F; 980 K) |
| -70,0 · 10 −6 cm 3 / mol | |
| Estrutura | |
| P2 1 / n (No. 11) | |
|
a = 1147,5 (5) pm, b = 957,7 (4) pm, c = 425,6 (2) pm
α = 90 °, β = 90,68 (8) °, γ = 90 °
|
|
| piramidal (As) | |
| Perigos | |
| Pictogramas GHS |
 
|
| Palavra-sinal GHS | Perigo |
| H300 , H331 , H400 , H411 | |
| NFPA 704 (diamante de fogo) | |
| NIOSH (limites de exposição à saúde dos EUA): | |
|
PEL (permitido)
|
[1910,1018] TWA 0,010 mg / m 3 |
|
REL (recomendado)
|
Ca C 0,002 mg / m 3 [15 minutos] |
|
IDLH (perigo imediato)
|
Ca [5 mg / m 3 (como As)] |
| Compostos relacionados | |
|
Outros ânions
|
Trióxido de arsênio Trisseleneto de arsênio Telureto de arsênio |
|
Outros cátions
|
Trissulfeto de fósforo Trissulfeto de antimônio Sulfeto de bismuto |
|
Compostos relacionados
|
Tetrassulfeto tetraarsênico |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O trissulfeto de arsênio é o composto inorgânico com a fórmula As 2 S 3 . É um sólido amarelo escuro insolúvel em água. Também ocorre como o mineral orpimento (latim: auripigment), que tem sido usado como um pigmento chamado King's yellow. É produzido na análise de compostos de arsênio. É um grupo V / VI, semicondutor intrínseco do tipo p e exibe propriedades de mudança de fase fotoinduzida. O outro sulfeto de arsênio principal é o As 4 S 4 , um sólido vermelho-laranja conhecido como realgar mineral .
Estrutura
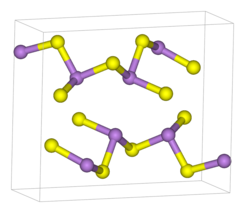
As 2 S 3 ocorre tanto na forma cristalina quanto na forma amorfa. Ambas as formas apresentam estruturas poliméricas consistindo de centros trigonais piramidais As (III) ligados por centros de sulfeto. Os centros de sulfeto são duplamente coordenados a dois átomos de arsênio. Na forma cristalina, o composto adota uma estrutura de folha ondulada. A ligação entre as folhas consiste em forças de van der Waals . A forma cristalina é geralmente encontrada em amostras geológicas. Amorfo As 2 S 3 não possui uma estrutura em camadas, mas é mais altamente reticulado. Como outros vidros, não há ordem de médio ou longo alcance, mas a primeira esfera de coordenação é bem definida. Como 2 S 3 é um bom formador de vidro e exibe uma ampla região de formação de vidro em seu diagrama de fase.
Propriedades
É um semicondutor , com um gap direto de 2,7 eV. O amplo gap de banda o torna transparente ao infravermelho entre 620 nm e 11 µm.
Síntese
Dos elementos
Amorfo As 2 S 3 é obtido através da fusão dos elementos a 390 ° C. O resfriamento rápido do fundido de reação dá um vidro. A reação pode ser representada com a equação química:
- 2 As + 3 S → As 2 S 3
Precipitação aquosa
O As 2 S 3 se forma quando as soluções aquosas contendo As (III) são tratadas com H 2 S. O arsênio era no passado analisado e testado por esta reação, que resulta na precipitação de As 2 S 3 , que é então pesado. As 2 S 3 podem mesmo ser precipitadas em HCl 6M. Como 2 S 3 é tão insolúvel que não é tóxico.
Reações
Após o aquecimento em vácuo, o As 2 S 3 polimérico "racha" para dar uma mistura de espécies moleculares, incluindo As 4 S 6 moleculares . O As 4 S 6 adota a geometria adamantana , como a observada para P 4 O 6 e As 4 O 6 . Quando um filme deste material é exposto a uma fonte de energia externa, como energia térmica (via recozimento térmico), radiação eletromagnética (ou seja, lâmpadas UV, lasers, feixes de elétrons)), As 4 S 6 polimeriza:
- 2 / n (As 2 S 3 ) n ⇌ As 4 S 6
Como 2 S 3 se dissolve caracteristicamente após o tratamento com soluções aquosas contendo íons sulfeto . A espécie de arsênio dissolvido é o trianion piramidal AsS3−
3:
- Como 2 S 3 + 6 NaSH → 2 AsS3−
3 + 3 H 2 S
As 2 S 3 é o anidrido do hipotético ácido tioarsenoso, As (SH) 3 . Após o tratamento com íons polissulfeto , As 2 S 3 se dissolve para dar uma variedade de espécies contendo ligações SS e As-S. Um derivado é S 7 As-S - , um anel que contém um centro de sulfido exocíclico ligado ao átomo de As. As 2 S 3 também se dissolvem em soluções fortemente alcalinas para dar uma mistura de AsS3−
3e AsO3−
3.
"Torrefação" como 2 S 3 no ar dá derivados tóxicos e voláteis, sendo esta conversão um dos riscos associados ao refino de minérios de metais pesados :
- 2 As 2 S 3 + 9 O 2 → As 4 O 6 + 6 SO 2
Usos contemporâneos
Como um fotorresiste inorgânico
Devido ao seu alto índice de refração de 2,45 e sua grande dureza Knoop em comparação com os fotorresistentes orgânicos , o As 2 S 3 foi investigado para a fabricação de cristais fotônicos com um gap fotônico completo. Avanços nas técnicas de padronização de laser, como gravação direta a laser tridimensional (3-D DLW) e química de corrosão química úmida , permitiram que esse material fosse usado como fotoresiste para fabricar nanoestruturas 3-D.
As 2 S 3 tem sido investigado para uso como material fotorresistente de alta resolução desde o início dos anos 1970, usando gravações aquosas. Embora esses decapantes aquosos permitissem a fabricação de estruturas 2-D de baixa razão de aspecto, eles não permitem a gravação de estruturas de alta razão de aspecto com periodicidade 3-D. Certos reagentes orgânicos, usados em solventes orgânicos, permitem a seletividade de alta corrosão necessária para produzir estruturas de alta razão de aspecto com periodicidade 3-D.
Aplicações médicas
As 2 S 3 e As 4 S 4 foram investigadas como tratamentos para a leucemia promielocítica aguda (APL).
Para óculos transmissores de infravermelho
O trissulfeto de arsênio fabricado na forma amorfa é usado como vidro calcogeneto para óptica infravermelha . É transparente entre 620 nm e 11 µm. O vidro de trissulfeto de arsênio é mais resistente à oxidação do que o trissulfeto de arsênio cristalino, o que minimiza as preocupações com a toxicidade. Também pode ser usado como material acústico-óptico .
O trissulfeto de arsênico foi usado para o distinto nariz cônico de oito lados sobre o buscador infravermelho do míssil de Havilland Firestreak .
Papel na arte antiga
Os antigos egípcios usavam orpimento, natural ou sintético, como pigmento na arte e na cosmética.
Diversos
O trissulfeto de arsênio também é usado como agente de bronzeamento . Antigamente, era usado com o corante índigo para a produção do azul lápis, que permitia a adição de tons de azul escuro ao tecido por meio de lápis ou pincel.
A precipitação de trissulfeto de arsênio é usada como um teste analítico para a presença de bactérias redutoras de arsênio dissimilatórias (DARB).
Segurança
Como 2 S 3 é tão insolúvel que sua toxicidade é baixa. Amostras envelhecidas podem conter quantidades substanciais de óxidos de arsênio, que são solúveis e, portanto, altamente tóxicos.
Ocorrência natural
Orpiment é encontrado em ambientes vulcânicos, frequentemente junto com outros sulfetos de arsênio, principalmente realgar . Às vezes é encontrado em veias hidrotérmicas de baixa temperatura, junto com alguns outros minerais de sulfeto e sulfossal.
Referências
Leitura adicional
- "Arsênico e compostos de arsênio", Avaliações Gerais de Carcinogenicidade: Uma Atualização dos Volumes 1 a 42 das Monografias da IARC (PDF) , Monografias da IARC sobre a Avaliação de Riscos Carcinogênicos para Suplemento Humano 7, Lyon, França: Agência Internacional de Pesquisa sobre o Câncer, 1987 , pp. 100-6, ISBN 92-832-1411-0. "Arsenic in Drinking Water", Some Drinking-water Disinfectants and Contaminants, including Arsenic (PDF) , IARC Monographs on the Evaluation of Carcinogenic Risks to Humans 84, Lyon, França: International Agency for Research on Cancer, 2004, pp. 39– 267, ISBN 92-832-1284-3.
- "Arsenic Compounds, Inorganic", Report on Carcinogens, décima primeira edição (PDF), US Department of Health and Human Services, Public Health Service, National Toxicology Program, 2005.

