Reação Barton-Kellogg - Barton–Kellogg reaction
| Reação Barton-Kellogg | |
|---|---|
| Nomeado após |
Sir Derek Barton Richard M. Kellogg |
| Tipo de reação | Reação de acoplamento |
| Identificadores | |
| ID da ontologia RSC | RXNO: 0000495 |
A reação de Barton-Kellogg é uma reação de acoplamento entre um composto diazo e uma tiocetona , dando um alceno por meio de um intermediário episulfeto . A reação de Barton-Kellogg também é conhecida como olefinação de Barton-Kellogg e síntese de olefina de Barton .
Esta reação foi iniciada por Hermann Staudinger , e também atende pelo nome de acoplamento diazo-tiocetona do tipo Staudinger .
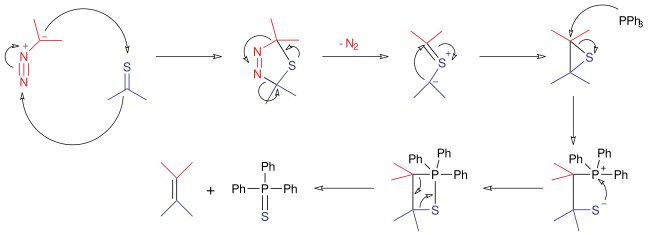
Mecanismo de reação
No mecanismo de reação para esta reação, o composto diazo reage como um 1,3-dipolo em uma cicloadição 1,3-dipolar com a tiocetona para dar um anel de tiadiazolina de 5 membros . Este intermediário é instável; ele expulsa uma molécula de nitrogênio para formar um ileto de tiocarbonil , que então se cicliza para formar um episulfeto estável . A trifenilfosfina reage como um nucleófilo , abrindo o anel de três membros para formar um sulfafosfatano. De maneira semelhante à reação de Wittig , esta estrutura expele sulfeto de trifenilfosfina para produzir um alceno.
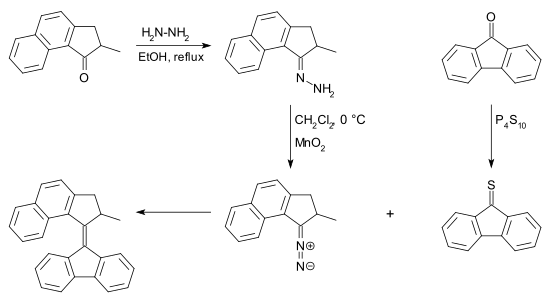
Escopo
O composto diazo pode ser obtido a partir de uma cetona por reação com hidrazina em uma hidrazona seguida de oxidação . Existem muitos reagentes para esta conversão, por exemplo óxido de prata (I) e (bis (trifluoroacetoxi) iodo) benzeno . A tiocetona necessária para esta reação pode ser obtida a partir de uma cetona e pentassulfeto de fósforo . A dessulfurização do episulfeto pode ser realizada por muitas fosfinas e também por pó de cobre .
A principal vantagem dessa reação sobre a reação de McMurry é a noção de que a reação pode ocorrer com duas cetonas diferentes. A este respeito, o acoplamento diazo-tiocetona é um acoplamento cruzado em vez de um homoacoplamento.
Referências
- ^ DHR Barton & BJ Willis (1970). "Síntese de olefinas por processos de extrusão dupla". J. Chem. Soc. D (19): 1225. doi : 10,1039 / C29700001225 .
- ^ RM Kellogg & S. Wassenaar (1970). "Iletos de tiocarbonila. Uma abordagem para" compostos de enxofre tetravalente ". Tetrahedron Lett. 11 (23): 1987. doi : 10.1016 / S0040-4039 (01) 98134-1 .
- ^ RM Kellogg (1976). "As moléculas R2CXCR2 incluindo azometina, carbonila e iletos de tiocarbonila. Suas sínteses, propriedades e reações". Tetraedro . 32 (18): 2165–2184. doi : 10.1016 / 0040-4020 (76) 85131-9 .
- ^ "Olefinação Barton-Kellogg". Reações e reagentes de nomes orgânicos abrangentes . 2010. pp. 249-253. doi : 10.1002 / 9780470638859.conrr056 . ISBN 9780470638859.
- ^ "Síntese de olefinas de Barton" . Merck Index (15ª ed.).
- ^ H. Staudinger & J. Siegwart (1920). "Einwirkungen von aliphatischen Diazoverbindungen auf Thioketone" . Helv. Chim. Acta . 3 : 833–840. doi : 10.1002 / hlca.19200030178 .
- ^ Matthijs KJ ter Wiel; Javier Vicario; Stephen G. Davey; Auke Meetsma e Ben L. Feringa (2005). "Novo procedimento para a preparação de alcenos altamente estericamente impedidos usando um reagente de iodo hipervalente" (PDF) . Química Orgânica e Biomolecular . 3 (1): 28–30. doi : 10.1039 / b414959a . PMID 15602594 .