Cianeto de cobre (I) - Copper(I) cyanide

|
|

|
|
| Nomes | |
|---|---|
|
Nome IUPAC
Cianeto de cobre (I)
|
|
| Outros nomes
Cianeto cuproso, cianeto de cobre, cupricina
|
|
| Identificadores | |
|
Modelo 3D ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100,008,076 |
| Número EC | |
|
PubChem CID
|
|
| Número RTECS | |
|
Painel CompTox ( EPA )
|
|
|
|
|
|
| Propriedades | |
| CuCN | |
| Massa molar | 89,563 g / mol |
| Aparência | pó esbranquiçado / amarelo claro |
| Densidade | 2,92 g / cm 3 |
| Ponto de fusão | 474 ° C (885 ° F; 747 K) |
| insignificante | |
|
Produto de solubilidade ( K sp )
|
3,47 × 10 −20 |
| Solubilidade | insolúvel em etanol , ácidos diluídos a frio ; solúvel em NH 4 OH , KCN |
| Estrutura | |
| monoclínico | |
| Perigos | |
| Ficha de dados de segurança | Oxford MSDS |
| Muito tóxico ( T + ) Perigoso para o meio ambiente ( N ) |
|
| Frases R (desatualizado) | R26 / 27/28 , R32 , R50 / 53 |
| Frases S (desatualizado) | (S1 / 2) , S7 , S28 , S29 , S45 , S60 , S61 |
| NFPA 704 (diamante de fogo) | |
| Ponto de inflamação | Não inflamável |
| NIOSH (limites de exposição à saúde dos EUA): | |
|
PEL (permitido)
|
TWA 1 mg / m 3 (como Cu) |
|
REL (recomendado)
|
TWA 1 mg / m 3 (como Cu) |
|
IDLH (perigo imediato)
|
TWA 100 mg / m 3 (como Cu) |
|
Exceto onde indicado de outra forma, os dados são fornecidos para materiais em seu estado padrão (a 25 ° C [77 ° F], 100 kPa). |
|
|
|
|
| Referências da Infobox | |
O cianeto de cobre (I) é um composto inorgânico com a fórmula CuCN. Este sólido esbranquiçado ocorre em dois polimorfos ; amostras impuras podem ser verdes devido à presença de impurezas de Cu (II). O composto é útil como catalisador , na eletrodeposição de cobre e como reagente na preparação de nitrilos .
Estrutura
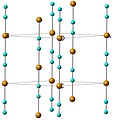
O cianeto de cobre é um polímero de coordenação . Ele existe em dois polimorfos, ambos contendo - [Cu-CN] - cadeias feitas de centros lineares de cobre (I) ligados por pontes de cianeto . No polimorfo de alta temperatura, HT-CuCN, que é isoestrutural com AgCN , o pacote de cadeias lineares em uma rede hexagonal e as cadeias adjacentes são deslocadas por +/- 1/3 c , Figura 1. No polimorfo de baixa temperatura, LT-CuCN, as cadeias se desviam da linearidade e se acumulam em camadas onduladas que se acumulam de forma AB com cadeias em camadas adjacentes giradas em 49 °, Figura 2.
O LT-CuCN pode ser convertido em HT-CuCN pelo aquecimento a 563 K em uma atmosfera inerte. Em ambos os polimorfos, os comprimentos das ligações de cobre para carbono e cobre para nitrogênio são de ~ 1,85 Å e os grupos de cianeto em ponte mostram desordem de ponta a ponta.
Preparação
O cianeto cuproso está disponível comercialmente e é fornecido como o polimorfo de baixa temperatura. Pode ser preparado pela redução de sulfato de cobre (II) com bissulfito de sódio a 60 ° C, seguido pela adição de cianeto de sódio para precipitar LT-CuCN puro como um pó amarelo pálido.
- 2 CuSO 4 + NaHSO 3 + H 2 O + 2 NaCN → 2 CuCN + 3 NaHSO 4
Com a adição de bissulfito de sódio, a solução de sulfato de cobre muda de azul para verde, momento em que o cianeto de sódio é adicionado. A reação é realizada em condições moderadamente ácidas. O cianeto de cobre tem sido historicamente preparado pelo tratamento de sulfato de cobre (II) com cianeto de sódio , nesta reação redox, o cianeto de cobre (I) se forma junto com o cianogênio :
- 2 CuSO 4 + 4 NaCN → 2 CuCN + (CN) 2 + 2 Na 2 SO 4
Porque esta rota sintética produz cianogênio , usa dois equivalentes de cianeto de sódio por equivalente de CuCN feito e o cianeto de cobre resultante é impuro, não é o método de produção industrial. A semelhança dessa reação com aquela entre o sulfato de cobre e o iodeto de sódio para formar o iodeto de cobre (I) é um exemplo de íons cianeto que atuam como um pseudo-haleto. Também explica por que o cianeto de cobre (II), Cu (CN) 2 , não foi sintetizado.
Reações
O cianeto de cobre é insolúvel em água, mas se dissolve rapidamente em soluções contendo CN - para formar [Cu (CN) 3 ] 2− e [Cu (CN) 4 ] 3− , que exibem geometria de coordenação trigonal planar e tetraédrica, respectivamente. Esses complexos contrastam com os de cianetos de prata e ouro, que formam íons [M (CN) 2 ] - em solução. O polímero coordenação KCU (CN) 2 contém [Cu (CN) 2 ] - unidades, que ligam entre si formando cadeias aniónicos helicoidais.
O cianeto de cobre também é solúvel em amônia aquosa concentrada, piridina e N-metilpirrolidona.
Formulários
O cianeto cuproso é usado para galvanoplastia de cobre.
Síntese orgânica
CuCN é um reagente proeminente na química de organocobre . Ele reage com reagentes de organolítio para formar "cupratos mistos" com as fórmulas Li [RCuCN] e Li 2 [R 2 CuCN]. O uso de CuCN revolucionou a implantação de reagentes organocobre mais simples do tipo CuR e LiCuR 2 , os chamados reagentes de Gilman . Na presença de cianeto, esses cupratos mistos são mais prontamente purificados e mais estáveis.
Os cupratos mistos Li [RCuCN] e Li 2 [R 2 CuCN] funcionam como fontes de carbânions R - , mas com reatividade diminuída em comparação com o reagente organolítio original. Assim, eles são úteis para adições de conjugados e algumas reações de deslocamento.
CuCN também forma reagentes silil e estanil, que são usados como fontes de R 3 Si - e R 3 Sn - .
CuCN é usado na conversão de halogenetos de arila em nitrilos.
CuCN também foi introduzido como uma fonte eletrofílica moderada de nitrila sob condições oxidativas, por exemplo, aminas secundárias, bem como sulfetos e dissulfetos foram eficientemente cianados usando esta metodologia. Esta última metodologia foi então introduzida em uma reação do componente dominó 3, resultando em 2-aminobentiazóis.