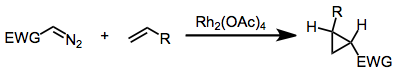Ciclopropanação - Cyclopropanation
Ciclopropanação refere-se a qualquer processo químico que gera anéis de ciclopropano . É um processo importante na química moderna, visto que muitos compostos úteis apresentam esse motivo; por exemplo, piretróides e vários antibióticos quinolona ( ciprofloxacina , esparfloxacina , etc.). No entanto, a alta tensão do anel presente nos ciclopropanos os torna difíceis de produzir e geralmente requerem o uso de espécies altamente reativas, como carbenos , ilídeos e carbânions . Muitas das reações ocorrem de maneira queletrópica .
Abordagens
A partir de alcenos usando reagentes carbenoides
Existem vários métodos para converter alcenos em anéis de ciclopropano usando reagentes do tipo carbeno . Como os próprios carbenos são altamente reativos, é comum que sejam usados em uma forma estabilizada, chamada de carbenóide .
Reação de Simmons-Smith
Na reação de Simmons-Smith, o carbenóide reativo é o iodeto de iodometilzinco , que é normalmente formado por uma reação entre o diiodometano e um par zinco-cobre . Modificações envolvendo alternativas mais baratas foram desenvolvidas, como dibromometano ou diazometano e iodeto de zinco . A reatividade do sistema também pode ser aumentada trocando o par zinco-cobre por dietilzinco . Versões assimétricas são conhecidas.
Usando compostos diazo
Certos compostos diazo , como o diazometano , podem reagir com olefinas para produzir ciclopropanos em 2 etapas. A primeira etapa envolve uma cicloadição 1,3-dipolar para formar uma pirazolina que então sofre desnitrogenação, seja fotoquimicamente ou por decomposição térmica , para dar ciclopropano. A rota térmica, que costuma usar KOH e platina como catalisadores, também é conhecida como a síntese de ciclopropano de Kishner, em homenagem ao químico russo Nikolai Kischner, e também pode ser realizada usando hidrazina e compostos de carbonila α, β-insaturados . O mecanismo de decomposição tem sido o assunto de vários estudos e permanece um tanto controverso, embora seja amplamente considerado que ocorre por meio de uma espécie diradical. Em termos de química verde, este método é superior a outras ciclopropanações baseadas em carbeno; pois não envolve metais ou reagentes halogenados, e produz apenas N 2 como subproduto. No entanto, a reação pode ser perigosa, pois quantidades residuais de compostos diazo não reagidos podem explodir durante o rearranjo térmico da pirazolina.
Usando compostos diazo com catálise de metal
O metilfenildiazoacetato e muitos derivados diazo relacionados são precursores de carbenos aceitadores doadores , que podem ser usados para ciclopropanação ou para inserir em ligações CH de substratos orgânicos. Essas reações são catalisadas por tetraacetato de diródio ou, mais espetacularmente, derivados quirais relacionados.
Usando carbenos livres
Carbenos livres podem ser empregados para reações de ciclopropanação, no entanto, há um escopo limitado para isso, pois poucos podem ser produzidos convenientemente e quase todos são instáveis (ver: dimerização de carbeno ). Uma excepção são dihalocarbenes tais como dichlorocarbene ou dif luorocarbeno , que são razoavelmente estáveis e irão reagir para formar geminais di-halogeno-ciclopropanos. Esses compostos podem então ser usados para formar alenos por meio do rearranjo de Skattebøl .
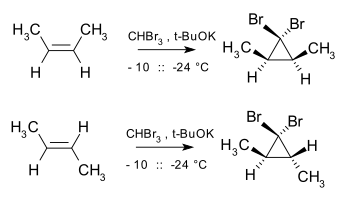
A reação de expansão do anel de Buchner também envolve a formação de um carbeno estabilizado. A ciclopropanação é também estereoespecífica como a adição de carbeno e carbenoids para alcenos é uma forma de uma reação quelotrópica , com a adição ter lugar em um syn maneira. Por exemplo, dibromocarbeno e cis -2-buteno produzem cis -2,3-dimetil-1,1-dibromociclopropano, enquanto o isômero trans produz exclusivamente o trans ciclopropano.
De alcenos usando ilídeos
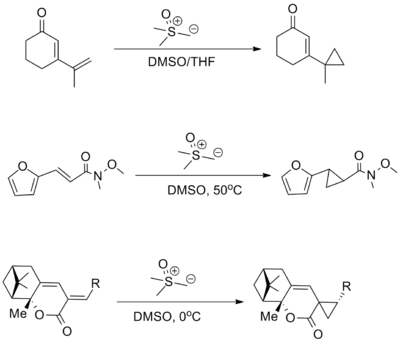
Os ciclopropanos podem ser gerados usando um ileto de enxofre na reação de Johnson-Corey-Chaykovsky , no entanto, esse processo é amplamente limitado ao uso em olefinas pobres em elétrons, particularmente compostos de carbonila α, β-insaturados .
Ciclização intramolecular
Os ciclopropanos podem ser obtidos por uma variedade de reações de ciclização intramolecular . Um método simples é usar haloalcanos primários contendo grupos de retirada de elétrons apropriadamente posicionados. O tratamento com uma base forte irá gerar um carbânion que se ciclizará de forma 3-exo-trigonométrica , com deslocamento do haleto. Os exemplos incluem a formação de cianeto de ciclopropil e ciclopropilacetileno. Este mecanismo também forma a base do rearranjo de Favorskii .
Um processo relacionado é a ciclização de 1,3-dibromopropano por meio de um acoplamento de Wurtz . Isso foi usado para a primeira síntese de ciclopropano por August Freund em 1881. Originalmente, essa reação era realizada usando sódio, no entanto, o rendimento pode ser melhorado trocando-o por zinco .
- BrCH 2 CH 2 CH 2 Br + 2 Na → (CH 2 ) 3 + 2 NaBr
Outras abordagens
- A reação de Kulinkovich forma ciclopropanóis por meio de uma reação entre ésteres e reagentes de Grignard na presença de um alcóxido de titânio.
- A reação de Bingel é uma reação de ciclopropanação especializada usada para funcionalizar um fulereno .
- No rearranjo di-pi-metano, a estimulação fotoquímica faz com que 1,4-dienos se reorganizem para formar vinilciclopropanos. Estes podem então sofrer rearranjos de vinilciclopropano
- Ciclopropano-acil-fosfolipídio sintase graxo realiza ciclopropanação em sistemas biológicos
Biossíntese

Embora os ciclopropanos sejam relativamente raros em bioquímica, muitas vias de ciclopropanação foram identificadas na natureza. As vias mais comuns envolvem reações de fechamento do anel de carbocations nos terpenóides . Os ácidos graxos do ciclopropano são derivados do ataque da S-adenosilmetionina (SAM) aos ácidos graxos insaturados. O precursor do hormônio etileno , ácido 1-aminociclopropano-1-carboxílico, é derivado diretamente de SMM via deslocamento nucleofílico intramolecular do grupo SMe 2 subsequente à condensação com fosfato de piridoxal . A transferência direta de carbeno de diazoésteres para olefinas também foi alcançada por meio de biocatálise in vitro usando variantes de engenharia da enzima citocromo P450 de Bacillus megaterium que foram otimizadas por evolução direcionada .